推 奨
・再発リスクが高くかつ十分な骨髄機能を有する症例には,原発乳癌術後化学療法としてG―CSF併用のdose―dense化学療法を行うことを強く推奨する。
〔推奨の強さ:1,エビデンスの強さ:強,合意率:92%(11/12)〕
背景・目的
Norton-Simonの仮説1)に基づき化学療法の投与間隔を短縮したdose-dense(DD)化学療法が,術後化学療法において有用であるか検討した。
解 説
術後DD化学療法に関する比較試験は複数報告されている。DD化学療法は広義にはG-CSFの併用なしに薬剤量を減らし投与間隔を短縮したものも含まれるが,狭義には薬剤の種類や投与量が同じでG-CSF併用で投与間隔を短くした方法である。本CQにおいては,化学療法の投与期間短縮の有用性を適切に評価することを目的に,対照群と介入群で同じ薬剤が同量投与されているランダム化比較試験(RCT)を用いてメタアナリシスを行った。
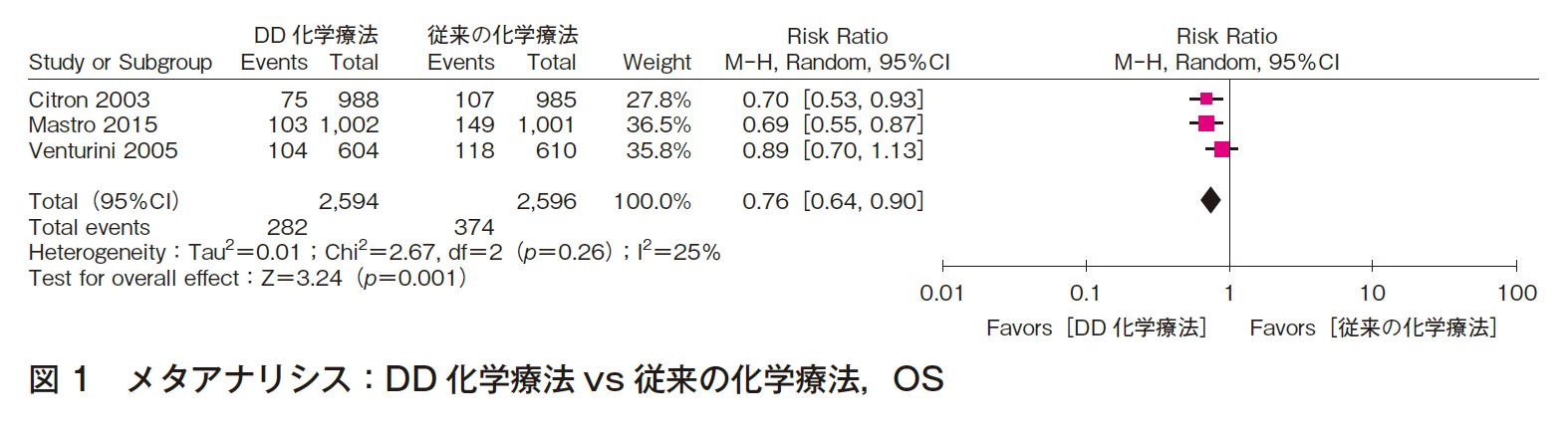
RCTが3つ報告されており,このうち2つはリンパ節転移陽性症例のみを対象とし,1つはリンパ節転移陰性症例も対象に含んでいた。投与薬剤は,Citronら2)はドキソルビシン,シクロホスファミド,パクリタキセルを,Venturiniら3)はFEC療法(5-FU,エピルビシン,シクロホスファミド併用)を,Del Mastroら4)はFEC療法もしくはEC療法とパクリタキセルを用いている。メタアナリシスの結果から,OSはリスク比(RR)0.76(95%CI 0.64-0.90)と有意にDD化学療法で予後を改善した(図1)。DFSもリスク比0.83(95%CI 0.75-0.91)と有意にDD化学療法で改善を認めていた。データの異質性に問題はなく,エビデンスの強さを「強」とした。害に関するアウトカムは,評価可能な2つのRCTでメタアナリシスを行った。Grade 3以上の白血球減少もしくは好中球減少については,介入群で有意にリスクが減少した(RR 0.29,95%CI 0.18-0.48)。介入群のDD化学療法では予防的なG-CFSの使用が必須とされていたが,対照群では必須とされていなかったことが要因と考えられる。貧血(ヘモグロビン8未満への低下)は対照群0.4%,介入群2%(RR 4.56,95%CI 2.01-10.34)とDD化学療法でリスクが上昇する。血小板低下(5万未満)についてはリスクの上昇を認めない。非血液毒性についてはメタアナリシスでの評価は不可能であったが,悪心・嘔吐については各々のRCTの結果では介入群で増加は認めていない。
益と害のバランスについては,貧血のリスクは上昇するものの発症頻度は2%であり,予後が改善することから「益が勝る」といえる。患者の希望は,予防的G-CSFによる費用負担と通院頻度の増加があるため,一貫しているとは言い難く,ばらつきが大きいと判断した。
以上より,エビデンスの程度,益と害のバランス,患者の希望などを勘案し,推奨は「再発リスクが高くかつ十分な骨髄機能を有する症例には,原発乳癌術後化学療法としてG-CSF併用のdose―dense化学療法を行うことを強く推奨する」とした。
検索キーワード・参考にした二次資料
PubMedで“Breast Neoplasms”,“dose dense”のキーワードで検索した。医中誌・Cochrane Libraryも同等のキーワードで検索した。検索期間は2016年11月までとし,205件がヒットした。その中で本CQの主旨に合致する1編のシステマティック・レビュー5)の記載のある2編の論文と,ハンドサーチで本CQの主旨に合致する1編の論文から定性的および定量的システマティック・レビューを行った。
エビデンス総体・システマティックレビュー・メタアナリシス
参考文献
1)Norton L, Simon R. Tumor size, sensitivity to therapy, and design of treatment schedules. Cancer Treat Rep. 1977;61(7):1307―17. [PMID:589597]
2)Citron ML, Berry DA, Cirrincione C, Hudis C, Winer EP, Gradishar WJ, et al. Randomized trial of dose―dense versus conventionally scheduled and sequential versus concurrent combination chemotherapy as postoperative adjuvant treatment of node―positive primary breast cancer:first report of Intergroup Trial C9741/Cancer and Leukemia Group B Trial 9741. J Clin Oncol. 2003;21(8):1431―9. [PMID:12668651]
3)Venturini M, Del Mastro L, Aitini E, Baldini E, Caroti C, Contu A, et al. Dose―dense adjuvant chemotherapy in early breast cancer patients:results from a randomized trial. J Natl Cancer Inst. 2005;97(23):1724―33. [PMID:16333028]
4)Del Mastro L, De Placido S, Bruzzi P, De Laurentiis M, Boni C, Cavazzini G, et al;Gruppo Italiano Mammella(GIM)investigators. Fluorouracil and dose―dense chemotherapy in adjuvant treatment of patients with early―stage breast cancer:an open―label, 2×2 factorial, randomised phase 3 trial. Lancet. 2015;385(9980):1863―72. [PMID:25740286]
5)Lemos Duarte I, da Silveira Nogueira Lima JP, Passos Lima CS, Deeke Sasse A. Dose―dense chemotherapy versus conventional chemotherapy for early breast cancer:a systematic review with meta―analysis. Breast. 2012;21(3):343―9. [PMID:22425607]


