推 奨
・原発乳癌の術後薬物療法で,静注化学療法の代わりに,経口フッ化ピリミジンの投与を行わないことを弱く推奨する。
〔推奨の強さ:3,エビデンスの強さ:弱,合意率:92%(11/12)〕
背景・目的
術後化学療法として,標準的な静注化学療法に替えて経口フッ化ピリミジンによる治療を行うことの有用性について検討した。
解 説
術後化学療法として,静注化学療法と経口フッ化ピリミジン〔UFT(テガフール・ウラシル),カペシタビン〕のランダム化比較試験は,現在までに4つ報告されている。UFTを用いた試験は以下の3試験である。まず,JCOG 9404試験1)は閉経前リンパ節転移陽性症例を対象としてAC療法(ドキソルビシン,シクロホスファミド)と比較し,N-SAS BC01試験2)は高リスク・リンパ節転移陰性症例を対象としてCMF療法(シクロホスファミド,メトトレキサート,5-FU)と比較し,CUBC試験3)はリンパ節転移陽性症例を対象としてCMFと比較した。カペシタビンを用いた試験であるCALGB 49907試験4)は65歳以上の高齢者を対象にACまたはCMFと比較検討した。
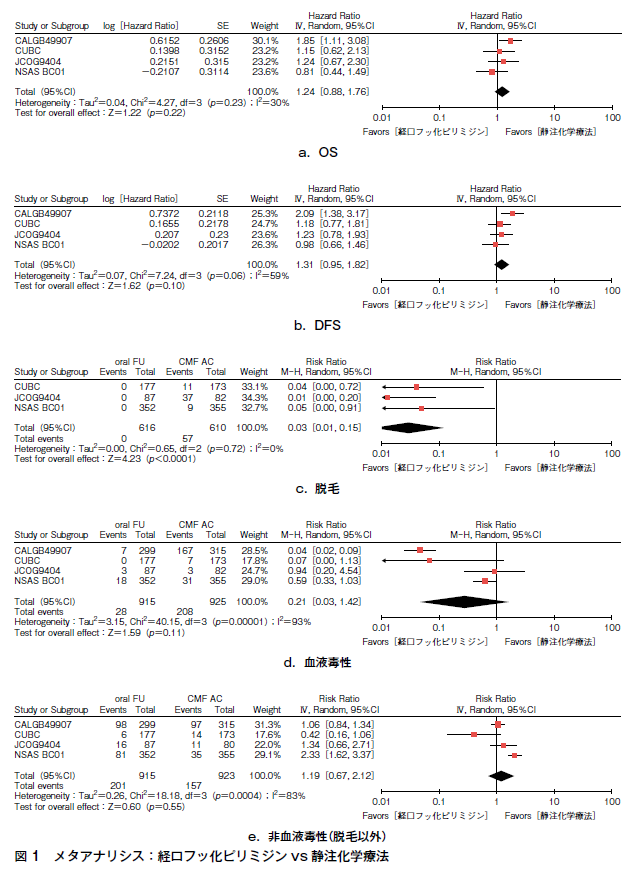
これら4試験を対象にメタアナリシスを行った結果,OSのハザード比は1.24(95%CI 0.88-1.76)(図1a)であり,DFSのハザード比は1.31(95%CI 0.95-1.82)(図1b)と,いずれも両群間に有意な差は認めなかった。有害事象の一つである脱毛は,リスク比0.03(95%CI 0.01-0.15)(図1c)と経口フッ化ピリミジン群で有意に少なかった。血液毒性はリスク比0.21(95%CI 0.03-1.42)(図1d)と経口フッ化ピリミジン群で低い傾向にある。脱毛を除く非血液毒性(G3以上)はリスク比1.19(95%CI 0.67-2.12)(図1e)と,両群間に有意な差を認めなかった。また,メタアナリシスの結果,脱毛以外の有害事象はばらつきが大きい(異質性が高い)ことがわかった。以上を考慮して,エビデンスの強さは「弱」とした。
乳癌診療ガイドラインの推奨決定会議において,今回対象とした4試験では,現在の標準的化学療法である,アンスラサイクリン系薬剤からタキサン系薬剤の順次投与や,TC療法(ドセタキセル,シクロホスファミド)が含まれないことから,アジュバント療法としてこれらの標準的化学療法の適応となる患者に対して,経口フッ化ピリミジンが代替となるとはいえない(外的妥当性が低い)ことが問題点として挙げられた。
益に関するアウトカムとして設定したOSとDFSの結果は,両群に有意差は認めなかったものの,経口フッ化ピリミジンで劣る傾向にあった。また,経口フッ化ピリミジンのその他の有害事象として色素沈着や下痢があり,カペシタビンの有害事象として手足症候群などが挙げられる。一方で,UFTはCMFより治療中のQOLは優れるとの報告もある2)。以上より,経口フッ化ピリミジンを術後化学療法として用いる場合の益と害のバランスの差は小さい(益が大きいとはいえない)と考えた。
経口療法の利便性や脱毛の回避などといった経口フッ化ピリミジンのメリットはあるものの,根治を目指す治療に伴う脱毛に関しては,患者の嗜好に実際には大きなばらつきがある。さらに,実際の診療現場において,今回のメタアナリシスにおけるOSおよびDFSの結果や,解析対象となった4試験において現在の標準的化学療法がコントロール群となっていないことなどを患者に説明した場合,術後薬物療法としての経口フッ化ピリミジンに対する患者の希望は必ずしも一致しないと考えられた。
以上の議論を踏まえて行われた推奨決定会議での投票の結果は,経口フッ化ピリミジンを「行うことを弱く推奨する」が8%,「行わないことを弱く推奨する」が92%であった。
以上より,エビデンスの程度,益と害のバランス,患者の希望などを勘案し,推奨は「原発乳癌の術後薬物療法で,静注化学療法の代わりに,経口フッ化ピリミジンの投与を行わないことを弱く推奨する」とした。
検索キーワード・参考にした二次資料
PubMedで“Breast Neoplasms”,“Chemotherapy, Adjuvant”,“fluorouracil”,“cape citabine”のキーワードで検索した。医中誌・Cochrane Libraryも同等のキーワードで検索した。検索期間は2016年11月までとし,1,456件がヒットした。一次スクリーニングで11編,二次スクリーニングで4編の論文が抽出され,定性的および定量的システマティック・レビューを行った。
エビデンス総体・システマティックレビュー・メタアナリシス
参考文献
1)Shien T, Iwata H, Fukutomi T, Inoue K, Aogi K, Kinoshita T, et al. Tamoxifen plus tegafur―uracil(TUFT)versus tamoxifen plus Adriamycin(doxorubicin)and cyclophosphamide(ACT)as adjuvant therapy to treat node―positive premenopausal breast cancer(PreMBC):results of Japan Clinical Oncology Group Study 9404. Cancer Chemother Pharmacol. 2014;74(3):603―9. [PMID:25055938]
2)Watanabe T, Sano M, Takashima S, Kitaya T, Tokuda Y, Yoshimoto M, et al. Oral uracil and tegafur compared with classic cyclophosphamide, methotrexate, fluorouracil as postoperative chemotherapy in patients with node―negative, high―risk breast cancer:National Surgical Adjuvant Study for Breast Cancer 01 Trial. J Clin Oncol. 2009;27(9):1368―74. [PMID:19204202]
3)Park Y, Okamura K, Mitsuyama S, Saito T, Koh J, Kyono S, et al. Uracil―tegafur and tamoxifen vs cyclophosphamide, methotrexate, fluorouracil, and tamoxifen in post―operative adjuvant therapy for stage I, II, or IIIA lymph node―positive breast cancer:a comparative study. Br J Cancer. 2009;101(4):598―604. [PMID:19638976]