推 奨
・有子宮女性への合成黄体ホルモンを用いたエストロゲン+黄体ホルモン併用療法では,長期投与により乳癌発症リスクを増加させる。
〔エビデンスグレード:Probable(ほぼ確実)〕・子宮摘出後女性へのエストロゲン単独療法では,短期投与においては乳癌発症リスクは増加しない。
〔エビデンスグレード:Probable(ほぼ確実)〕
背景・目的
閉経後女性ホルモン補充療法〔(menopausal)hormone therapy;(M)HTあるいはhormone replacement therapy;HRT〕とは「エストロゲン欠乏に伴う諸症状や疾患の予防ないし治療を目的に考案された療法で,エストロゲン製剤を投与する治療の総称」であり,有子宮者に対しては子宮内膜癌を予防するためにエストロゲン+黄体ホルモン併用療法(combined estrogen—progestogen therapy;EPT)が,一方,子宮摘出後女性にはエストロゲン単独療法(estrogen therapy;ET)が施行される。
HRTは自然閉経か外科的閉経かを問わず,症状を有する閉経後女性に対する治療の第一選択として考慮すべきであると考えられているが,従来,最も懸念される有害事象として,エストロゲンに依存する組織の癌,特に乳癌発症のリスク増加が議論されてきた。
解 説
HRT施行の益のアウトカムとして更年期障害・卵巣欠落症状改善効果(重要度8点),骨量改善効果(重要度6点)と循環器疾患リスク低減効果(重要度6点),また,害のアウトカムとして有子宮者の性器出血(重要度4点)と乳癌発症リスク(重要度9点)を設定した。
HRTは自然閉経後あるいは両側卵巣摘出術後の外科的閉経,放射線治療後の女性における更年期障害や卵巣欠落症状,脂質異常症,骨粗鬆症などの退行期疾患はもちろんのこと,皺の改善などの皮膚領域,メタボリック症候群などの代謝性疾患などいわゆるアンチエイジングとしての効果も期待できることが知られている(二次資料①)。実際,更年期障害に対しては,メタアナリシスにおいてHRTによりホットフラッシュの回数が有意に減少することが示されており1),ランダム化比較試験(RCT)において健康関連QOLや各種症状が有意に改善することが報告されている2)3)。日本における検討においても,RCTにてホットフラッシュの回数が有意に減少することが報告されている4)。骨量については,メタアナリシスにおいてHRTは骨量を有意に増加させることが報告されており5)6),日本におけるRCTにおいてもプラセボと比較して有意に骨量を増加させていた7)。また,骨折リスクについても,メタアナリシスにおいてリスクを有意に減少させることが報告されており8),2016年に発表された閉経や内分泌に関連した7つの国際学会のHRTに関する共同コンセンサスにおいても,HRTは閉経後女性の大腿骨近位部や椎体,その他の部位の骨粗鬆症に関連した骨折リスクを有意に減少させると述べられている(二次資料②)。心血管系への効果については,全体としては,死亡をエンドポイントとした場合,一次予防としても,二次予防としてもリスク軽減効果がないことがメタアナリシスから明らかになっているが9),いわゆるタイミング仮説として,閉経後10年以内や60歳未満での施行ではリスクが減少することが示されている9)10)。以上のことから,HRTは症状を有する閉経後女性に対する治療の第一選択として考慮すべきであると考えられている。
一方,害としての性器出血については,有子宮女性に対するEPTにおいては30~40%に出血を認め,4つのRCTのメタアナリシスを行うと,プラセボ投与と比較して約8倍と出血リスクが有意に増加していた11)~14)。
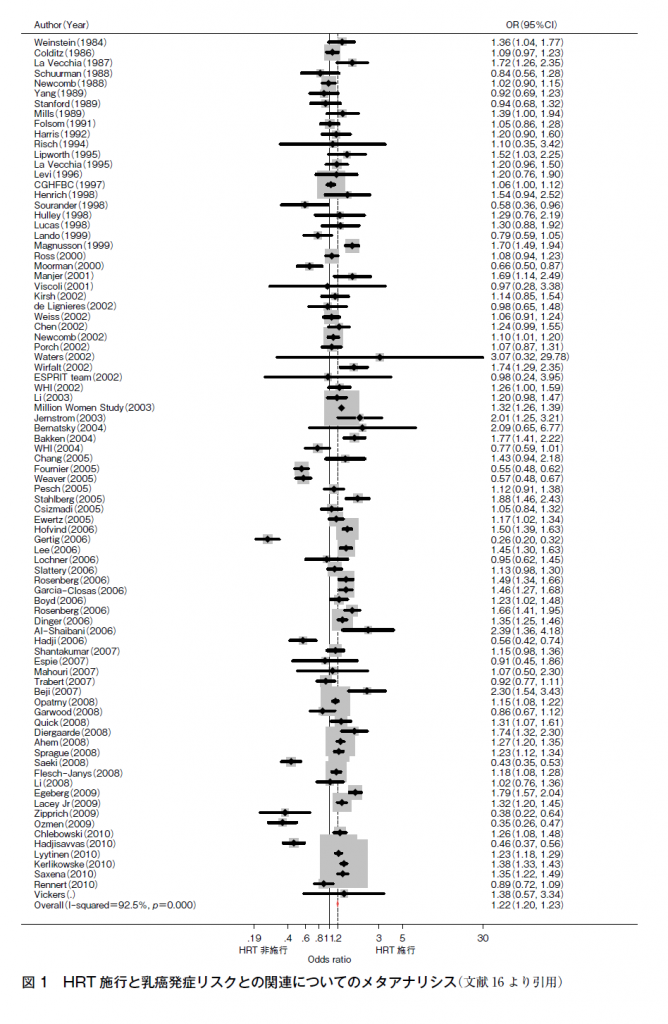
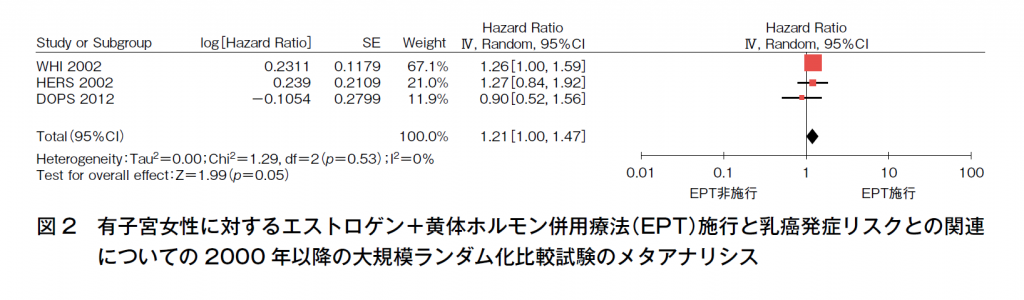
HRTと乳癌発症リスクについては1980年代から議論されてきた。有子宮女性へのEPTについては,米国における大規模RCTであるWomen’s Health Initiative(WHI)試験の中間解析の結果(平均観察期間5.2年),結合型エストロゲン(CEE)+酢酸メドロキシプロゲステロン(MPA)投与群(E+P群)はプラセボ群と比較し,乳癌発症リスクのハザード比(HR)が1.26(95%CI 1.00-1.59)と有意な乳癌発症リスクの増加が認められていた15)。また,2011年1月までの34研究のメタアナリシスではHRT全体としてオッズ比(OR)1.22(95%CI 1.20-1.23)(図1),有子宮者へのEPTではOR 1.33(95%CI 1.30—1.36)と報告されており16),2000年以降の大規模研究のメタアナリシスを行うと,3つのRCTからはHR 1.21(95%CI 1.00-1.47)(図2)15)17)18),4つのコホート研究からは相対リスク(RR)1.54(95%CI 1.40-1.69)19)~22)とともに有意な増加を認めていたことから,有子宮者に対するエストロゲン+黄体ホルモン併用療法では乳癌発症リスクを増加させると考えられる。しかし,このリスクは1000人・年の使用に対して増加は1.0未満であり,2016年に発表された閉経あるいは内分泌に関係する7つの学会によるHRTに関する国際的なコンセンサスにおいては「乳癌リスクに及ぼすHRTの影響は小さく,座ってばかりのライフスタイルや肥満,アルコール摂取といった一般的な要因による増加と同等かそれよりも低い」とされている(二次資料②)。また,WHI研究でも中間解析まではリスクに有意差はなく15),HRT施行期間が延長するとリスクが増加することが報告されており23),施行期間がリスクに関連していると考えられている。一方,このリスクはHRT中止後には3~5年でリスクの増加は消失する24)。さらに,併用される黄体ホルモンの種類により,リスクに差異があることも知られている。MPAをはじめとする,現在わが国でHRTに利用できる合成黄体ホルモンはすべてリスクを増加させ,種類による差異は認めないが,天然型プロゲステロン(日本未発売)やその立体異性体であるジドロゲステロンではリスクを増加させないことが報告されている25)26)。また,周期的同時投与法よりも持続的同時併用投与法のほうがリスクが高いという報告や,経口薬よりも経皮薬のほうがリスクが低いという報告もあること,閉経からHRT開始までの期間を示すgap timeが5年以上では5年未満と比較して有意にリスクが減少すること24)も報告されており,EPTのレジメンによって乳癌発症リスクは異なると考えられる。
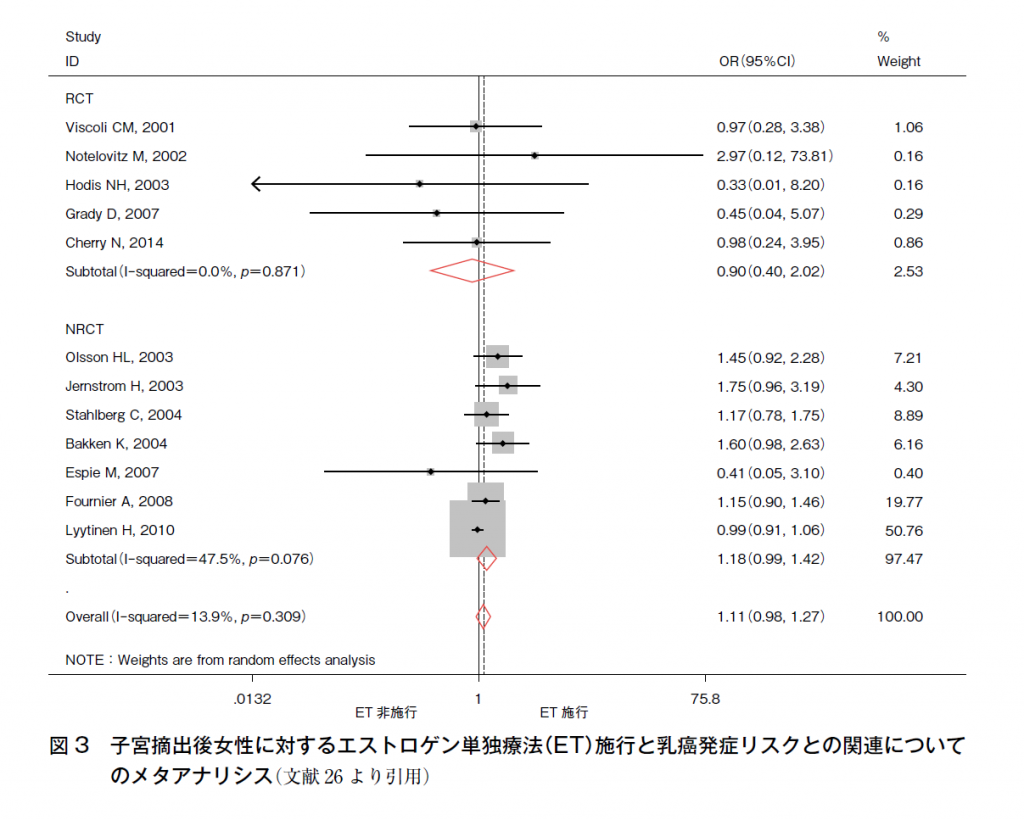
一方,子宮摘出後女性に対するETについては,WHI研究におけるエストロゲン単独試験において,6.8年時ではHR 0.77(95%CI 0.59-1.01)と有意差はないものの乳癌発症リスクの減少が認められ27),同研究のフォローアップにおいては,中央値として5.9年のCEE投与にて中止後平均7.1年,試験開始から中央値で11.8年における乳癌発症リスクの検討にてHR 0.77(95%CI 0.62-0.95)とプラセボと比較して有意に減少していたことから28),子宮摘出者における5年間程度のETは乳癌罹患リスクを増加させることはなく,むしろ減少させる可能性が示唆されている。12研究のメタアナリシスにおいては1.11(95%CI 0.98-1.27)(図3)26)と有意差を認めず,ETは少なくとも短期投与においては,乳癌発症リスクは増加させないと考えられる。
日本人を対象とした検討では,症例対照研究においてはHRTによる乳癌発症リスクはRR 0.432(95%CI 0.352-0.530)と少なくともリスクの増加を認めてはいない29)。また,日本人を対象としたコホート研究でもリスクの増加は認められなかった30)。
検索キーワード
検索はPubMedにて,“Breast Neoplasms”,“Hormone Replacement Therapy”,“Estrogen”,“Risk”のキーワードを,また,医中誌にて,乳房腫瘍,ホルモン補充療法,リスクのキーワードを用いて検索した。検索期間は2000年1月~2017年4月とした。該当文献としてPubMed 1,438件,医中誌157件の計1,595件およびその参考文献から論文をリストアップした。原文査読により一次資料として30件,二次資料として2件,合計32件の文献を選択し,引用した。
参考にした二次資料
① 日本産科婦人科学会,日本女性医学学会.ホルモン補充療法ガイドライン2017年度版.東京,日本産科婦人科学会,2017.
② de Villiers TJ, Hall JE, Pinkerton JV, Cerdas Perez S, Rees M, Yang C, et al. Revised Global Consensus Statement on Menopausal Hormone Therapy. Climacteric. 2016;19(4):313—5. [PMID:27322027]
参考文献
1)Maclennan AH, Broadbent JL, Lester S, Moore V. Oral oestrogen and combined oestrogen/progestogen therapy versus placebo for hot flushes. Cochrane Database Syst Rev. 2004;(4):CD002978. [PMID:15495039]
2)Welton AJ, Vickers MR, Kim J, Ford D, Lawton BA, MacLennan AH, et al;WISDOM team. Health related quality of life after combined hormone replacement therapy:randomised controlled trial. BMJ. 2008;337:a1190. [PMID:18719013]
3)Santoro N, Allshouse A, Neal—Perry G, Pal L, Lobo RA, Naftolin F, et al. Longitudinal changes in menopausal symptoms comparing women randomized to low—dose oral conjugated estrogens or transdermal estradiol plus micronized progesterone versus placebo:the Kronos Early Estrogen Prevention Study. Menopause. 2017;24(3):238—46. [PMID:27779568]
4)Honjo H, Taketani Y. Low—dose estradiol for climacteric symptoms in Japanese women:a randomized, controlled trial. Climacteric. 2009;12(4):319—28. [PMID:19330598]
5)Wells G, Tugwell P, Shea B, Guyatt G, Peterson J, Zytaruk N, et al;Osteoporosis Methodology Group and The Osteoporosis Research Advisory Group. Meta—analyses of therapies for postmenopausal osteoporosis. V. Meta—analysis of the efficacy of hormone replacement therapy in treating and preventing osteoporosis in postmenopausal women. Endocr Rev. 2002;23(4):529—39. [PMID:12202468]
6)Abdi F, Mobedi H, Bayat F, Mosaffa N, Dolatian M, Ramezani Tehrani F. The effects of transdermal estrogen delivery on bone mineral density in postmenopausal women:A meta—analysis. Iran J Pharm Res. 2017;16(1):380—9. [PMID:28496491]
7)Mizunuma H, Taketani Y, Ohta H, Honjo H, Gorai I, Itabashi A, et al. Dose effects of oral estradiol on bone mineral density in Japanese women with osteoporosis. Climacteric. 2010;13(1):72—83. [PMID:19591010]
8)Torgerson DJ, Bell—Syer SE. Hormone replacement therapy and prevention of vertebral fractures:a meta—analysis of randomised trials. BMC Musculoskelet Disord. 2001;2:7. [PMID:11716794]
9)Boardman HM, Hartley L, Eisinga A, Main C, Roqué i Figuls M, Bonfill Cosp X, et al. Hormone therapy for preventing cardiovascular disease in post—menopausal women. Cochrane Database Syst Rev. 2015;(3):CD002229. [PMID:25754617]
10)Salpeter SR, Cheng J, Thabane L, Buckley NS, Salpeter EE. Bayesian meta—analysis of hormone therapy and mortality in younger postmenopausal women. Am J Med. 2009;122(11):1016—22. e1. [PMID:19854329]
11)Lin SQ, Sun LZ, Lin JF, Yang X, Zhang LJ, Qiao J, et al. Estradiol 1 mg and drospirenone 2 mg as hormone replacement therapy in postmenopausal Chinese women. Climacteric. 2011;14(4):472—81. [PMID:21469973]
12)Lindenfeld EA, Langer RD. Bleeding patterns of the hormone replacement therapies in the postmenopausal estrogen and progestin interventions trial. Obstet Gynecol. 2002;100(5 Pt 1):853—63. [PMID:12423841]
13)Simon JA, Liu JH, Speroff L, Shumel BS, Symons JP. Reduced vaginal bleeding in postmenopausal women who receive combined norethindrone acetate and low—dose ethinyl estradiol therapy versus combined conjugated equine estrogens and medroxyprogesterone acetate therapy. Am J Obstet Gynecol. 2003;188(1):92—9. [PMID:12548201]
14)Vickers MR, MacLennan AH, Lawton B, Ford D, Martin J, Meredith SK, et al. Main morbidities recorded in the women’s international study of long duration oestrogen after menopause(WISDOM):a randomised controlled trial of hormone replacement therapy in postmenopausal women. BMJ. 2007;335(7613):239. [PMID:17626056]
15)Rossouw JE, Anderson GL, Prentice RL, LaCroix AZ, Kooperberg C, Stefanick ML, et al;Writing Group for the Women’s Health Initiative Investigators. Risks and benefits of estrogen plus progestin in healthy postmenopausal women:principal results From the Women’s Health Initiative randomized controlled trial. JAMA. 2002;288(3):321—33. [PMID:12117397]
16)Anothaisintawee T, Wiratkapun C, Lerdsitthichai P, Kasamesup V, Wongwaisayawan S, Srinakarin J, et al. Risk factors of breast cancer:a systematic review and meta—analysis. Asia Pac J Public Health. 2013;25(5):368—87. [PMID:23709491]
17)Hulley S, Furberg C, Barrett—Connor E, Cauley J, Grady D, Haskell W, et al;HERS Research Group. Noncardiovascular disease outcomes during 6.8 years of hormone therapy:Heart and Estrogen/progestin Replacement Study follow—up(HERS II). JAMA. 2002;288(1):58—66. [PMID:12090863]
18)Schierbeck LL, Rejnmark L, Tofteng CL, Stilgren L, Eiken P, Mosekilde L, et al. Effect of hormone replacement therapy on cardiovascular events in recently postmenopausal women:randomised trial. BMJ. 2012;345:e6409. [PMID:23048011]
19)Chen WY, Colditz GA, Rosner B, Hankinson SE, Hunter DJ, Manson JE, et al. Use of postmenopausal hormones, alcohol, and risk for invasive breast cancer. Ann Intern Med. 2002;137(10):798—804. [PMID:12435216]
20)Beral V;Million Women Study Collaborators. Breast cancer and hormone—replacement therapy in the Million Women Study. Lancet. 2003;362(9382):419—27. [PMID:12927427]
21)Fournier A, Berrino F, Riboli E, Avenel V, Clavel—Chapelon F. Breast cancer risk in relation to different types of hormone replacement therapy in the E3N—EPIC cohort. Int J Cancer. 2005;114(3):448—54. [PMID:15551359]
22)Saxena T, Lee E, Henderson KD, Clarke CA, West D, Marshall SF, et al. Menopausal hormone therapy and subsequent risk of specific invasive breast cancer subtypes in the California Teachers Study. Cancer Epidemiol Biomarkers Prev. 2010;19(9):2366—78. [PMID:20699377]
23)Schairer C, Lubin J, Troisi R, Sturgeon S, Brinton L, Hoover R. Menopausal estrogen and estrogen—progestin replacement therapy and breast cancer risk. JAMA. 2000;283(4):485—91. [PMID:10659874]
24)Beral V, Reeves G, Bull D, Green J;Million Women Study Collaborators. Breast cancer risk in relation to the interval between menopause and starting hormone therapy. J Natl Cancer Inst. 2011;103(4):296—305. [PMID:21278356]
25)Fournier A, Berrino F, Clavel—Chapelon F. Unequal risks for breast cancer associated with different hormone replacement therapies:results from the E3N cohort study. Breast Cancer Res Treat. 2008;107(1):103—11. [PMID:17333341]
26)Yang Z, Hu Y, Zhang J, Xu L, Zeng R, Kang D. Estradiol therapy and breast cancer risk in perimenopausal and postmenopausal women:a systematic review and meta—analysis. Gynecol Endocrinol. 2017;33(2):87—92. [PMID:27898258]
27)Anderson GL, Limacher M, Assaf AR, Bassford T, Beresford SA, Black H, et al;Women’s Health Initiative Steering Committee. Effects of conjugated equine estrogen in postmenopausal women with hysterectomy:the Women’s Health Initiative randomized controlled trial. JAMA. 2004;291(14):1701—12. [PMID:15082697]
28)Anderson GL, Chlebowski RT, Aragaki AK, Kuller LH, Manson JE, Gass M, et al. Conjugated equine oestrogen and breast cancer incidence and mortality in postmenopausal women with hysterectomy:extended follow—up of the Women’s Health Initiative randomised placebo—controlled trial. Lancet Oncol. 2012;13(5):476—86. [PMID:22401913]
29) Saeki T, Sano M, Komoike Y, Sonoo H, Honjyo H, Ochiai K, et al. No increase of breast cancer incidence in Japanese women who received hormone replacement therapy:overview of a case—control study of breast cancer risk in Japan. Int J Clin Oncol. 2008;13(1):8—11. [PMID:18307013]
30)Kawai M, Minami Y, Kuriyama S, Kakizaki M, Kakugawa Y, Nishino Y, et al. Reproductive factors, exogenous female hormone use and breast cancer risk in Japanese:the Miyagi Cohort Study. Cancer Causes Control. 2010;21(1):135—45. [PMID:19816778]
図1 HRT施行と乳癌発症リスクとの関連についてのメタアナリシス(文献16より引用)
図2 有子宮女性に対するエストロゲン+黄体ホルモン併用療法(EPT)施行と乳癌発症リスクとの関連についての2000年以降の大規模ランダム化比較試験のメタアナリシス
図3 子宮摘出後女性に対するエストロゲン単独療法(ET)施行と乳癌発症リスクとの関連についてのメタアナリシス(文献26より引用)