推 奨
・Stage Ⅳ乳癌に対する予後の改善を期待しての原発巣切除を行わないことを弱く推奨する。
〔推奨の強さ:3,エビデンスの強さ:中,合意率100%(12/12)〕
背景・目的
遠隔転移を有する乳癌は治癒が極めて困難であり,治療の目標は症状のコントロール,QOLの改善,生存の延長になる。治療は全身療法(薬物療法)を主に,局所療法(放射線療法・手術療法)を必要に応じて行う。初診時より遠隔転移を有するStage Ⅳ乳癌においては,原発巣の外科的切除により長期生存を得られる可能性を示唆する報告がある。そこで本CQでは,Stage Ⅳ乳癌に対する原発巣切除が予後の改善に寄与するかどうかエビデンスをもとに検討した。
解 説
文献検索を行った2016年11月の時点で,Stage Ⅳ乳癌に対して原発巣切除を行うか否かの前向きランダム化比較試験は,登録が終了したものが4試験〔NCT 00193778試験1),NCT 00557986(MF07―01)試験2),NCT 01242800(ECOG 2108)試験,NCT 01015625(ABCSG-28 POSYTIVE)試験3)〕あり,1つが登録中〔UMIN 000005586(JCOG 1017)試験4)〕である。登録が終了した3試験のうち,インドの単施設で行われた試験1)のみ論文化されており,この結果についてのみ検討を行った。前向き試験の結果が出揃っていないことから,いくつか行われている後ろ向き試験の結果について,前向き試験とは別に定量的および定性的システマティック・レビューを行った。
1)エビデンスの強さ
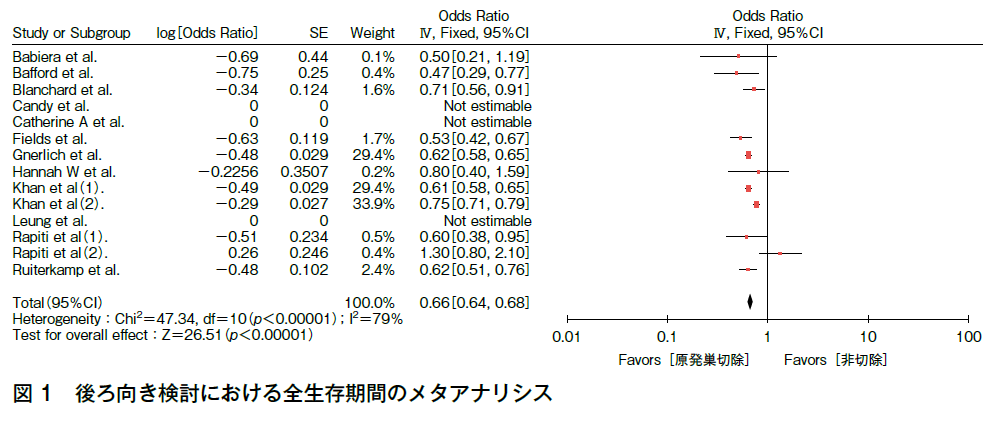
インドから報告された前向き試験(n=350)1)では,Stage Ⅳ乳癌に対して初期薬物療法(CAFまたはCEFが95%)を施行したのち原発巣が切除可能な症例を原発巣切除群と非切除群にランダム化し予後を検討した。その結果,主要評価項目である全生存期間(生存期間中央値:手術群19.2カ月vs非手術群20.5カ月,HR 1.04,95%CI 0.81―1.34,p=0.79)で両群間に有意な差を認めなかった。副次評価項目である局所無増悪期間では手術群で有意な延長効果を認めたものの(中央値:手術群 中央値達せずvs非手術群18.2カ月,HR 0.16,95%CI 0.10―0.26,p<0.0001),遠隔転移無増悪期間では逆に手術群で有意な予後の悪化を認めた(中央値:手術群11.3カ月vs非手術群19.8カ月,HR 1.42,95%CI 1.08―1.85,p=0.012)。これに対して,これまで出されている12編の後ろ向き検討5)~7)のメタアナリシスでは,Stage Ⅳ乳癌に対する原発巣切除は生存期間を改善する結果であった(HR 0.65,p<0.00001)(図1)。遠隔転移無増悪期間に関しては,正確に評価されている後ろ向き試験はほとんどなかった。
今回の検討では1つの前向き試験の結果と多数の後ろ向き検討で逆の結果となった。後ろ向き試験では手術のタイミングや適格基準が詳細に解析できておらず多くのバイアスを含んでおり,正確な検討はできていない。他方,前向き試験ではこれらのバイアスは含まれないものの,インドの単施設での結果であることから,わが国および欧米諸国で標準的に行われている分子標的療法を含んだ全身薬物療法が行われていない。生存期間の遠隔転移増悪期間の中央値が非常に短いことからも,ベースの予後の違いが大きいことが推察される。確固たるエビデンスを得るためには残り3つの前向き試験の結果を待つ必要があると考える。
他方,出血や潰瘍による創部感染は患者のQOLを著しく低下させることがあり,状況によっては手術により改善可能である。しかし,術後合併症の発生や乳房の整容性の低下といった「害」もある。Stage IV乳癌治療の目的を考えると,症状緩和のための原発巣切除は考慮されるべきであるが,全身療法のみでも局所の症状を改善することは可能である。
患者の希望に関しては,原発巣の局所制御が不良でなければ,手術による整容性の低下を避けたい希望と,触知可能な腫瘍を抱えていることの不安が予想され,価値観のばらつきはあると考えられる。
以上より,今あるエビデンスでは,インドと同様の背景をもつStage IV乳癌では原発巣切除により生存期間を延長するのは困難であり,むしろ遠隔転移を悪くする可能性があることから推奨されない。前向き試験の結果ではあるが,今後さらなる検討が行われることを考慮して弱い推奨とした。
2018年5月にトルコから報告されたMF07-01試験8)では、当初の仮説(原発巣切除による3年生存率18%の改善効果)は証明されなかったが、後解析による生存期間中央値は手術群で9か月の延長を認めた(手術群46か月vs非手術群37か月, HR 0.66, 95%CI 0.49-0.88; P=0.005)。一方、ヨーロッパで行われたABCSG-28 POSYTIVE trial3)では、予定の登録数516例のところ90例のみの登録での結果が報告されたが原発巣切除の有意な生存期間延長は認めなかった(生存期間中央値:手術群34.6か月vs 54.8か月 HR 0.691, 95%CI 0.358–1.333; P =0.267)。今回の2つの試験はいずれもStage IV乳癌に対する初期治療としての手術の効果を検討しており、薬物療法を手術の前に行うインドの試験とは対象が異なる。また、生存期間中央値はインドの試験に比べて1年以上も長い。患者背景のばらつきは大きく結果の解釈に注意が必要であるが、この3つの試験の結果のメタアナリシスでは、原発巣切除による生存期間の有意な延長効果は認めなかった。今後、残り2つの試験(JCOG1017, ECOG2108)の結果が待たれる。
図2 前向き試験における全生存期間のメタアナリシス
検索キーワード・参考にした二次資料
PubMedで“Breast Neoplasms”,“Mastectomy”のキーワードと,“stage-Ⅳ”の同義語で検索した。医中誌・Cochrane Libraryも同等のキーワードで検索した。検索期間は2016年11月までとし,465件がヒットした。一次スクリーニングで43編の論文が抽出され,二次スクリーニングで15編の論文が抽出された。うち後ろ向き検討の12編の論文に対して定量的および定性的システマティック・レビューを行った。
エビデンス総体・システマティックレビュー
参考文献
1)Badwe R, Hawaldar R, Nair N, Kaushik R, Parmar V, Siddique S, et al. Locoregional treatment versus no treatment of the primary tumour in metastatic breast cancer:an open―label randomised controlled trial. Lancet Oncol. 2015;16(13):1380―8. [PMID:26363985]
2)Soran A, Ozbas S, Kelsey SF, Gulluoglu BM. Randomized trial comparing locoregional resection of primary tumor with no surgery in stage IV breast cancer at the presentation(Protocol MF07―01):a study of Turkish Federation of the National Societies for Breast Diseases. Breast J. 2009;15(4):399―403. [PMID:19496782]
3) Fitzal F, Bjelic-Radisic V, Knauer M, Steger G, Hubalek M, Balic M, Singer C, et al. Impact of Breast Surgery in Primary Metastasized Breast Cancer: Outcomes of the Prospective Randomized Phase III ABCSG-28 POSYTIVE Trial. Ann Surg. 2018 Apr 24. [Epub ahead of print]
4)Shien T, Nakamura K, Shibata T, Kinoshita T, Aogi K, Fujisawa T, et al. A randomized controlled trial comparing primary tumour resection plus systemic therapy with systemic therapy alone in metastatic breast cancer(PRIM―BC):Japan Clinical Oncology Group Study JCOG1017. Jpn J Clin Oncol. 2012;42(10):970―3. [PMID:22833684]
5)Ruiterkamp J, Voogd AC, Bosscha K, Tjan―Heijnen VC, Ernst MF. Impact of breast surgery on survival in patients with distant metastases at initial presentation:a systematic review of the literature. Breast Cancer Res Treat. 2010;120(1):9―16. [PMID:20012891]
6)Akay CL, Ueno NT, Chisholm GB, Hortobagyi GN, Woodward WA, Alvarez RH, et al. Primary tumor resection as a component of multimodality treatment may improve local control and survival in patients with stage Ⅳ inflammatory breast cancer. Cancer. 2014;120(9):1319―28. [PMID:24510381]
7)Hazard HW, Gorla SR, Scholtens D, Kiel K, Gradishar WJ, Khan SA. Surgical resection of the primary tumor, chest wall control, and survival in women with metastatic breast cancer. Cancer. 2008;113(8):2011―9. [PMID:18780312]
8) Soran A, Ozmen V, Ozbas S, Karanlik H, Muslumanoglu M, Igci A, Canturk Z, et al. Randomized Trial Comparing Resection of Primary Tumor with No Surgery in Stage IV Breast Cancer at Presentation: Protocol MF07-01. Ann Surg Oncol. 2018;25(11):3141-3149. [PMID: 29777404]
図1 後ろ向き検討における全生存期間のメタアナリシス