A
病理検査により,乳房のしこりや分泌物などの原因がどのような病気によるものかを判断します。また,乳がんの場合,その種類や性質,広がりや進行度を明らかにします。病理検査では生検で得られた組織と手術で得られた組織いずれも対象となります。これらにより,その後の手術や薬物療法,放射線療法などの治療方針が決定されます。
解説
病理検査
患者さんのからだから採取された組織や細胞を染色し,顕微鏡で観察する検査を「病理検査」,その結果を「病理診断」といいます。病理検査は病理医が担当しています。乳腺に関する診療で病理検査が行われる場面は,大きく2つに分けられます。
1つは,乳房のしこりや分泌物の原因がどのような病気によるものかを判断し,症状の原因が悪性(がん)か良性かを診断する場合です(☞Q2参照)。この場合の病理検査には,症状の原因と思われるところの組織を針や小さな手術で取ってくる「生検」と,細い針を用いて細胞を採取する「細胞診」があります(☞Q3参照)。
もう1つは,乳がんと診断された後に,その生検標本や手術で切除された標本を観察し,乳がんの種類や性質,広がりや進行度(どこのリンパ節に,何個の転移があるかなど)を診断する場合です。手術中の断端判定や,センチネルリンパ節転移の判定も病理検査の一部です。このような情報は,その後の手術や薬物療法,放射線療法などの治療方針決定に必要不可欠です。
乳がん組織の病理検査では何を検査していますか
病理検査では,浸潤の有無,腫瘍の大きさ,がんの種類(組織型 表1 ),がん細胞の悪性度(グレード),リンパ節転移の有無と個数,脈管侵襲(がん周囲の血管やリンパ管にがん細胞が侵入しているかどうか),ホルモン受容体の有無や発現割合,HER2タンパクの過剰発現あるいはHER2遺伝子増幅の有無,がん細胞の増殖能(増えやすさ)(Ki67陽性がん細胞の割合など),PD-L1の発現などを検査しています。主要な病理診断項目を 表2 に示しました。これらの項目と年齢,月経の状況(閉経の有無)などをもとに,術前・術後の治療を選択します(☞Q15, 17参照)。がんの組織型のうち,まれなものを「特殊型がん」といいますが,その中には性質が通常の乳がん(浸潤性乳管がん)とは異なるものがあります。そのため,特殊型がんの場合には,その性質に応じた治療法が選択されることがあります(☞Q28参照)。
非浸潤がんと浸潤がんおよび組織型
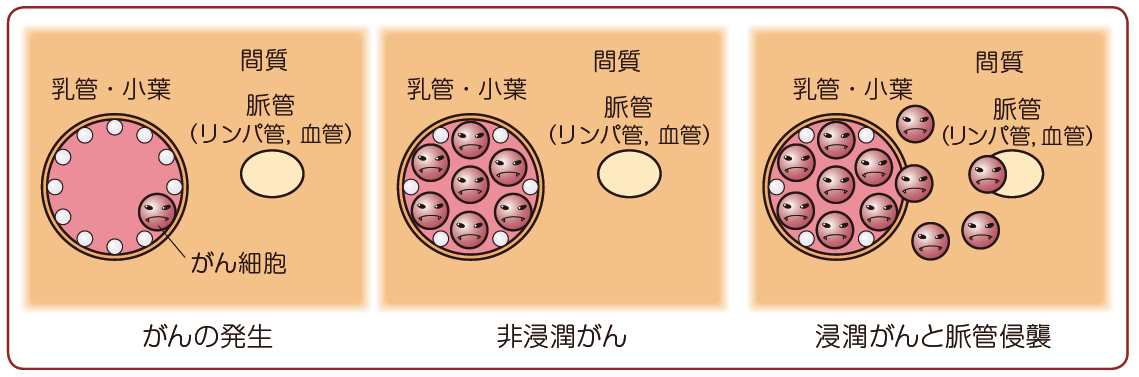
乳がん細胞のほとんどは,乳汁をつくって分泌する乳腺組織の一番末梢部分(乳管末梢から小葉に至る部位 図1 )に発生し,時間が経過すると,乳管・小葉の周囲(間質に広がります。がん細胞が乳管・小葉の周囲に広がることを「浸潤」といいます。この浸潤の有無によって,乳がんは大きく非浸潤がんと浸潤がんに分けられます。非浸潤がんは,がん細胞が乳管・小葉の中にとどまる乳がんで,適切な治療を行えば,転移や再発をすることはほとんどありません。一方,浸潤がんは,乳管・小葉の周囲に広がった乳がんで,後述の脈管侵襲を介して転移や再発をする危険性があります 図2 。浸潤がんは浸潤性乳管がんと特殊型がんに分類されます(☞Q28参照)。特殊型がんは浸潤がんの1~2割程度と報告されています。
表1 組織型
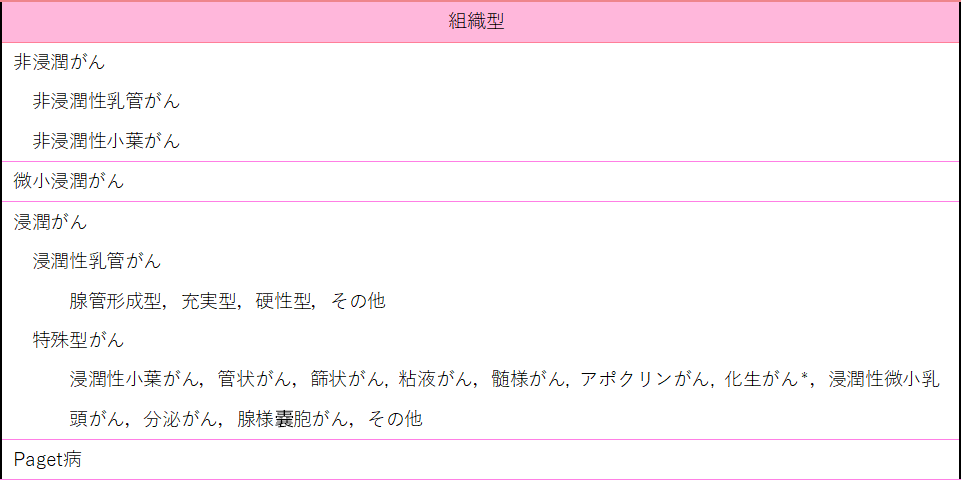
*「化生がん」はさらに,扁平上皮がん,間葉系分化を伴うがん(紡錘細胞がん,骨・軟骨化生を伴うがん,基質産生がん,その他),混合型に分類される。
(臨床・病理 乳癌取扱い規約第18版,金原出版,2018より改変)
図1 乳腺の構造

図2 非浸潤がんと浸潤がんおよび脈管(リンパ管,血管)侵襲
がん細胞の悪性度
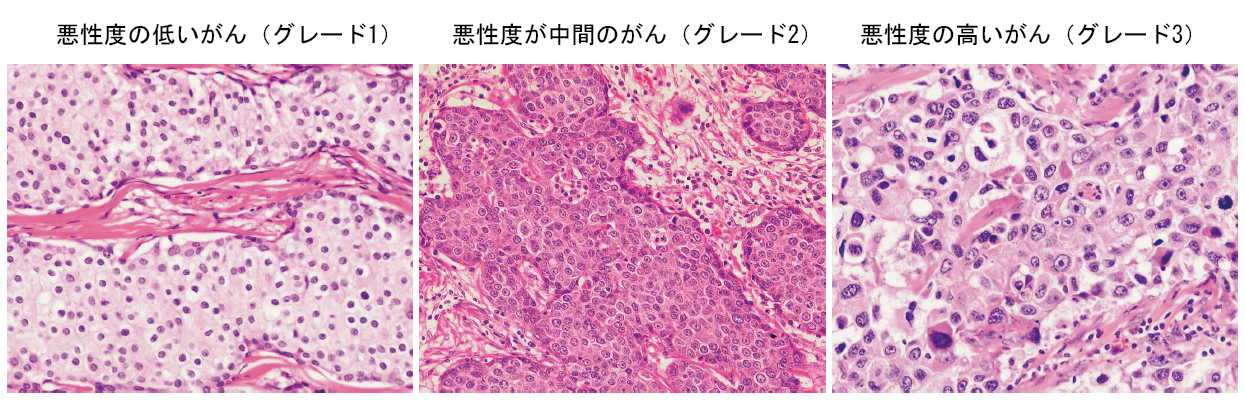
がん細胞の悪性度とは,顕微鏡でみたがん細胞の形から判断するもので,わかりやすくいうとがん細胞の顔つきのことです。浸潤がんでは,がん細胞の悪性度が高いと転移・再発のリスクが高くなります。悪性度は,グレード1~3の3段階に分けられます 図 3 。
図3 がん細胞の悪性度
脈管侵襲
血管やリンパ管は「脈管」ともいい,がん周囲の血管やリンパ管の中にがん細胞がみられることを脈管侵襲といいます 図2 。乳がんが,肺や骨,肝臓などの乳腺以外の臓器に転移する場合,がん細胞は脈管を通ります。このため,病理検査で脈管侵襲が確認されると,転移・再発するリスクが高くなります。
ホルモン受容体
ホルモン受容体とは,エストロゲン受容体(estrogen receptor; ER)とプロゲステロン受容体(progesterone receptor; PgR)のことで,乳がんにこのどちらかが陽性であれば,「ホルモン受容体陽性乳がん」といいます。ホルモン受容体陽性乳がんでは,女性ホルモンであるエストロゲンが,エストロゲン受容体に結び付いて,がん細胞が増殖するように刺激します。乳がんの70~80%がホルモン受容体陽性乳がんで,このような乳がんでは,体内のエストロゲンの量を減らしたり,エストロゲンががん細胞のエストロゲン受容体に結び付くのを邪魔したりする薬を用いるホルモン療法が有効です(☞Q16参照)。ホルモン受容体の有無は,乳がんの組織を用いた免疫組織化学法という病理検査でわかります。ホルモン受容体陽性乳がんでは,がん細胞の核が茶色く染まります 図4 。より強く染まる細胞の割合がより高いほど,ホルモン療法の効果が高いことがわかっています。
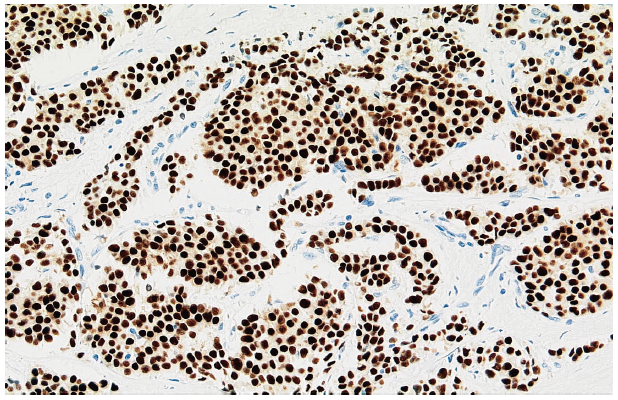
図4 ホルモン受容体陽性の乳がん
免疫組織化学法でがん細胞の核の中のホルモン受容体が茶色く染まっています。
HER2とは
HER2とは,Human Epidermal Growth Factor Receptor type 2(ヒト表皮成長因子受容体2型)の略です。HER2タンパクは,細胞の表面に存在して,細胞の増殖調節などに関係しますが,たくさんあると,細胞増殖の制御が効かなくなります。乳がんの15~25%では,がん細胞の表面に正常細胞の1,000~10,000倍ものHER2タンパクが存在しています。このような乳がんを「HER2タンパクの過剰発現がある乳がん」と呼びます。このような乳がんでは,HER2タンパクをつくるように司令を出す遺伝子の数も増えており,この状態を「HER2遺伝子の増幅がある」といい,HER2タンパクの過剰発現がある乳がん,HER2遺伝子の増幅がある乳がんを「HER2陽性乳がん」といいます。
HER2タンパクの過剰発現あるいはHER2遺伝子の増幅があるHER2陽性の浸潤がんは,そうでないものに比べて,悪性度が高く,細胞が増殖しやすく,転移・再発の危険性が高いことが知られています。しかし,トラスツズマブ(商品名 ハーセプチン),ペルツズマブ(商品名 パージェタ),ラパチニブ(商品名 タイケルブ)など,HER2陽性乳がんに対するさまざまな薬の登場で,予後が大幅に改善されました(☞Q42参照)。
HER2についての検査は,がんの転移・再発の危険性を予測したり,抗HER2薬の有効性を予測するために行われ,現在の乳がん診療においてはとても重要な検査の一つです。具体的には,乳がん組織を用いてHER2タンパクの過剰発現を調べる免疫組織化学法 図5 ,またはHER2遺伝子の増幅を調べるin situ hybridization(ISH)法で検査します。ISH法には,FISH法やDISH法などがあります。通常は,まず免疫組織化学法でHER2タンパクを検査し,必要に応じて,ISH法でHER2遺伝子検査を追加します。
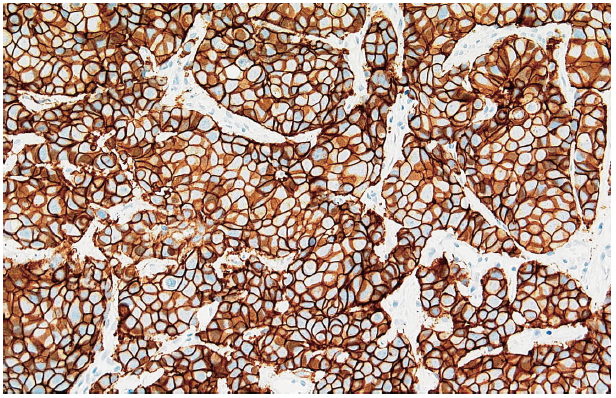
図5 HER2タンパクの過剰発現がある乳がん
免疫組織化学法でがん細胞の表面のHER2タンパクが茶色く染まっています。
がん細胞の増殖能,Ki67
1個の細胞が2個に,2個の細胞が4個に増えることを「細胞の増殖」といいます。一般的に,細胞が増殖する能力(増殖能)の高い(細胞が増えやすい)乳がんは低い乳がんに比べて,悪性度が高いといわれています。Ki67は細胞増殖の程度を表す指標です。Ki67陽性の細胞は,増殖の状態にあると考えられています。したがって,Ki67陽性細胞の割合が高い乳がんは,増殖能が高く,悪性度が高いと考えられます。具体的には,前述のホルモン受容体と同様,乳がん組織について免疫組織化学法という病理検査を行います。しかし,今のところ,病理標本のつくり方や,陽性細胞をどのように数えるか,また,陽性の細胞がどれくらいあれば陽性率が高いと考えるのかなどについて,一定の決まりがありません。そのため,Ki67をどのように調べるのが一番良いのかについての研究が,日本を含め,世界的に行われています。
サブタイプ分類
病理検査の結果で,「サブタイプ分類」の説明をされることがあります。サブタイプ分類は,本来,乳がん組織の多数の遺伝子発現検査の結果によってわかるものですが,多数の遺伝子発現検査をすべての患者さんで実施するのは高価であり,検査施設も充実していないため,遺伝子発現検査の代わりに,上記のホルモン受容体(エストロゲン受容体,プロゲステロン受容体),HER2,悪性度(グレード),Ki67の結果に基づいて,便宜的に分類して,サブタイプ分類を模した名付けをします。乳がんのサブタイプとして,「ルミナルA」,「ルミナルB」,「HER2」,「トリプルネガティブ」などの説明を受けることがあります。例えば,「トリプルネガティブ」とは,エストロゲン受容体,プロゲステロン受容体,HER2いずれも陰性のことで,ホルモン療法や抗HER2療法の効果が期待できません。「ルミナル」とはホルモン受容体陽性のことで,「ルミナル」であればホルモン療法の効果が期待できます。そのうち,「ルミナルA」は予後が比較的良好でホルモン療法単独での効果が期待されるタイプ,「ルミナルB」はホルモン療法に加え抗がん薬治療(化学療法)を行うことも考えたほうがよいタイプです。しかし,このような分類はあくまでも便宜的なものであり,本来の遺伝子発現検査によるものではありません。また,分類の基準が厳密には定まっていないため,混乱をきたしやすいという問題もあります。実際の治療方針はさまざまな情報を組み合わせて決定されますので,「サブタイプ」だけを気にしすぎるのは望ましくありません(☞Q29参照)。
PD-L1とは
PD-L1とは,programmed cell death 1 ligand 1(プログラム細胞死リガンド1)の略です。PD-L1は,がん細胞に対する免疫を抑制したり停止させたりする働きをもち,がん細胞はPD-L1をもつことでがんを攻撃する免疫細胞から逃れています。免疫チェックポイント阻害薬はこの仕組みをブロックすることでがん細胞を攻撃します(☞Q42参照)。
PD-L1についての検査は,ホルモン受容体陰性かつHER2陰性(トリプルネガティブ乳がん)の転移・再発乳がんに対して行われ,免疫組織化学法が用いられます。PD-L1が陽性の場合は,免疫チェックポイント阻害薬を使用します。PD-L1タンパクの検出には複数の抗体が用いられますが,これは免疫チェックポイント阻害薬の種類によって使い分けられます。アテゾリズマブ(商品名 テセントリク)に対してはSP-142,ペムブロリズマブに対しては22C3という抗体が用いられ,それぞれ厳密に定められた基準で診断が行われます 図6 (☞Q42参照)。
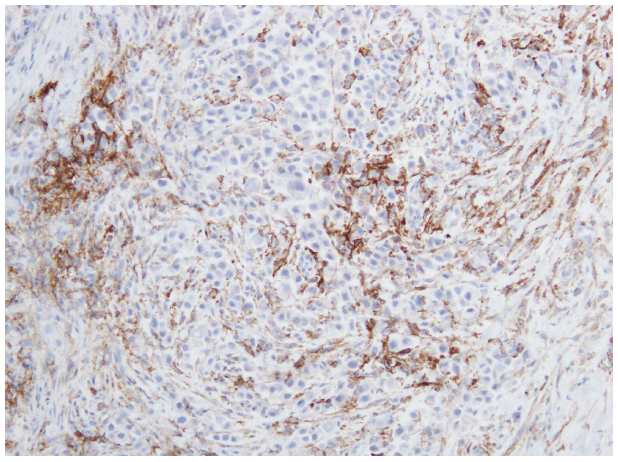
図6 PD-L1陽性を示す乳がん
免疫組織化学法でがん細胞と周りの炎症細胞の表面のPD-L1タンパクが茶色く染まっています。
多遺伝子アッセイ
最近,乳がん患者さんに対して,さまざまな遺伝子検査が行われるようになりましたが(☞Q52参照),その一部である多遺伝子アッセイは病理標本を使って行います。多遺伝子アッセイは,患者さん一人ひとりの乳がんの性質をより詳しく知るために,乳がん細胞にある遺伝子の発現の仕方や活性度を調べる検査で,欧米を中心に行われています。現在,商用化されているものにはOncotype DXやMammaPrintがあります。手術で採った乳がんの組織について,Oncotype DXは21個の遺伝子を,MammaPrintは70個の遺伝子を解析し,再発の危険度を予測します。患者さん個人個人に合った,最適な治療計画を立てる〔特に抗がん薬治療(化学療法)を加えるかどうかの決定の〕助けになることが期待され,日本でも検査が可能です。特にOncotype DXについては日本人を対象とした研究も行われており,有用であることが確認されています。Oncotype DXは2021年8月に薬事承認され,2022年12月現在,保険適用に向けての整備が行われているところです。検査を実施するには,通常の臨床情報や病理検査結果に基づく条件が細かく規定されています。この検査の必要性および実施の可否については乳腺専門医の説明を受けることが勧められます。
表2 病理レポートに記載される主要な病理診断項目

(臨床・病理 乳癌取扱い規約第18版,金原出版,2018より改変)