CQ2 術前化学療法後に,腋窩リンパ節郭清省略を目的としたセンチネルリンパ節生検は推奨されるか?
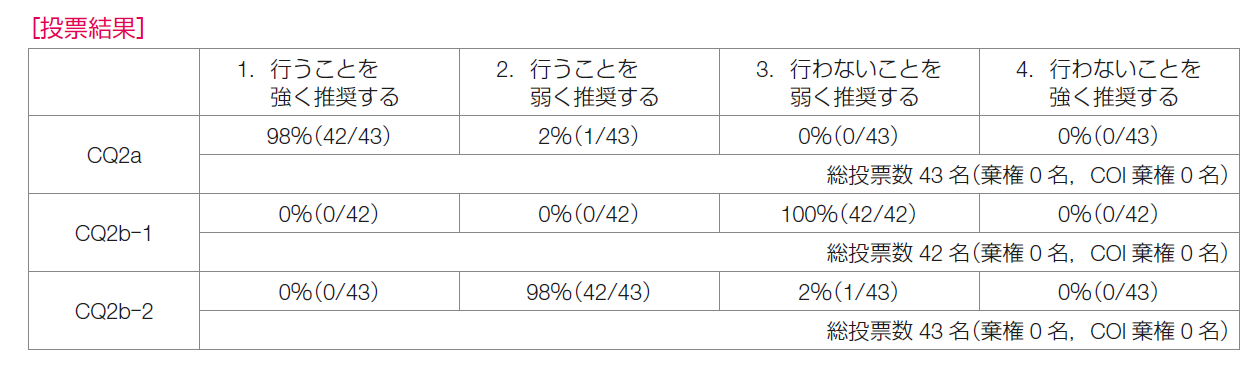
CQ2a 術前化学療法の前後とも臨床的腋窩リンパ節転移陰性の乳癌に対してセンチネルリンパ節生検による腋窩リンパ節郭清省略は推奨されるか?
CQ2b 臨床的腋窩リンパ節転移陽性乳癌が術前化学療法施行後に臨床的リンパ節転移陰性と判断された場合,センチネルリンパ節生検による腋窩リンパ節郭清省略は推奨されるか?
CQ2b-1 センチネルリンパ節生検の結果のみによる場合
CQ2b-2 Tailored axillary surgery(TAS*)を行う場合
*TAS:偽陰性を可能な限り少なくすることを目的に,TAD(targeted axillary dissection),SLNB,samplingなどを複合的に行い,元来転移のあったリンパ節を含めて切除する腋窩縮小手術
背 景・目 的
センチネルリンパ節生検(SLNB)は術前化学療法(NAC)を行わない臨床的リンパ節転移陰性乳癌では,正確な腋窩ステージングが可能であり,センチネルリンパ節(SLN)転移陰性の場合は腋窩リンパ節郭清(ALND)を省略しても予後に影響しないことが明らかとなった1)2)。一方,NACは局所進行乳癌に対して,ダウンステージングにより手術不能乳癌を手術可能にし,乳房温存率を向上させるなど既に標準的治療となっており,さらにNACによる病理学的完全奏効が予後良好のサロゲートマーカーになり得ることから,その適応は早期乳癌にも及んでいる。また,NACは腋窩リンパ節に対しても有意な治療効果が確認されており,臨床的腋窩リンパ節転移陽性乳癌がNAC後,臨床的腋窩リンパ節転移陰性となることも経験する。SLNBがNAC施行患者に対して安全に適応可能かどうかを明らかにすることを目的として,NAC前の臨床的リンパ節転移の状態別にエビデンスを整理し,検討を行った。
解 説
NAC後のSLNBにおいて想定される「害」は,生存率の低下,腋窩再発率の上昇,同定率の低下,偽陰性率の上昇である。一方で,SLNBによる「益」は,腋窩手術に伴う合併症の低下である。本CQに対する推奨の作成にあたっては,ALND省略における全生存率,無再発生存率に明らかな低下がないこと,腋窩再発率が対照となる症例(CQ2aでは手術先行例,CQ2bではALND症例)とほぼ同等であること,SLN同定率や偽陰性率が手術先行例とほぼ同等であること,および,ALNDをした場合にリンパ浮腫等の合併症が増えることを重視した。
推奨を決定するにあたり,CQ2a,CQ2bともに病理学的にSLN転移陰性であることをALND省略の前提とした。また,CQ2bでは,SLNBにおける手技の工夫の有無により推奨度が異なるため,CQ2b-1とCQ2b-2に分けて記載した。
1)CQ2a
(1)エビデンスの強さ
文献検索の結果,CQ2aに対する論文として,後ろ向き症例集積16論文のメタアナリシスを行った1編3)と前向きコホート研究2編4)5),症例集積研究4編の計7編を採用した6)~9)。さらに合併症の評価のため,2編10)11)を追加した。2018年の改訂時と比べると,多数例の前向きコホート研究4)や症例集積研究7)の結果が新たに報告されたが,全体としては症例集積研究が多いこと,またランダム化比較試験は実施されていないことから,エビデンスの強さは「弱」とした。
(2)エビデンスの内容
全生存率は前向きコホート研究1編4)と症例集積1編6)で,無病生存率はこれに症例集積研究1編7)を加えた3編,腋窩再発はさらに症例集積研究1編9)を加えた4編で評価が行われている。その結果,全生存率は93.3%6)~97.8%4),腋窩再発率は0.2%4)~1.2%9)と比較的ばらつきは小さかったが,無再発生存率は81.5%6)~97.2%4)とややばらつきが大きかった。腋窩再発に関して手術先行例との比較を行った論文では,NAC症例と手術先行例の間に有意差を認めなかった(NAC症例1.2%,手術先行例0.9%)9)。同定率については,メタアナリシス1編3)とコホート研究2編4)5)ならびに症例集積3編7)~9)を用いて検討した。年代の古い1編のみ84.8%と不良であったものの5),その他では95%8)~99.1%7)と高い値を示した。また,2編では非NAC症例との比較が行われ,手術先行例の同定率との間に有意差を認めなかった8)9)(手術先行例98~98.7%,NAC症例95~97.4%)。偽陰性率の評価は3編で行われており3)5)9),やはり年代の古い1編では10.7%とやや高かったものの5),残りの2編では5.9~6%と低い水準であった3)9)。手術合併症としてのリンパ浮腫の発生は,参照した文献いずれにおいてもALND症例において有意に高頻度に発生し10)11),メタアナリシスでのハザード比は2.5であった11)。
(3)推奨の強さ
以上のように,一部の項目で結果にばらつきがあるものの,概ね一貫した結果が得られている。SLNに転移がなければALND省略を行っても予後の悪化は認められず,SLNBそのものの指標となる同定率,偽陰性率の悪化も認められない。加えて,ALND省略による合併症の低減効果は明白である。以上より,「術前化学療法前後とも臨床的リンパ節転移陰性乳癌に対してSLNBによるALND省略を強く推奨する」とした。
2)CQ2b
(1)エビデンスの強さ
CQ2bに対しては,同定率,偽陰性率等を検討した19論文を網羅し,定量的システマティック・レビューとメタアナリシスを行った1編12)と前向きコホート研究4編5)13)~15),症例集積研究5編を採用し,さらに合併症の評価のための2編,計12編を採用した。多施設共同の前向きコホート試験として実施された臨床研究の成果が含まれている。予後に関しては質の高いエビデンスがないことから,全体としてのエビデンスの強さは「弱」とした。
(2)エビデンスの内容
① 予後について
SLNBガイドでALNDの適応を決めた場合と当初からALNDを行った場合の予後を直接比較した論文は2報存在した。うち1報では遠隔無再発率と腋窩無再発率を指標に比較が行われ16),もう1報では全生存率と無再発生存率を指標に比較が行われたが17),いずれも両者の間で予後の差は認めなかった。ただし,後者ではNAC前にもcN0であった症例が含まれているという問題を考慮する必要がある。SLNBガイドで治療を行った場合の腋窩再発率はほかに3つの文献で報告があり,それぞれ0.2,0.7,7.1%であった。腋窩再発率7.1%とは対象症例28例中1例に再発があったためであり18),症例数の多い文献では,より低い値が報告されていた6)7)。
② 同定率,偽陰性率について
SLNの同定率,偽陰性率に関してはコホート研究が行われており,同定率80.1~92.7%,偽陰性率7.0~14.2%と報告され,比較対象となる非NAC症例のSLNBの結果と比較すると劣る結果であった1)19)20)。コホート研究では,偽陰性率を改善させられるようなサブセットに関する検討が行われた。BoileauらはSLNの同定にdual tracer(ラジオアイソトープ+色素)を用いれば偽陰性率を5.2%まで低下できると述べている13)。Kuehnらはdual tracerで偽陰性率を8.6%に,3個以上のSLNを摘出すれば4.9%まで低下させられることを示した14)。また,Bougheyらもdual tracerで偽陰性率を10.8%へ,3個以上の摘出で9.1%まで低下させることができると述べている15)。以上より,SLNBに際してdual tracerを用いること,および3個以上のSLNを摘出することが偽陰性率を低下させる共通した条件であると考えられる。
転移陽性もしくは転移が疑わしいリンパ節をクリップ,ワイヤー,もしくはタトゥーなどで標識し,手術の際にSLNに加えて,この標識リンパ節および触診で腫大が確認されたリンパ節を摘出する手技を総称してtailored axillary surgery(TAS)と呼ぶ21)。このTASを行うことにより,NAC前に転移があったリンパ節の同定率は89~100%22)~32),偽陰性率は0~4.1%22)24)26)29)30)になると報告されており,これはSLNBのみを行った場合の同定率,偽陰性率と比較し,良好な結果である。
TASを行った症例の予後を通常のALNDを行った場合と比較した検討はなく,また,TASの手技についても標準化はされておらず,さらなる研究成果が待たれる。また,TASではSLNBに比較して摘出するリンパ節の個数が増えるため,リンパ浮腫の出現リスクはALNDを行った場合に近いものになると予想されるが,データはないため比較することができない。
(3)推奨の強さ
SLNBを行ってその結果をもとに郭清の適応を決定した場合と,当初よりALNDを行った場合で予後に明らかな差はないことが報告されているが,それは症例集積報告のみの結果である。一方,比較的質の高いコホート研究では,非NAC症例におけるSLNBと比較して,同定率や偽陰性率の悪化が示された。サブセットで検討すると,dual tracerによりSLNを3個以上同定,摘出すれば,同定率,偽陰性率を改善させられるものの,SLNを確実に3個以上同定する方法は確立されていない。
このことから,「臨床的腋窩リンパ節転移陽性乳癌が術前化学療法施行後に臨床的腋窩リンパ節転移陰性と判断された場合,SLNBの結果のみによるALND省略を弱く推奨しない」とした。
一方で,こうした症例に対してTASを行うことにより,SLNBのみを実施した場合の最大の問題点であった同定率ならびに偽陰性率に関しては改善をみることが示された。しかし,ALNDとの予後の比較がないこと,また,リンパ浮腫の発生頻度に関する比較もされていないという問題は残る。
以上を踏まえ,「臨床的腋窩リンパ節転移陽性乳癌が術前化学療法施行後に臨床的リンパ節転移陰性と判断された場合,tailored axillary surgery(TAS)によるALND省略は行うことを弱く推奨する」とした。
検索キーワード・参考にした二次資料
PubMedで,“Breast Neoplasms”,“Neoadjuvant chemotherapy”,“Sentinel Lymph Node Biopsy”,の共通キーワードに加え,CQ2aでは“Clinically node-negative”,CQ2bでは“Clinically node-positive”のキーワードを追加して検索した。医中誌・Cochrane Libraryも同等のキーワードで検索した。検索期間は2021年5月までとし,CQ2aで887編,CQ2bで622編の論文がヒットした。それ以外に腋窩リンパ節郭清の合併症に関する文献をハンドサーチで2編追加した。一次,二次スクリーニングの結果,CQ2aは9編,CQ2bは12編の論文が抽出された。なお,CQ2bのうち,TADに関する部分は別にFRQとして項目立てする予定であったため,上記とは別に11編の論文を抽出しており,CQ2bの参考文献に後で追加した。
参考文献
1)Krag DN, Anderson SJ, Julian TB, Brown AM, Harlow SP, Costantino JP, et al. Sentinel-lymph-node resection compared with conventional axillary-lymph-node dissection in clinically node-negative patients with breast cancer:overall survival findings from the NSABP B-32 randomised phase 3 trial. Lancet Oncol. 2010;11(10):927-33. [PMID:20863759]
2)Veronesi U, Paganelli G, Viale G, Luini A, Zurrida S, Galimberti V, et al. Sentinel-lymph-node biopsy as a staging procedure in breast cancer:update of a randomised controlled study. Lancet Oncol. 2006;7(12):983-90. [PMID:17138219]
3)Geng C, Chen X, Pan X, Li J. The feasibility and accuracy of sentinel lymph node biopsy in initially clinically node-negative breast cancer after neoadjuvant chemotherapy:a systematic review and meta-analysis. PLoS One. 2016;11(9):e0162605. [PMID:27606623]
4)Classe JM, Loaec C, Gimbergues P, Alran S, de Lara CT, Dupre PF, et al. Sentinel lymph node biopsy without axillary lymphadenectomy after neoadjuvant chemotherapy is accurate and safe for selected patients:the GANEA 2 study. Breast Cancer Res Treat. 2019;173(2):343-52. [PMID:30343457]
5)Mamounas EP, Brown A, Anderson S, Smith R, Julian T, Miller B, et al. Sentinel node biopsy after neoadjuvant chemotherapy in breast cancer:results from National Surgical Adjuvant Breast and Bowel Project Protocol B-27. J Clin Oncol. 2005;23(12):2694-702. [PMID:15837984]
6)Galimberti V, Ribeiro Fontana SK, Maisonneuve P, Steccanella F, Vento AR, Intra M, et al. Sentinel node biopsy after neoadjuvant treatment in breast cancer:five-year follow-up of patients with clinically node-negative or node-positive disease before treatment. Eur J Surg Oncol. 2016;42(3):361-8. [PMID:26746091]
7)Wong SM, Basik M, Florianova L, Margolese R, Dumitra S, Muanza T, et al. Oncologic safety of sentinel lymph node biopsy alone after neoadjuvant chemotherapy for breast cancer. Ann Surg Oncol. 2021;28(5):2621-9. [PMID:33095362]
8)van der Heiden-van der Loo M, de Munck L, Sonke GS, van Dalen T, van Diest PJ, van den Bongard HJ, et al. Population based study on sentinel node biopsy before or after neoadjuvant chemotherapy in clinically node negative breast cancer patients:identification rate and influence on axillary treatment. Eur J Cancer. 2015;51(8):915-21. [PMID:25857549]
9)Hunt KK, Yi M, Mittendorf EA, Guerrero C, Babiera GV, Bedrosian I, et al. Sentinel lymph node surgery after neoadjuvant chemotherapy is accurate and reduces the need for axillary dissection in breast cancer patients. Ann Surg. 2009;250(4):558-66. [PMID:19730235]
10)Ashikaga T, Krag DN, Land SR, Julian TB, Anderson SJ, Brown AM, et al;National Surgical Adjuvant Breast, Bowel Project. Morbidity results from the NSABP B-32 trial comparing sentinel lymph node dissection versus axillary dissection. J Surg Oncol. 2010;102(2):111-8. [PMID:20648579]
11)DiSipio T, Rye S, Newman B, Hayes S. Incidence of unilateral arm lymphoedema after breast cancer:a systematic review and meta-analysis. Lancet Oncol. 2013;14(6):500-15. [PMID:23540561]
12)El Hage Chehade H, Headon H, El Tokhy O, Heeney J, Kasem A, Mokbel K. Is sentinel lymph node biopsy a viable alternative to complete axillary dissection following neoadjuvant chemotherapy in women with node-positive breast cancer at diagnosis? An updated meta-analysis involving 3,398 patients. Am J Surg. 2016;212(5):969-81. [PMID:27671032]
13)Boileau JF, Poirier B, Basik M, Holloway CM, Gaboury L, Sideris L, et al. Sentinel node biopsy after neoadjuvant chemotherapy in biopsy-proven node-positive breast cancer:the SN FNAC study. J Clin Oncol. 2015;33(3):258-64. [PMID:25452445]
14)Kuehn T, Bauerfeind I, Fehm T, Fleige B, Hausschild M, Helms G, et al. Sentinel-lymph-node biopsy in patients with breast cancer before and after neoadjuvant chemotherapy(SENTINA):a prospective, multicentre cohort study. Lancet Oncol. 2013;14(7):609-18. [PMID:23683750]
15)Boughey JC, Suman VJ, Mittendorf EA, Ahrendt GM, Wilke LG, Taback B, et al;Alliance for Clinical Trials in Oncology. Sentinel lymph node surgery after neoadjuvant chemotherapy in patients with node-positive breast cancer:the ACOSOG Z1071(Alliance)clinical trial. JAMA. 2013;310(14):1455-61. [PMID:24101169]
16)Kang YJ, Han W, Park S, You JY, Yi HW, Park S, et al. Outcome following sentinel lymph node biopsy-guided decisions in breast cancer patients with conversion from positive to negative axillary lymph nodes after neoadjuvant chemotherapy. Breast Cancer Res Treat. 2017;166(2):473-80. [PMID:28766131]
17)Ogawa Y, Ikeda K, Watanabe C, Kamei Y, Tokunaga S, Tsuboguchi Y, et al. Sentinel node biopsy for axillary management after neoadjuvant therapy for breast cancer:a single-center retrospective analysis with long follow-up. Surg Today. 2018;48(1):87-94. [PMID:28647776]
18)Park S, Lee JE, Paik HJ, Ryu JM, Bae SY, Lee SK, et al. Feasibility and prognostic effect of sentinel lymph node biopsy after neoadjuvant chemotherapy in cytology-proven, node-positive breast cancer. Clin Breast Cancer. 2017;17(1):e19-29. [PMID:27495997]
19)Veronesi U, Paganelli G, Galimberti V, Viale G, Zurrida S, Bedoni M, et al. Sentinel-node biopsy to avoid axillary dissection in breast cancer with clinically negative lymph-nodes. Lancet. 1997;349(9069):1864-7. [PMID:9217757]
20)Veronesi U, Paganelli G, Viale G, Luini A, Zurrida S, Galimberti V, et al. A randomized comparison of sentinel-node biopsy with routine axillary dissection in breast cancer. N Engl J Med. 2003;349(6):546-53. [PMID:12904519]
21)Henke G, Knauer M, Ribi K, Hayoz S, Gérard MA, Ruhstaller T, et al. Tailored axillary surgery with or without axillary lymph node dissection followed by radiotherapy in patients with clinically node-positive breast cancer(TAXIS):study protocol for a multicenter, randomized phase-Ⅲ trial. Trials. 2018;19(1):667. [PMID:30514362]
22)Caudle AS, Yang WT, Krishnamurthy S, Mittendorf EA, Black DM, Gilcrease MZ, et al. Improved axillary evaluation following neoadjuvant therapy for patients with node-positive breast cancer using selective evaluation of clipped nodes:implementation of targeted axillary dissection. J Clin Oncol. 2016;34(10):1072-8. [PMID:26811528]
23)Donker M, Straver ME, Wesseling J, Loo CE, Schot M, Drukker CA, et al. Marking axillary lymph nodes with radioactive iodine seeds for axillary staging after neoadjuvant systemic treatment in breast cancer patients:the MARI procedure. Ann Surg. 2015;261(2):378-82. [PMID:24743607]
24)Diego EJ, McAuliffe PF, Soran A, McGuire KP, Johnson RR, Bonaventura M, et al. Axillary staging after neoadjuvant chemotherapy for breast cancer:a pilot study combining sentinel lymph node biopsy with radioactive seed localization of pre-treatment positive axillary lymph nodes. Ann Surg Oncol. 2016;23(5):1549-53. [PMID:26727919]
25)Natsiopoulos I, Intzes S, Liappis T, Zarampoukas K, Zarampoukas T, Zacharopoulou V, et al. Axillary lymph node tattooing and targeted axillary dissection in breast cancer patients who presented as cN+before neoadjuvant chemotherapy and became cN0 after treatment. Clin Breast Cancer. 2019;19(3):208-15. [PMID:30922804]
26)Siso C, de Torres J, Esgueva-Colmenarejo A, Espinosa-Bravo M, Rus N, Cordoba O, et al. Intraoperative ultrasound-guided excision of axillary clip in patients with node-positive breast cancer treated with neoadjuvant therapy(ILINA trial):a new tool to guide the excision of the clipped node after neoadjuvant treatment. Ann Surg Oncol. 2018;25(3):784-91. [PMID:29197044]
27)Kim WH, Kim HJ, Jung JH, Park HY, Lee J, Kim WW, et al. Ultrasound-guided restaging and localization of axillary lymph nodes after neoadjuvant chemotherapy for guidance of axillary surgery in breast cancer patients:experience with activated charcoal. Ann Surg Oncol. 2018;25(2):494-500. [PMID:29134374]
28)Allweis TM, Menes T, Rotbart N, Rapson Y, Cernik H, Bokov I, et al. Ultrasound guided tattooing of axillary lymph nodes in breast cancer patients prior to neoadjuvant therapy, and identification of tattooed nodes at the time of surgery. Eur J Surg Oncol. 2020;46(6):1041-5. [PMID:31801656]
29)García-Novoa A, Acea-Nebril B, Díaz Carballada C, Bouzón Alejandro A, Conde C, et al. Combining wire localization of clipped nodes with sentinel lymph node biopsy after neoadjuvant chemotherapy in node-positive breast cancer:preliminary results from a prospective study. Ann Surg Oncol. 2021;28(2):958-67. [PMID:32725521]
30)Spautz CC, Schunemann Junior E, Budel LR, Cavalcanti TCS, Louveira MH, Junior PG, et al. Marking axillary nodes with 4% carbon microparticle suspension before neoadjuvant chemotherapy improves sentinel node identification rate and axillary staging. J Surg Oncol. 2020;122(2):164-9. [PMID:32291774]
31)Kim EY, Byon WS, Lee KH, Yun JS, Park YL, Park CH, et al. Feasibility of preoperative axillary lymph node marking with a clip in breast cancer patients before neoadjuvant chemotherapy:a preliminary study. World J Surg. 2018;42(2):582-9. [PMID:28808843] 32)Plecha D, Bai S, Patterson H, Thompson C, Shenk R. Improving the accuracy of axillary lymph node surgery in breast cancer with ultrasound-guided wire localization of biopsy proven metastatic lymph nodes. Ann Surg Oncol. 2015;22(13):4241-6. [PMID:25814365]