総説3 乳癌初期治療における乳房再建
乳癌治療において根治性の追求は当然であるが,近年,乳房の整容性維持にも高い関心が寄せられている。乳癌の根治性と乳癌術後の整容性を追求する目的で生まれた手術手技を表す乳房オンコプラスティックサージャリー(OPBS)の概念が登場して以降,乳癌術式に応じた乳房再建の必要性が問われている。OPBSという用語・概念は1990年代にAudretshらによって提唱され,ヨーロッパを中心に急速に広まってきた。乳房全切除術時の乳房再建や乳房部分切除術時の乳房形成手術のほか,胸壁合併切除時の胸壁再建などもOPBSに該当する1)。
それぞれの再建術式の利点・欠点について説明を十分に行い,患者の同意を得たうえで再建術を実施する必要がある。
1)再建時期と回数
乳房全切除術と同時に行う一次(primary)再建と,乳房全切除術後に一定期間を経て行う二次(secondary)再建がある2)。また,一期(one-stage)再建とは1回の手術で再建を行う方法であり,二期(two-stage)再建はまず組織拡張器(tissue expander;TE)を用いて皮膚を伸展させてから後日再建する(TEをインプラントまたは自家組織に置き換える)方法である。
2)乳房全切除術後の再建術
乳房皮膚を含めて乳腺組織を全切除する乳房全切除術のほかに,乳頭乳輪組織と乳腺組織のみを全切除する皮膚温存乳房全切除術と乳頭乳輪組織を含む乳房皮膚をすべて温存し乳腺組織のみを全切除する乳頭温存乳房全切除術が再建術の対象となる術式である。乳房再建術はインプラントを含むほとんどすべての再建が保険適用となったので,適応となる全ての患者に情報提供をしなければならない。さらには,2020年4月より遺伝性乳癌卵巣癌症候群(HBOC)に対するリスク低減手術として片側乳癌発症患者への対側乳房のリスク低減乳房切除術・再建術,および卵巣癌発症患者への両側乳房のリスク低減乳房切除・再建術が保険適用となった。
(1)組織拡張器(TE)+インプラント2)~5)
2013年からインプラントを用いた乳房再建が保険適用となり,希望する患者が増加した(表1)。本法は,乳腺が全切除され,大胸筋が温存されている症例に対して適応となる。乳房が大きい患者や下垂した患者は再建が難しいが,健側乳房固定術や縮小術により対称性を得ることは可能である。本法は初回にTEを挿入し,皮膚や大胸筋を伸展させた後,インプラントを挿入するため二度の手術を要するが,インプラントの正確なサイズの決定や,入れ替え時に位置や乳房下溝の修正が可能という利点を有する。挿入するTEやインプラントの安全性を担保するため,日本乳房オンコプラスティックサージャリー学会により,TE,インプラントの施設認定や実施医師認定,年次報告の義務化を行って管理している。ただし,保険適用のTEやインプラントに関する使用要件基準は,日本乳房オンコプラスティックサージャリー学会により,術前診断において原則としてStage Ⅱ以下で皮膚浸潤,大胸筋浸潤や高度のリンパ節転移を認めない症例と規定されているため,注意が必要である(☞外科CQ3参照)。合併症としては,血腫,漿液腫,感染といった一般的な合併症のほかに,皮膚壊死によるインプラント露出や被膜拘縮をきたすことがある(表2)。特に放射線照射後の再建において生じやすいため,適応を見極める必要がある(☞外科BQ3参照)。
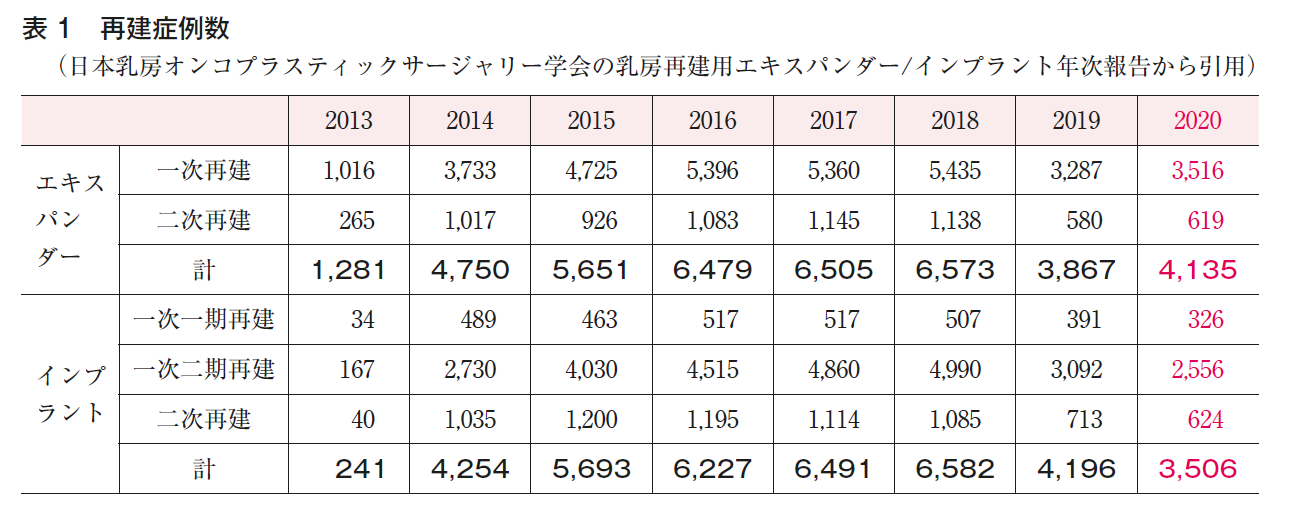
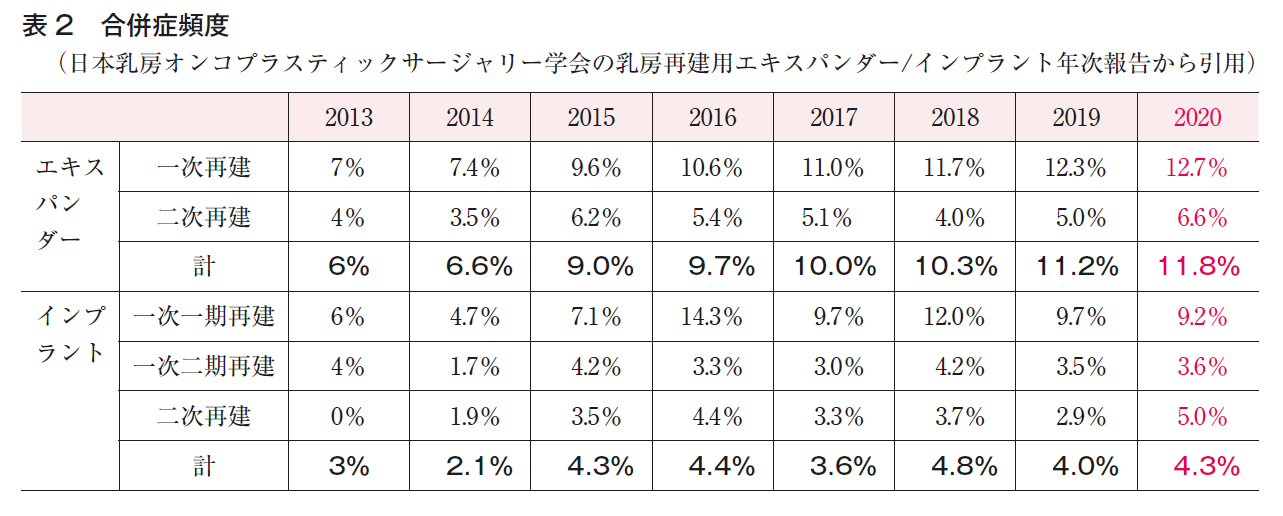
また,特殊な合併症としてブレスト・インプラント関連未分化大細胞型リンパ腫(BIA-ALCL)が欧米で報告され,世界中で993例の報告があり,わが国では2件である(2021年11月30日現在)。発生頻度はテクスチャードブレスト・インプラント全体では約2,200~86,000人に1人の割合とされている6)。今後患者数が増加する可能性もあり,注意が必要である。TE挿入・インプラント再建を希望する患者には再建を行う「益」とともに,「害」(合併症,インプラントの耐久年数など)についても十分な情報提供を行い,患者への意思決定支援を行うことが重要である。
2019年7月24日,FDAはBIA-ALCLの発症例および死亡例の世界的症例を報告したglobal safety informationに基づき,BIA-ALCLのリスクから患者を保護するため,アラガン社に対してマクロテクスチャードブレスト・インプラントおよびTEを市場から自主回収するように要請し,アラガン社はこれに従った。それ以降,わが国では保険適用のテクスチャードブレスト・インプラントおよびTEは皆無となり,インプラントを用いた再建が一時停止した。その代替品として同年10月8日にアラガン社のスムースタイプのインプラントとTEが認可され,10月16日に保険適用となった。その処置により,インプラントを用いた再建が全国で再開された。またその後,シエントラ社のブレスト・インプラントが2020年8月20日に保険適用になった(マイクロテクスチャード,スムースタイプとも)。新たに保険適用になったアラガン社のスムースタイプのインプラントを含めた10年間の715例の検討では,合併症に関してインプラント破損率は全体で13%(自主回収となった以前のアナトミカル型マクロテクスチャードタイプでは9.7%),Ⅲ度またはⅣ度の被膜拘縮率は豊胸で18.9%,再建で24.6%,被膜拘縮率はスムースタイプとマクロテクスチャードタイプで大きな差を認めなかった(19.9% vs 17.2%)7)。次に,シエントラ社のブレスト・インプラントの10年間の99例の検討では,合併症に関してインプラント破損率は全体で8.6%,Ⅲ度またはⅣ度の被膜拘縮率は13.5%,被膜拘縮はマイクロテクスチャードタイプのほうがスムースタイプより有意に少ない結果であった(9% vs 17.5%)8)。ただし,これらの臨床試験は,メーカー間で直接比較するようには設計されておらず,個々の製品の合併症率が表示されていることに留意する必要がある。
FDAへの報告(2020年1月5日)によると,全BIA-ALCL症例903例中アラガン社のインプラントは620例,シエントラ社のインプラントは10例であった。いずれにおいてもインプラント施行総数は不明なため,本結果では,その発生割合については不明である。スムースタイプのインプラントが挿入されていたBIA-ALCL症例は28例確認されているが,そのうち8例は過去にマクロテクスチャードタイプのインプラントの挿入歴があった。スムースタイプのインプラントのみを挿入する場合,マクロテクスチャードタイプに比べ,BIA-ALCLに関するリスクは低いと報告されている9)。
現時点でのこの問題に関する情報や方針については,日本乳癌学会ホームページ(https://www.jbcs.gr.jp/modules/citizens/)において,日本乳癌学会を含む国内関連4学会が連名で発表しているので,ご覧いただきたい。まだ,根拠のある情報が少なく,今後のさらなるデータの集積が待たれる。
(2)広背筋皮弁2)~4)
広背筋皮弁は乳房再建において最も利用しやすい自家組織の一つであり,背部の広背筋とその直上の脂肪組織を移植材料として用いる筋皮弁である。ただし,広背筋皮弁の採取量には限度があり,大きな組織量を必要とする再建には向いていない。したがって,通常,乳房の比較的小さい患者に適応される。一方で,最近,広背筋皮弁へ一期的に後述の脂肪注入を行うことで皮弁のボリュームを増大させる報告もあり,今後,本法の適応が拡大する可能性がある10)11)。合併症としては,筋皮弁採取部の浸出液貯留,皮弁の部分壊死,血腫などを生じることがある。
(3)腹直筋皮弁2)3)
腹直筋皮弁は片側の腹直筋を血流の担体とし,下腹部の皮膚皮下脂肪を移植材料として用いるスタンダードな筋皮弁である。広背筋皮弁に比べて大きな組織の移植が可能であることがその特徴である。しかし,腹直筋を採取することによる腹壁の脆弱化が合併症として存在し,腹直筋を犠牲にしない同様の手術が出現したため,施行例は減少傾向である。その他の合併症として血流不全により皮弁の部分壊死をきたすことがある。
(4)遊離深下腹壁動脈穿通枝皮弁2)~4)
深下腹壁動脈穿通枝皮弁は腹直筋を犠牲にせずに臍周囲の太い穿通枝とそれに連続する深下腹壁動静脈のみを茎とする皮弁であり,腹直筋皮弁に比べると機能的な損失がほとんどなく,有益な皮弁である。ただ,皮弁血管を内胸動静脈や胸背動静脈に顕微鏡下で吻合する必要があり,難易度は高く,手術時間も比較的長い。本法を用いると,大きく下垂した乳房も再建可能であるが,下腹部に乳房と同等の脂肪組織および太い穿通枝を有することが前提となる。ただし,吻合した血管が閉塞すると合併症として皮弁壊死を生じる可能性(2~5%)があるので注意を要する。
また,浅下腹壁動脈が発達している患者では,浅下腹壁動静脈を茎とする腹部皮弁が利用できることがある12)。本法では腹直筋の筋膜切開が不要であるため,深下腹壁動脈穿通枝皮弁よりも,さらに機能的損失を少なくすることができる。
(5)その他の皮弁13)
腹部皮弁のほかにも,さまざまな部位からの穿通枝皮弁が開発され,乳房再建に用いられている。代表的な皮弁として,深大腿動脈穿通枝皮弁,上・下殿動脈穿通枝皮弁,腰動脈穿通枝皮弁などがある。それぞれの特徴を以下に示す。
深大腿動脈穿通枝皮弁:瘢痕は大腿内側後面に隠れ,両側から採取し,両側乳房再建に用いることもできる。一方,採取量は限られており,大きな乳房の再建には向いていない。
上・下殿動脈穿通枝皮弁:瘢痕は下着に隠れ,両側から採取し,両側乳房再建に用いることができる。一方,皮弁血管の長さが短い,採取に体位変換が必要,片側採取の場合には採取部の左右非対称が目立つことがあるなどの欠点を有する。
腰動脈穿通枝皮弁:比較的大きな組織の移植が可能で,両側から採取することもできる。一方,上・下殿動脈穿通枝皮弁と同様に,皮弁血管の長さが短く血管移植がしばしば必要,採取に体位変換を要するなどの欠点を有する。
(6)脂肪注入(保険適用外)5)(☞外科FRQ6参照)
下腹部や大腿内側から余剰脂肪を吸引し,精製(遠心分離,洗浄,または静置)することで脂肪細胞のみを抽出して患部に注入する方法である。再建乳房の小陥凹変形の修正やボリューム増大が良い適応である。脂肪細胞の生着率は通常,40~50%であり,移植床の条件に大きく影響を受ける。複数回の注入を必要とするものの,脂肪注入単独による全乳房再建の報告もある14)。また,注入脂肪の生着率を向上させる手段として,体外式組織拡張器の併用や14),少量の吸引脂肪から体外で培養増幅した脂肪組織由来幹細胞移植の併用が報告されている15)。一方で,不適切な手技による注入を行うと,術後,注入脂肪の石灰化や硬結をきたして乳癌との判別が困難になる問題点も有している。本法は,現時点では保険適用ではなく自費診療として行われている。
〔追記〕自家脂肪注入は手軽で効果的な治療手段として普及したが,1987年にアメリカ形成外科学会は,脂肪壊死や微小石灰化が乳癌発見の妨げになるとして問題視した。その後,2009年には新しく発足した特別委員会が脂肪注入術の安全性(少ない合併症率)と効果(外科医の高い満足度)について調査し,新しい推奨文を報告した16)。それによると脂肪注入に関しては,脂肪採取・脂肪細胞の分離・注入方法がいまだ標準化されていないため,臨床的な使用において特別に推奨することはできないとした。術後結果は術者の技量や経験によるところが大きく,今後長期的な安全性と効率性に関する信頼性の高い臨床的研究が必要とされている。脂肪注入により乳癌の診察に支障をきたす危険性はあるが,放射線学的診断には支障をきたさないとしている。委員会の報告後,自家脂肪注入の安全性,効果および効率に焦点を当てた論文が多く報告されたが,概ね良好な結果が得られている17)~19)。しかし,依然として脂肪採取手技,採取した脂肪の加工工程や脂肪注入手技は統一・標準化されておらず,術者の経験に基づいた方法で行われている。
近年,脂肪注入はわが国においても関心が高まっており,保険適用を目指す動きがある。その際に,比較的容易な手技であるために安易に行って良くない結果や合併症を生む可能性がある。したがって,今後は本手技の講習会等を行い,許可を得た医師のみが施行できる手技とするなどの精度管理や標準化に向けた取り組みが必要と思われる。
(7)乳頭乳輪再建2)3)5)
乳頭乳輪再建は乳房再建の仕上げの手術であり,再建乳房の整容性の鍵となる手術である。その方法はさまざま報告されているが,乳頭再建は健側乳頭半切移植や局所皮弁法があり,乳輪再建はタトゥー(保険適用外)や大腿内側基部の皮膚移植が主に行われている。
3)乳房部分切除術時の再建術20)~23)
乳房部分切除術と術後放射線療法による乳房温存療法は腫瘍径の小さな乳癌に,あるいは非浸潤性乳管癌(DCIS)に対して,さらに全身療法と組み合わせた場合にはより大きな浸潤癌に対しても安全に施行し得ることが明らかとなってきた。しかし,切除量が乳房の20%を超える部分切除術を行った場合,整容性を維持することは難しい。腫瘍が乳房内側1/4領域あるいは乳房下部1/4領域に占居する場合や,乳房部分切除術に用いた皮膚切開創から腋窩リンパ節郭清を行った場合,欠損部周囲の乳腺脂肪組織が適切に授動されなかった場合も整容性を損ねる結果を招くことが知られている。
術後の変形を防ぐ目的で乳房全切除術後の再建と同様に,乳房部分切除術時に一次的に乳房形成を行うと手技的・経済的に,また患者精神面で良好な結果が得られることが報告された。乳癌治療時に一次的に行うと,①切除検体の大きさ,厚さ,重量などが正確にわかる,②切除側の皮下脂肪,乳腺切離断端の状態が正確にわかる,③移動(充填)に用いる周囲組織の血行の信頼性が高い,などの長所が挙げられる。一方,二次的に形成手術を実施すると,①欠損の範囲,大きさ,形,容量などの予測が難しい,②乳房の皮膚皮下脂肪,残存乳腺組織が硬く,伸展不良のことが多い,③乳房およびその周辺組織の血行が手術や放射線照射により障害されている可能性がある,などの問題がある。総じて手技的に難易度が高く,良好な整容性を得ることは難しいといえる。乳房部分切除術時と同時のほうが手技的にも良好な,また結果的にも整容性に配慮した形成が行える。乳房部分切除術後の欠損に対しては,乳腺弁,遊離真皮脂肪,脂肪幹細胞(保険適用外),有茎および遊離皮弁,各種人工材料などが用いられている24)。
乳房部分切除術と同時に,より整容性を整える手技を加えた乳房温存オンコプラスティックサージャリーは,ヨーロッパを中心に確立されている25)。乳房のサイズが大きく,特に乳房下垂の程度が著しい症例では,乳房縮小手術・乳房固定手術の要素を取り入れた手技により,より整容性に優れた結果を得ることができる。わが国においても,前述の乳房部分切除術+欠損部補填と並んで,乳房部分切除術時の乳房再建手技として有用な手法となり得る可能性がある26)27)。
参考文献
1)Audretsch WP, Rezai M, Kolotas C, Zamboglou N, Schnabel T, Bojar H, et al. Oncoplastic surgery:“target”volume reduction(BCT mastopexy), lumpectomy reconstruction(BCT reconstruction)and flap-supported operability in breast cancer. Proceedings 2nd European Congress on Senology, Vienna, Austria, Bologna, Italy, Monduzzi, pp139-57. 1994.
2)矢野健二.乳がん術後一期的乳房再建術 乳がん術式に応じた乳房再建のテクニック.東京,克誠堂出版,2007.
3)波利井清監修,矢野健二編著.乳房・乳頭の再建と整容 最近の進歩 改訂第2版.東京,克誠堂出版,2010.
4)矢野健二,小川朋子編.乳房オンコプラスティック・サージャリー ―根治性と整容性を向上させる乳がん手術―.東京,克誠堂出版,2014.
5)矢野健二,小川朋子,佐武利彦編著.乳房オンコプラスティックサージャリー2 症例から学ぶ手術手技.東京,克誠堂出版,2017.
6)American Society of Plastic Surgeons. BIA-ALCL Physician Resources. https://www.plasticsurgery.org/for-medical-professionals/health-policy/bia-alcl-physician-resources(Page last updated on January 13, 2021)
7)Spear SL, Murphy DK;Allergan Silicone Breast Implant U. S. Core Clinical Study Group. Natrelle round silicone breast implants:Core Study results at 10 years. Plast Reconstr Surg. 2014;133(6):1354-61. [PMID:24867717]
8)Stevens WG, Calobrace MB, Alizadeh K, Zeidler KR, Harrington JL, d’Incelli RC. Ten-year core study data for Sientra’s Food and Drug Administration-approved round and shaped breast implants with cohesive silicone gel. Plast Reconstr Surg. 2018;141(4S Sientra Shaped and Round Cohesive Gel Implants):7S-19S. [PMID:29595714]
10)Santanelli di Pompeo F, Laporta R, Sorotos M, Pagnoni M, Falesiedi F, et al. Latissimus dorsi flap for total autologous immediate breast reconstruction without implants. Plast Reconstr Surg. 2014;134(6):871e-9e. [PMID:25415109]
11)Taminato M, Tomita K, Nomori M, Maeda D, Seike S, Tashima H, et al. Fat-augmented latissimus dorsi myocutaneous flap for total breast reconstruction:a report of 54 consecutive Asian cases. J Plast Reconstr Aesthet Surg. 2021;74(6):1213-22. [PMID:33257301]
12)Wu LC, Bajaj A, Chang DW, Chevray PM. Comparison of donor-site morbidity of SIEA, DIEP, and muscle-sparing TRAM flaps for breast reconstruction. Plast Reconstr Surg. 2008;122(3):702-9. [PMID:18766032]
13)Myers PL, Nelson JA, Allen RJ Jr. Alternative flaps in autologous breast reconstruction. Gland Surg. 2021;10(1):444-59. [PMID:33634002]
14)Khouri RK, Rigotti G, Khouri RK Jr, Cardoso E, Marchi A, Rotemberg SC, et al. Tissue-engineered breast reconstruction with Brava-assisted fat grafting:a 7-year, 488-patient, multicenter experience. Plast Reconstr Surg. 2015;135(3):643-58. [PMID:25719686]
15)Kølle ST, Duscher D, Taudorf M, Fischer-Nielsen A, Svalgaard JD, Munthe-Fog L, et al. Ex vivo-expanded autologous adipose tissue-derived stromal cells ensure enhanced fat graft retention in breast augmentation:a randomized controlled clinical trial. Stem Cells Transl Med. 2020;9(11):1277-86. [PMID:32639099]
16)Gutowski KA;ASPS Fat Graft Task Force. Current applications and safety of autologous fat grafts:a report of the ASPS fat graft task force. Plast Reconstr Surg. 2009;124(1):272-80. [PMID:19346997]
17)Spear SL, Coles CN, Leung BK, Gitlin M, Parekh M, Macarios D. The safety, effectiveness, and efficiency of autologous fat grafting in breast surgery. Plast Reconstr Surg Glob Open. 2016;4(8):e827. [PMID:27622095]
18)Gabriel A, Champaneria MC, Maxwell GP. Fat grafting and breast reconstruction:tips for ensuring predictability. Gland Surg. 2015;4(3):232-43. [PMID:26161308]
19)Strong AL, Cederna PS, Rubin JP, Coleman SR, Levi B. The current state of fat grafting:a review of harvesting, processing, and injection techniques. Plast Reconstr Surg. 2015;136(4):897-912. [PMID:26086386]
20)Baildam AD. Oncoplastic surgery of the breast. Br J Surg. 2002;89(5):532-3. [PMID:11972541]
21)Clough KB, Lewis JS, Couturaud B, Fitoussi A, Nos C, Falcou MC. Oncoplastic techniques allow extensive resections for breast-conserving therapy of breast carcinomas. Ann Surg. 2003;237(1):26-34. [PMID:12496527]
22)O’Brien W, Hasselgren PO, Hummel RP, Coith R, Hyams D, Kurtzman L, et al. Comparison of postoperative wound complications and early cancer recurrence between patients undergoing mastectomy with or without immediate breast reconstruction. Am J Surg. 1993;166(1):1-5. [PMID:8392300]
23)Eberlein TJ, Crespo LD, Smith BL, Hergrueter CA, Douville L, Eriksson E. Prospective evaluation of immediate reconstruction after mastectomy. Ann Surg. 1993;218(1):29-36. [PMID:8328826]
24)日本乳癌学会編.乳腺腫瘍学 第3版.東京,金原出版,2020年.
25)Clough KB, Nos C, Salmon RJ, Soussaline M, Durand JC. Conservative treatment of breast cancers by mammaplasty and irradiation:a new approach to lower quadrant tumors. Plast Reconstr Surg. 1995;96(2):363-70. [PMID:7624409]
26)Kijima Y, Yoshinaka H, Funasako Y, Natsugoe S, Aikou T. Oncoplastic surgery after mammary reduction and mastopexy for bilateral breast cancer lesions:report of a case. Surg Today. 2008;38(4):335-9. [PMID:18368323]
27)Kijima Y, Yoshinaka H, Ishigami S, Hirata M, Kaneko K, Mizoguchi T, et al. Oncoplastic surgery for Japanese patients with ptotic breasts. Breast Cancer. 2011;18(4):273-81. [PMID:20084556]