総説 Ⅴ.転移・再発乳癌
1.治療の目的
- 転移・再発乳癌に対する治療の目的は,以下の3つのPであり,前二者は「生活の質(QOL)の維持・改善」とも言い換えられる。
① 「癌による症状の緩和(palliate symptoms)」
② 「癌による症状出現の先送り(prevent symptoms)」
③ 「生存期間の延長(prolong survival)」
2.転移・再発乳癌の現状と治療の原則
- 転移・再発乳癌は,根治が困難である。
- 転移・再発乳癌の予後は,サブタイプによって異なり,全生存期間の中央値は,ホルモン受容体陽性HER2陰性乳癌では44.8カ月,HER2陽性では58カ月,トリプルネガティブ乳癌は14.2カ月との報告がある1)。
- 治療としては,薬物療法を中心とした集学的治療を行う。
- 転移・再発乳癌治療においては,癌に由来する苦痛を対症的に取り除くことを目的とする緩和治療を積極的に併用する。
- 転移・再発乳癌に対して局所療法を加えることで生存期間の延長が得られるかどうかについてのエビデンスは未確立であり,現在,臨床試験が進行中である。少数転移(オリゴ転移:oligometastasis)に対する局所療法が生存率の延長に寄与する可能性はあるが,エビデンスは十分ではない。
3.治療選択において考慮すべき因子
- 転移・再発乳癌は多様な背景をもつため,以下の4つを治療選択において考慮する。
① 患者の個別性
② 腫瘍の個別性
③ エビデンス
④ 患者の希望
- 患者の個別性については以下を考慮する。
① 年齢
② 併存症の有無
③ 社会的・経済的背景 など
- 腫瘍の個別性については以下を考慮する。
① 腫瘍の生物学的特性(ER,PgR,HER2,PD-L1,BRCA病的バリアントなど)
② 転移臓器とその広がり
③ 再発までの期間(disease-free interval;DFI)
④ 術前・術後薬物療法の種類
⑤ 癌による症状の有無 など
4.治療方針
a.薬物療法
- 治療開始前に,治療効果予測因子であるホルモン受容体(ER,PgR)とHER2状況の評価を必ず行う。可能であれば転移病巣から組織を採取して評価することが望ましいが,不可能である場合は原発腫瘍で行う。
- ホルモン受容体とHER2状況により治療方針が大きく異なる。
- 薬物療法には,内分泌療法,化学療法,分子標的療法,免疫療法がある。
- 乳癌における「免疫療法」は,「免疫チェックポイント阻害薬」による治療を指す。
- トリプルネガティブ乳癌(アンスラサイクリン・タキサン既治療例)の場合,治療開始前に,さらに,①PD-L1発現の検査と,②生殖細胞系列BRCA病的バリアントの検査を行い,①では免疫チェックポイント阻害薬,②ではPARP阻害薬の適応の有無をそれぞれ確認する。→「Ⅴ.4.a.a-2.トリプルネガティブ転移・再発乳癌の場合」参照。
- ホルモン受容体陽性HER2陰性であり,かつ軟部組織や骨転移がない場合,あるいは内臓転移があっても差し迫った生命の危険(例えば,広範な肝転移や肺転移,癌性リンパ管症など,「visceral crisis」とも呼ぶ)がない場合や,再発までの期間(DFI)が長い症例などは,内分泌療法から開始する。
- ホルモン受容体陽性HER2陰性であっても,差し迫った生命の危機がある内臓転移(visceral crisis)を有する場合は化学療法から治療を開始する。
【豆知識】Visceral crisis(ヴィッセラル クライシス)とは
ABC5コンセンサスガイドライン(Advanced Breast Cancer 5th International Consensus Conference)2)では,visceral crisisとは,徴候や症状,臨床検査で評価される重度の臓器障害,および疾患の急速な進行と定義される。Visceral crisisは,単に内臓転移が存在することではなく,最も迅速で効果的な治療の臨床的適応となる重要な臓器障害を意味する。 ❖肝のvisceral crisis:肝転移が原因でビリルビンが急速に増加して,基準値上限の1.5倍を超える状態。 ❖肺のvisceral crisis:安静時の呼吸困難が急速に悪化して,胸水を排出しても緩和されない状態。
- 原発巣と転移巣では,ホルモン受容体とHER2の発現状況が異なる場合もある。
- バイオマーカーが原発巣と転移巣で異なった場合には,少なくともどちらかで陽性と判定されれば,そのバイオマーカーに関連する薬剤の有効性が期待できるため,投与を考慮する。
- 関連課題:薬物BQ8「乳癌骨転移に対して骨修飾薬(デノスマブ,ゾレドロン酸)は推奨されるか?」
- 関連課題:薬物BQ12「乳癌治療として補完・代替療法は推奨されるか?」
- 関連課題:薬物FRQ17「転移・再発男性乳癌に対する薬物療法は何が推奨されるか?」
- 関連課題:薬物FRQ16「転移・再発高齢者乳癌に対する薬物療法として何が推奨されるか?」
- 関連課題:薬物FRQ19「乳癌脳転移および髄膜播種に抗悪性腫瘍薬は勧められるか?」
- 関連課題:薬物FRQ20「乳癌診療において次世代シークエンサー等を用いた遺伝子パネル検査は有用か?」
- 関連課題:薬物FRQ21「乳腺悪性葉状腫瘍の遠隔転移に対して薬物療法は勧められるか?」
a-1.ホルモン受容体(HR)陽性HER2陰性転移・再発乳癌の場合
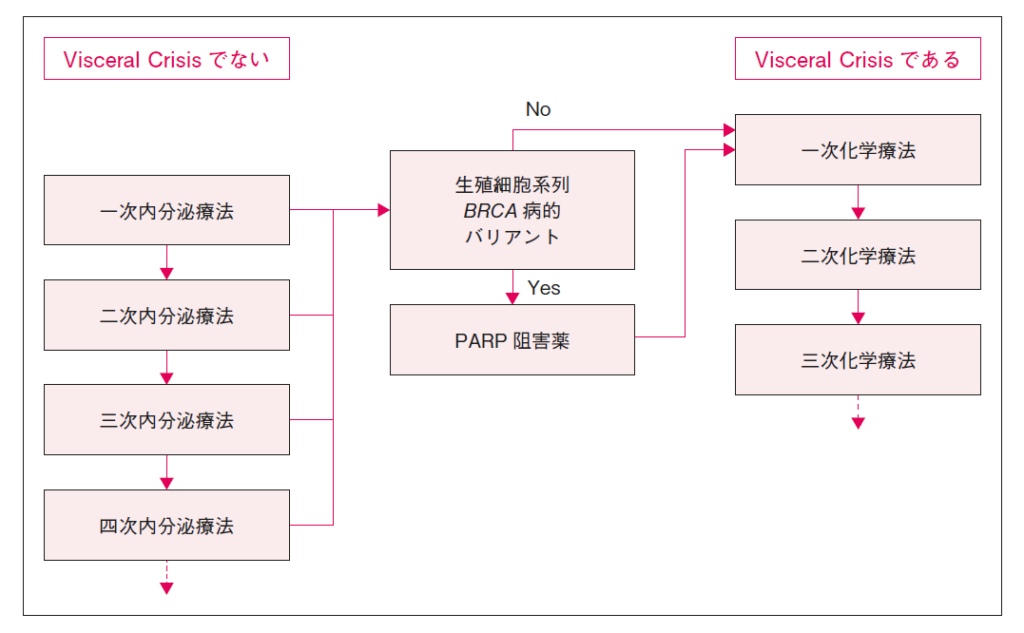
1)一次・二次内分泌療法の定義
- 再発時期にかかわらず,転移・再発後に「最初に行う内分泌療法」は,すべて「一次内分泌療法」と定義し,「その次に行う内分泌療法」を「二次内分泌療法」と定義する。
2)術後療法で用いた内分泌療法が再発一次内分泌療法の選択に及ぼす影響
- ホルモン受容体陽性の転移・再発乳癌に対する内分泌療法を行う際は,再発時期や周術期に使用した内分泌療法の種類を考慮のうえ薬剤を選択すべきである。
- ABC3コンセンサスガイドライン(Advanced Breast Cancer 3rd International Consensus Conference)では,術後内分泌療法を開始して2年以内に再発した症例を「primary(de novo)endocrine resistance」,開始2年以降の再発を「secondary(acquired)endocrine resistance」と定義している3)。
- 「術後内分泌療法治療中もしくは内分泌療法終了から1年以内」の再発に対する内分泌療法には,術後内分泌療法と異なる薬剤を選択する。
- 「術後内分泌療法終了から1年以上」経過してからの再発に対する内分泌療法は,術後内分泌療法と同じ薬剤の再投与(CDK4/6阻害薬の併用投与を含む)も選択肢となる。
3)治療方針
- ホルモン受容体陽性HER2陰性であり,かつ軟部組織や骨転移,あるいは内臓転移であっても差し迫った生命の危険(visceral crisis)(広範な肝転移や肺転移,癌性リンパ管症など)がない場合,再発までの期間(DFI)が長い症例などは,内分泌療法±CDK4/6阻害薬から開始する。
- ホルモン受容体陽性HER2陰性であっても,差し迫った生命の危機がある内臓転移(visceral crisis)を有する場合は化学療法から治療を開始する。
- 生殖細胞系列のBRCA病的バリアントの有無(BRACAnalysis®検査)を必ず調べて,PARP阻害薬(オラパリブ)の適応の有無を確認しておく。検査を施行する時期は,周術期のアンスラサイクリン・タキサン既治療例の場合には内分泌療法中に,アンスラサイクリン・タキサン未治療例の場合には,それらを終了する前が適切である。
- PARP阻害薬(オラパリブ)の適応:アンスラサイクリンおよびタキサン既治療HER2陰性進行・再発乳癌。なお,アンスラサイクリンとタキサンの使用が周術期であっても適応となる。
- 一次内分泌療法が奏効した場合は,無効になるまで治療を継続する。同様にvisceral crisisの有無や直前の内分泌療法の感受性などを参考に,二次以降の内分泌療法を行う。
- 内分泌療法が無効と判断される場合は化学療法に移行する。
(1)閉経前患者に対する内分泌療法
- 一次内分泌療法として,CDK4/6阻害薬+LH-RHアゴニスト+非ステロイド系アロマターゼ阻害薬併用療法が勧められる。
- 一次内分泌療法として,LH-RHアゴニスト+タモキシフェン,または,LH-RHアゴニスト+アロマターゼ阻害薬も選択肢である。
- 一次療法として,内分泌療法のみを施行した場合,二次内分泌療法として,CDK4/6阻害薬+LH-RHアゴニスト+フルベストラント併用療法が勧められる。
- 関連課題:薬物BQ5「閉経前ホルモン受容体陽性転移・再発乳癌に対して最も有用な卵巣機能抑制方法は何か?」
- 関連課題:薬物CQ18「閉経前ホルモン受容体陽性HER2陰性転移・再発乳癌に対する一次内分泌療法として,何が推奨されるか?」
- 関連課題:薬物CQ19「閉経前ホルモン受容体陽性HER2陰性転移・再発乳癌に対する二次以降の内分泌療法として,何が推奨されるか?」
(2)閉経後患者に対する内分泌療法
- 一次内分泌療法として,CDK4/6阻害薬+非ステロイド系アロマターゼ阻害薬併用療法が勧められる。
- 一次内分泌療法にアロマターゼ阻害薬単剤が使用された場合の二次内分泌療法として,CDK4/6阻害薬+フルベストラント併用療法が勧められる。
- 三次内分泌療法として,エキセメスタン+エベロリムスが勧められる。
- 関連課題:薬物CQ20「閉経後ホルモン受容体陽性HER2陰性転移・再発乳癌に対する一次内分泌療法として,何が推奨されるか?」
- 関連課題:薬物CQ21「閉経後ホルモン受容体陽性HER2陰性転移・再発乳癌の一次療法にアロマターゼ阻害薬単剤を使用したときの二次内分泌療法として,何が推奨されるか?」
- 関連課題:薬物CQ22「閉経後ホルモン受容体陽性HER2陰性転移・再発乳癌に対する三次治療以降の内分泌療法として,何が推奨されるか?」
- 関連課題:薬物FRQ10「閉経後ホルモン受容体陽性HER2陰性転移・再発乳癌の二次内分泌療法として何が推奨されるか?(一次内分泌療法として,アロマターゼ阻害薬単剤を行った場合はCQ21参照)」
(3)内分泌療法終了後の薬剤選択
- BRCA病的バリアントを有する場合:PARP阻害薬を投与する。
- BRCA病的バリアントを有しない場合:化学療法を行う〔Ⅴ.4.a.a-2.3)(1)③トリプルネガティブ乳癌(PD-L1陰性,かつ,BRCA病的バリアントを有しない)の治療方針参照〕。
- 化学療法奏効後の内分泌療法による維持療法で,化学療法継続よりもQOLの改善が期待されるが,治療効果を維持できるかどうかは不明である。
a-2.トリプルネガティブ転移・再発乳癌の場合
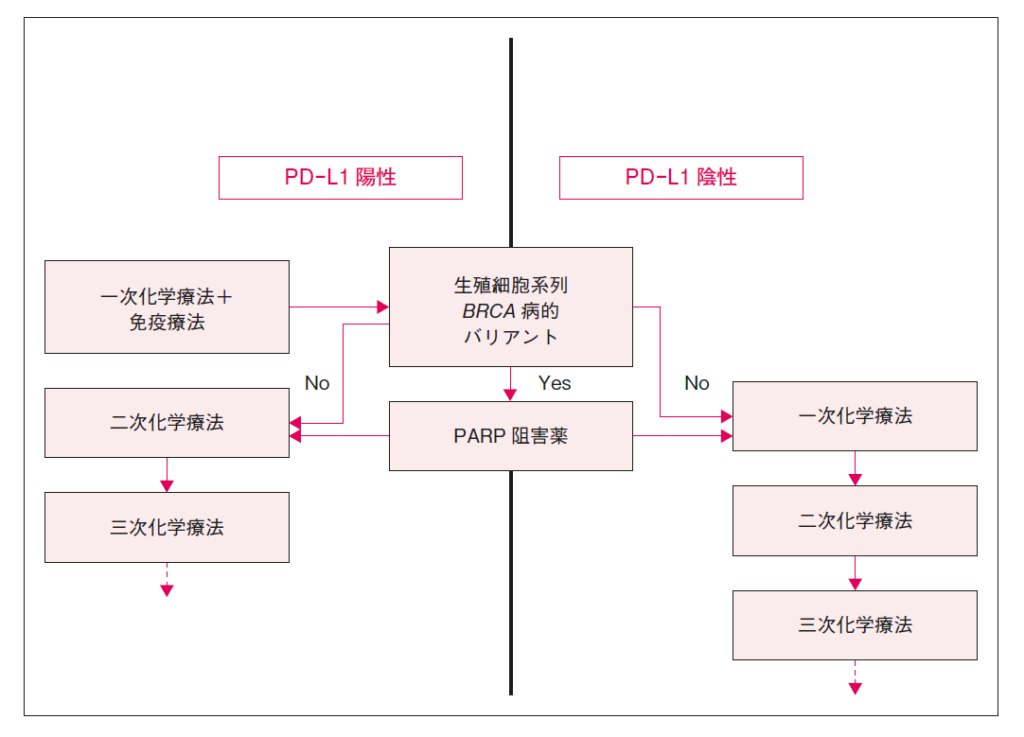
1)一次・二次化学療法の定義
- 内分泌療法と同様に,再発時期にかかわらず,転移・再発後に「最初に行う化学療法」をすべて「一次化学療法」と定義し,「その次に行う化学療法」を「二次化学療法」と定義する。
2)治療開始前に行う検査
- 周術期のアンスラサイクリン・タキサン既治療例の場合には,治療開始前に,① PD-L1発現の検査と,② 生殖細胞系列のBRCA病的バリアントの検査(BRACAnalysis®検査)を行い,① では免疫チェックポイント阻害薬,② ではPARP阻害薬の適応の有無をそれぞれ確認する。
- アンスラサイクリン・タキサン未治療例の場合には,それらを終了する前に,生殖細胞系列のBRCA病的バリアントの有無を必ず調べて,PARP阻害薬の適応の有無を確認する。
- 関連課題:病理診断FRQ5「浸潤性乳癌におけるPD-L1検査はどのように行うか?」
- 関連課題:薬物CQ31「転移・再発乳癌に対してPD-1/PD-L1阻害薬は勧められるか?」
- 関連課題:薬物CQ32「生殖細胞系列BRCA病的バリアントを有する進行・再発乳癌患者の薬物療法として,PARP阻害薬は推奨されるか?」
3)治療方針
(1)PD-L1発現,BRCA病的バリアントの有無の確認
① PD-L1陽性の場合
- 一次治療として,免疫チェックポイント阻害薬+化学療法併用療法が勧められる。
- BRCA病的バリアントも有する場合:一次治療としての,免疫チェックポイント阻害薬+化学療法併用療法とPARP阻害薬を比較した試験は存在しない。しかし,免疫チェックポイント阻害薬+化学療法併用療法の臨床試験のエビデンスは一次療法しかない一方で,PARP阻害薬の臨床試験の対象患者は一次療法以降の患者も含んでいることから,上図では,免疫チェックポイント阻害薬+化学療法併用療法を優先したが,PARP阻害薬を先行することも選択肢の一つである4)。
② PD-L1陰性,かつ,BRCA病的バリアントを有する場合
- PARP阻害薬(オラパリブ)の投与が勧められる。
③ PD-L1陰性,かつ,BRCA病的バリアントを有しない場合
- 化学療法薬単剤が勧められる。
- 関連課題:薬物BQ6「HER2陰性転移・再発乳癌に対する一次・二次化学療法として,アンスラサイクリン系薬剤は推奨されるか?」
- 関連課題:薬物BQ7「HER2陰性転移・再発乳癌に対する一次・二次化学療法として,タキサン系薬剤は推奨されるか?」
- 関連課題:薬物CQ23「HER2陰性転移・再発乳癌に対する一次・二次化学療法として,ベバシズマブを併用することは推奨されるか?」
- 関連課題:薬物CQ24「HER2陰性転移・再発乳癌に対する一次・二次化学療法として,経口フッ化ピリミジンは推奨されるか?」
- 関連課題:薬物CQ25「HER2陰性転移・再発乳癌に対する一次・二次化学療法として,エリブリンは推奨されるか?」
- 関連課題:薬物CQ30「転移・再発トリプルネガティブ乳癌に対してプラチナ製剤は勧められるか?」
(2)化学療法の実施方法
- 化学療法は,単剤順次投与が基本。
- 化学療法の同時併用は単剤投与よりも奏効率は高いものの毒性が増加し,臨床的に有意な生存期間の延長は認められないため,転移・再発乳癌に対する化学療法では単剤順次投与が勧められる。
(3)転移・再発乳癌に対する動注化学療法
- 転移・再発乳癌に対して,動注化学療法は行うべきでない。
- 転移・再発乳癌には全身薬物療法が標準治療である。動注化学療法が全身化学療法に勝るというエビデンスは存在しない。
- 動注化学療法の最適レジメンは不明であり,手技が煩雑でカテーテルトラブルのリスクがあることなどを考慮すると,日常臨床で転移・再発乳癌に対する動注化学療法は行うべきでない。
(4)化学療法の継続期間
- 転移・再発乳癌に対する有効性の示された化学療法を三次治療以降も順に使用していくことは妥当であるが,漫然と治療を継続するのではなく,個々の症例の治療経過,治療目標,リスクとベネフィットのバランスなどを考慮して,慎重に治療方針を検討する必要がある。
(5)MSI-high乳癌に対するペムブロリズマブ
- マイクロサテライト不安定性が高頻度に認められる場合をmicrosatellite instability(MSI)-highと呼ぶ。
- TCGAのデータベースでは乳癌の中でMSI-high腫瘍は1.53%(16/1,044例)であった。
- PD-1阻害薬であるペムブロリズマブが,「がん化学療法後に増悪した進行・再発の高頻度マイクロサテライト不安定性(MSI-high)を有する固形癌(標準的な治療が困難な場合に限る)」を対象に承認された。
- MSI-highの判定にはMSI検査キット(FALCO),FoundationOne® CDxがんゲノムプロファイルが,ニボルマブ(結腸・直腸癌)およびペムブロリズマブ(固形癌)のコンパニオン診断薬として承認されている。
【豆知識】マイクロサテライト不安定性とは
DNA複製の際に生じるミスマッチを修復する機能(mismatch repair;MMR)の低下により,1から数塩基の繰り返し配列(マイクロサテライト)の反復回数に変化が生じた状態をマイクロサテライト不安定性という。
【豆知識】臓器横断的治療(tumor-agnostic therapy)とは
臓器横断的治療(tumor-agnostic therapy)とは,原発巣やがん種を越えて,バイオロジーに基づいて薬剤選択を行う治療を指す。2018年12月,わが国において,進行・再発の高頻度マイクロサテライト不安定性(MSI-high)を有する固形癌に対して,抗PD-1抗体であるペムブロリズマブが薬事承認された。臓器横断的な適応症をもつ薬剤としては国内でのはじめての承認となった。さらに,NTRK融合遺伝子陽性固形癌に対するTRK阻害薬の有効性が示され,2019年6月にエヌトレクチニブが承認され,臓器横断的な承認として,国内で2番目の薬剤となった。その後,2021年3月にはTRK阻害薬のラロトレクチニブも承認されている。
【豆知識】NTRK融合遺伝子と乳腺分泌癌
NTRK遺伝子ファミリーは癌遺伝子であり,NTRK1~3までが知られている。NTRK 1~3はそれぞれ受容体チロシンキナーゼであるtropomyosin receptor kinase(TRK)A,TRKB,TRKCをコードする。乳腺分泌癌の約90%にNTRK融合遺伝子を認める。乳腺分泌癌は,非常に稀な乳癌(全乳癌の0.15%以下)であり,多くはトリプルネガティブ乳癌である。乳腺分泌癌以外の乳癌においても,NTRK融合遺伝子は稀ながら報告されている(FoundationCoreデータベースでは乳癌30,182例で0.39%)5)。
- 関連ガイドライン:日本癌治療学会,日本臨床腫瘍学会,日本小児血液・がん学会編「成人・小児進行固形がんにおける臓器横断的ゲノム診療のガイドライン」
a-3.HER2陽性転移・再発乳癌の場合
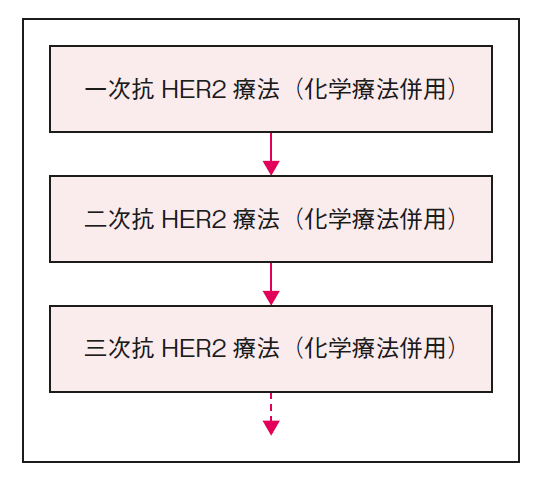
1)一次・二次抗HER2療法の定義
- 再発時期にかかわらず,転移・再発後に「最初に行う治療」をすべて「一次治療」と定義し,「その次に行う治療」を「二次治療」と定義する。
2)治療方針
- 化学療法と抗HER2療法の併用による生存期間の延長が示されているため,化学療法を併用した抗HER2療法が基本となる。
- 一次治療として,トラスツズマブ+ペルツズマブ+タキサン併用療法が勧められる。
- 関連課題:薬物CQ26「HER2陽性転移・再発乳癌に対する一次治療として,トラスツズマブ+ペルツズマブ+タキサン併用療法は推奨されるか?」
- 関連課題:薬物CQ27「HER2陽性転移・再発乳癌に対する一次治療として,トラスツズマブ エムタンシンは推奨されるか?」
- 二次治療として,トラスツズマブ デルクステカン(T-DXd)が勧められる。
- 関連課題:薬物CQ28「HER2陽性転移・再発乳癌に対する二次治療として,トラスツズマブ デルクステカンは推奨されるか?」
- 関連課題:薬物CQ29「HER2陽性・ホルモン受容体陽性転移・再発乳癌に対して内分泌療法単独や抗HER2療法と内分泌療法併用は勧められるか?」
b.外科療法
- 遠隔転移に対する外科的切除に関しては生存期間の延長に寄与するエビデンスはないため,基本的には勧められない。
- 病期Ⅳ乳癌においては,薬物療法を中心とした集学的治療を行うのが原則である。原発巣を切除する臨床的意義に関してはいまだ結論は出ていない。
- 遠隔転移を伴わない局所・領域リンパ節再発(乳房内再発,局所再発,領域リンパ節再発)に対しては,治癒を念頭に置いて外科治療を含む集学的治療を行う。
- 領域リンパ節再発は,腋窩リンパ節再発,鎖骨上リンパ節再発,内胸リンパ節再発の3つに分類される。
- 遠隔転移を伴わない腋窩リンパ節再発は,初回手術時の遺残である可能性があり,手術の適応がある。
- 関連課題:外科BQ4「初回腋窩リンパ節郭清後の腋窩リンパ節再発に対する外科的切除は勧められるか?」
- 関連課題:薬物FRQ18「局所・領域再発切除術後に薬物療法は勧められるか?」
- 関連課題:外科FRQ11「乳房全切除後の胸壁再発巣に対する外科的切除は勧められるか?」
- 関連課題:放射線FRQ4「乳癌の局所・領域リンパ節再発では,根治を目指した放射線療法が勧められるか?」
- 乳房温存療法後の局所再発は,いわゆる温存乳房内再発であり,約10%未満にみられる。
- 温存乳房内再発と診断された病変には,もとの癌の遺残による真の再発と,初発の癌とは別に発生した新たな癌とが含まれる。
- 関連課題:外科FRQ9「乳房温存療法後の温存乳房内再発に対して再度の乳房部分切除術は勧められるか?」
- 関連課題:外科FRQ10「乳房温存療法後の温存乳房内再発に対するセンチネルリンパ節生検は勧められるか?」
c.放射線療法
1)局所・領域リンパ節再発
- 局所再発は,乳房温存療法後では乳房内再発,乳房全切除術後では胸壁再発を指す。
- 領域リンパ節再発は,腋窩リンパ節再発,鎖骨上リンパ節再発,内胸リンパ節再発の3つに分類される。
- 鎖骨上および内胸リンパ節再発は原則的には放射線療法の適応である。
- 放射線療法が適応となる局所・領域リンパ節再発に対しては,放射線療法を含む集学的治療により長期間の無病生存期間の継続を目標とする。
2)遠隔転移
- 骨転移・脳転移に対して,原則,放射線療法では治癒は望めないが,疼痛や神経症状など,患者のQOLを低下させるさまざまな症状を予防・緩和することが期待できる。
(1)脳転移
- 目的:症状改善および癌の頭蓋内制御
- 脳全体に分割照射する全脳照射と,病巣部位のみに限局して1回ないし複数回の照射をする定位放射線照射がある。
- 関連課題:放射線CQ8「3 cm未満で1~4個までの乳癌脳転移に対して定位手術的照射(SRS)を行った場合,全脳照射の追加は勧められるか?」
- 関連課題:放射線FRQ5「全身状態のよい10個以下の脳転移症例において,一次治療として定位放射線照射(STI)を行い経過観察することで,全脳照射を待機することが勧められるか?」
- 定位放射線照射の種類:
◦ガンマナイフ:頭部を覆うヘルメットに201個のコバルト線源を配置し,コバルト線源からのガンマ線を用いる。
◦リニアックを用いた定位放射線照射:汎用のリニアックの照射口に筒状の絞り装置(コーン)または特殊な多分割コリメータを使用し,ガンマナイフと同様にナロービームで多方向から照射する。
◦サイバーナイフ:小型のリニアックを工業用ロボットで操作して,多方向から病巣に放射線を集中させる。着脱可能な固定具を使用する。
(2)骨転移
- 目的:疼痛緩和と運動機能維持
- 分割照射法以外に,8 Gyの1回照射も用いられる。
- 関連課題:放射線BQ11「有痛性乳癌骨転移に対して放射線療法は勧められるか?」
- 関連課題:放射線CQ7「8 Gy/1回照射は有痛性乳癌骨転移の疼痛緩和を目的とした場合,分割照射と同等の治療として勧められるか?」
- 関連課題:放射線FRQ6「少数個転移・再発では,体幹部定位放射線治療が勧められるか?」
参考文献
1)Grinda T, Antoine A, Jacot W, Blaye C, Cottu PH, Diéras V, et al. Evolution of overall survival and receipt of new therapies by subtype among 20 446 metastatic breast cancer patients in the 2008-2017 ESME cohort. ESMO Open. 2021;6(3):100114. [PMID:33895695]
2)Cardoso F, Paluch-Shimon S, Senkus E, Curigliano G, Aapro MS, André F, et al. 5th ESO-ESMO international consensus guidelines for advanced breast cancer(ABC 5). Ann Oncol. 2020;31(12):1623-49. [PMID:32979513]
3)Cardoso F, Costa A, Senkus E, Aapro M, André F, Barrios CH, et al. 3rd ESO―ESMO international consensus guidelines for advanced breast cancer(ABC 3). Ann Oncol. 2017;28(12):3111. [PMID:28327998]
4)Moy B, Rumble RB, Come SE, Davidson NE, Di Leo A, Gralow JR, et al. Chemotherapy and targeted therapy for patients with human epidermal growth factor receptor 2-negative metastatic breast cancer that is either endocrine-pretreated or hormone receptor-negative:ASCO guideline update. J Clin Oncol. 2021;39(35):3938-58. [PMID:34324366]
5)Westphalen CB, Krebs MG, Le Tourneau C, Sokol ES, Maund SL, Wilson TR, et al. Genomic context of NTRK1/2/3 fusion-positive tumours from a large real-world population. NPJ Precis Oncol. 2021;5(1):69.