FRQ4 浸潤径1 cm以下・リンパ節転移陰性のトリプルネガティブ乳癌に対して,術後化学療法は勧められるか?
背 景
浸潤径1 cm以下・リンパ節転移陰性の乳癌は一般的には予後良好であるが1),トリプルネガティブ乳癌は,他の乳癌サブタイプに比べて悪性度が高く予後が不良とされている2)。トリプルネガティブ乳癌に対する周術期薬物療法の中心は化学療法であるが,浸潤径1 cm以下・リンパ節転移陰性の場合,ほとんどの臨床試験において適格基準から外れており,化学療法の有効性については明らかにされていない。
解 説
これまでに浸潤径1 cm以下・リンパ節転移陰性のトリプルネガティブ乳癌に対する術後化学療法の有効性に関するランダム化比較試験(RCT)の報告は認めないが,複数の後ろ向き研究の結果が報告されており,表1に主要な報告の概要を示す。サンプル数,フォローアップ期間,解析方法などから論文を選択した。結果については,1つの研究の中で複数の解析がされている場合は,主解析を採用した。主解析が明記されていない場合は,多変量解析,単変量解析の順で1つの結果を採用した。
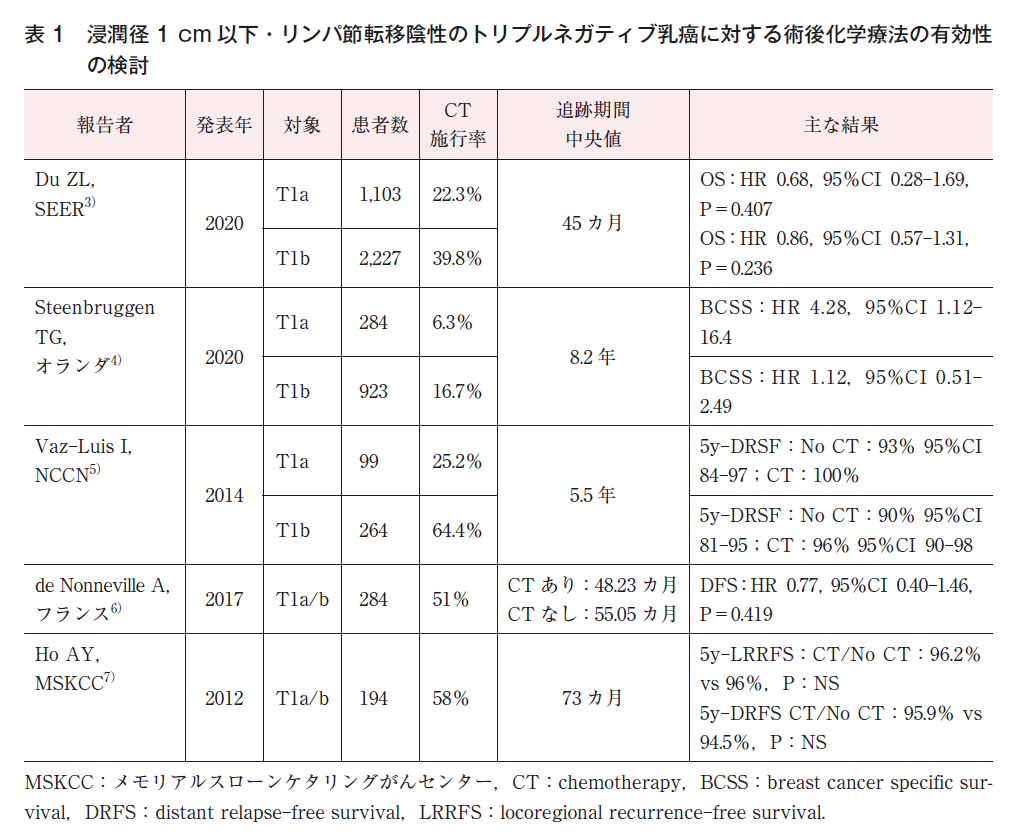
報告の中にはT1a/T1bで結果をそれぞれ解析したものもあり,腫瘍サイズごとに解説を行う。
T1aにおいては,SEER3),オランダ4),NCCN5)のデータベースからの報告で,計1,486例のうち287例(19.3%)に化学療法が施行されており,2群間で検定がされたものでは,化学療法が予後を改善させたとするものはなかった。T1bにおいては,SEER3),オランダ4),NCCN5)のデータベースからの報告で,計3,414例のうち1,210例(35.4%)に化学療法が施行されていた。こちらも2群間で化学療法が予後を改善させたという報告はなかった。フランス6)とメモリアルスローンケタリングがんセンター(MSKCC)7)のデータベースを加え,T1a/bにおいて検討すると,計5,378例のうち,1,756例(32.7%)に化学療法が施行されていたが,2群間で化学療法が予後を改善させたという報告はなかった。
また,化学療法のレジメンについても検討されている報告が3編あった。オランダからの報告4)では,アンスラサイクリン+タキサン系:44%,アンスラサイクリン系:13%,タキサン系:8%,NCCNからの報告5)では,アンスラサイクリン系:57.4%,アンスラサイクリン+タキサン系:21.0%,タキサン系:13.8%,CMF:4.1%,またMSKCCからの報告7)ではCMF/メソトレキサート,5-フルオロウラシル,ロイコボリン(MFL):56.6%,アンスラサイクリン+タキサン系:24.8%,アンスラサイクリン系:12.4%,が投与されていた。化学療法レジメンの時代的変遷もあり,どのレジメンが適切であるかについての一定の見解は得られていない。
海外のガイドラインでは,浸潤径1 cm以下・リンパ節転移陰性のトリプルネガティブ乳癌に対して,化学療法の推奨はさまざまではあるが,根拠となる文献が示されているものはなかった。NCCNガイドライン(Ver. 1. 2021)ではT1aでは無治療,T1bでは化学療法を考慮,ザンクトガレン国際コンセンサスガイドラインではT1aでは患者ごとに,T1bではTC(ドセタキセル+シクロホスファミド)8),Pan-Asian adapted ESMO Clinical Practice Guidelinesでは腫瘍サイズによらず化学療法を推奨となっている9)。
以上より,後ろ向き研究の結果からは浸潤径1 cm以下・リンパ節転移陰性のトリプルネガティブ乳癌に対して4割以上の症例に術後化学療法が行われていたが,化学療法が予後を改善させたという報告はなく,現時点において予後の改善のために術後化学療法を勧める根拠は乏しいと考えられる。ただし,腫瘍サイズやリンパ節転移状況以外の背景因子が化学療法施行の決定に関与していた可能性があり,化学療法の有効性についての結論は出ていないため,この群に対する化学療法の効果予測因子や適切なレジメンについての検討が今後の課題である。
検索キーワード・参考にした二次資料
PubMedで“Breast neoplasms(またはbreast cancer)”,“Adjuvant”,“T1ab(または)1 cmまたはpT1ab”,“chemotherapy”のキーワードで検索した。検索期間は2021年3月までとした。195件がヒットし,一次スクリーニングでハンドサーチ4編を含む15編,二次スクリーニングで9編に絞り込んだ。
参考文献
1)Welch HG, Prorok PC, O’Malley AJ, Kramer BS. Breast-cancer tumor size, overdiagnosis, and mammography screening effectiveness. N Engl J Med. 2016;375(15):1438-47. [PMID:27732805]
2)Nishimura R, Arima N. Is triple negative a prognostic factor in breast cancer? Breast Cancer. 2008;15(4):303-8. [PMID:18369692]
3)Du ZL, Wang Y, Wang DY, Zhang L, Bian ZM, Deng Y, et al. Evaluation of a beneficial effect of adjuvant chemotherapy in patients with stage Ⅰ triple-negative breast cancer:a population-based study using the SEER 18 database. Breast Cancer Res Treat. 2020;183(2):429-38. [PMID:32647940]
4)Steenbruggen TG, van Werkhoven E, van Ramshorst MS, Dezentjé VO, Kok M, Linn SC, et al. Adjuvant chemotherapy in small node-negative triple-negative breast cancer. Eur J Cancer. 2020;135:66-74. [PMID:32554215]
5)Vaz-Luis I, Ottesen RA, Hughes ME, Mamet R, Burstein HJ, Edge SB, et al. Outcomes by tumor subtype and treatment pattern in women with small, node-negative breast cancer:a multi-institutional study. J Clin Oncol. 20140;32(20):2142-50. [PMID:24888816]
6)de Nonneville A, Gonçalves A, Zemmour C, Cohen M, Classe JM, Reyal F, et al. Adjuvant chemotherapy in pT1ab node-negative triple-negative breast carcinomas:Results of a national multi-institutional retrospective study. Eur J Cancer. 2017;84:34-43. [PMID:28780480]
7)Ho AY, Gupta G, King TA, Perez CA, Patil SM, Rogers KH, et al. Favorable prognosis in patients with T1a/T1bN0 triple-negative breast cancers treated with multimodality therapy. Cancer. 2012;118(20):4944-52. [PMID:22392492]
8)Burstein HJ, Curigliano G, Thürlimann B, Weber WP, Poortmans P, Regan MM, et al;Panelists of the St Gallen Consensus Conference. Customizing local and systemic therapies for women with early breast cancer:the St. Gallen International Consensus Guidelines for treatment of early breast cancer 2021. Ann Oncol. 2021;32(10):1216-35. [PMID:34242744]
9)Park YH, Senkus-Konefka E, Im SA, Pentheroudakis G, Saji S, Gupta S, et al. Pan-Asian adapted ESMO clinical practice guidelines for the management of patients with early breast cancer:a KSMO-ESMO initiative endorsed by CSCO, ISMPO, JSMO, MOS, SSO and TOS. Ann Oncol. 2020;31(4):451-69. [PMID:32081575]