FRQ9 原発乳癌に対する再発予防を目的とする術後薬物療法として骨吸収抑制薬(ビスホスホネート製剤,デノスマブ)は勧められるか?
背 景
乳癌の再発予防を目的とする術後薬物療法としての骨吸収抑制薬に関して,ビスホスホネート製剤についてはEBCTCGのメタアナリシス1)のサブ解析で,閉経状態(投与開始時に閉経後,または閉経前でLH-RHアナログを投与中)の患者においては乳癌死亡〔リスク比(RR)0.82,p=0.002〕,全再発(RR 0.86,p=0.002),骨転移再発(RR 0.72,p=0.0002)の有意な改善を認めた。しかし,未閉経状態の患者においては有効性が示されなかった。ビスホスホネート製剤を投与された患者群に,顎骨壊死の有意なリスク増加がみられた。コクランレビューも行われているが2),基本的に同様の結論である。ASCOの周術期の骨吸収抑制薬使用に関するガイドラインでは,「全身治療の適応となる閉経後乳癌の患者に対して,利用可能であれば,ゾレドロン酸4 mgを半年毎またはクロドロン酸1,600 mgを毎日投与」が推奨されている3)。ESMOの早期乳癌に対するガイドラインでは,「低エストロゲン状態の女性に対してはビスホスホネート製剤の使用」が推奨されている4)。
解 説
検索で同定された8試験(表1)を概説する。※画像クリックで拡大表示します
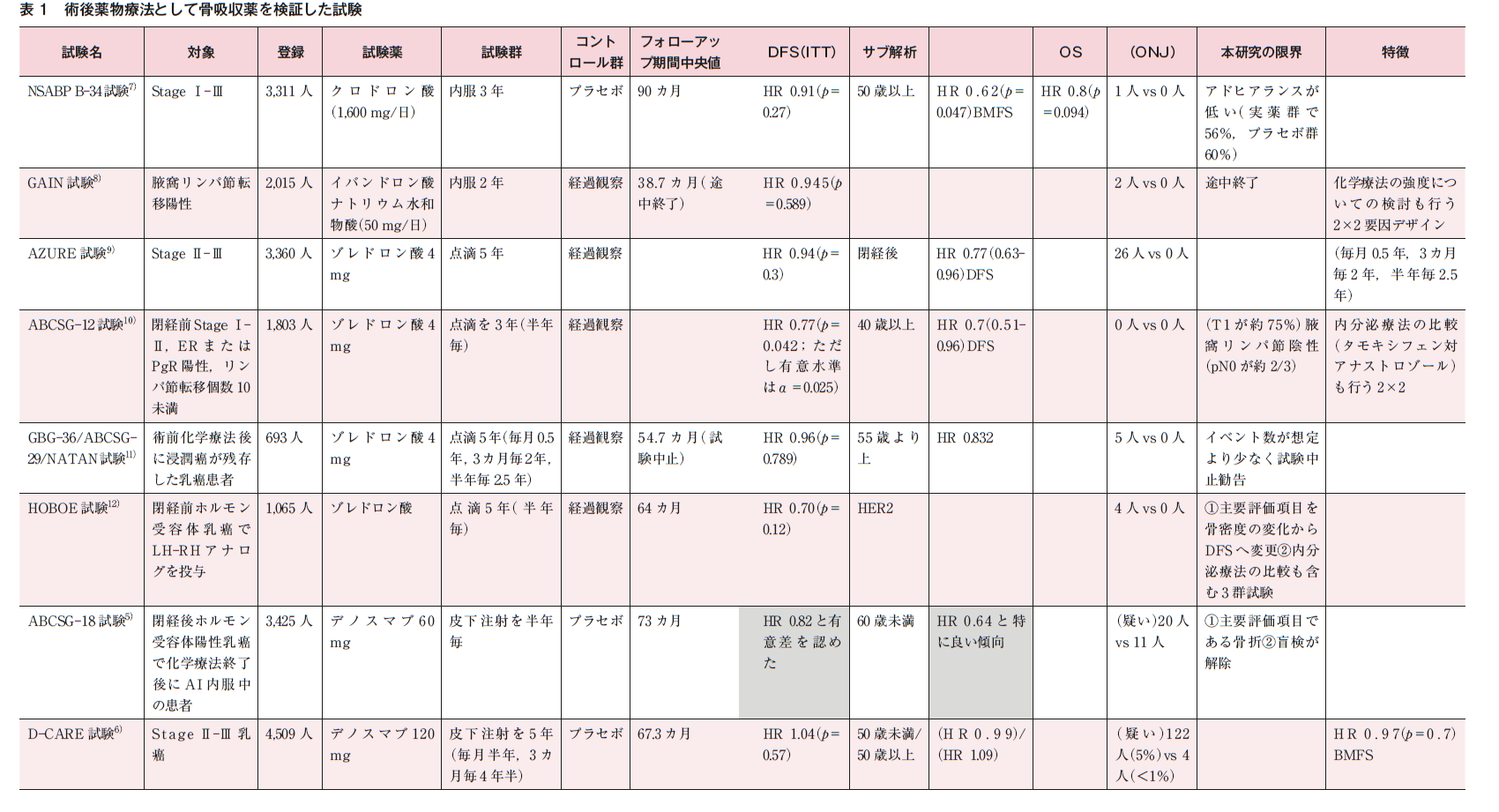
NSABP B-34試験はStage Ⅰ-Ⅲ乳癌患者を対象に,試験治療であるクロドロン酸(1,600 mg/日)内服3年とプラセボとを比較した7)。2001年1月~2004年3月に3,311人が登録された。フォローアップ期間中央値90カ月の時点の報告では,主要評価項目である無病生存期間(DFS)(ITT)ではハザード比(HR)0.91(p=0.27)と有意差がみられなかった。サブ解析で50歳以上ではBMFS(bone metastasis free survival)でHR 0.62(p=0.047),OSでもHR 0.8(p=0.094)と良い傾向がみられた。顎骨壊死(ONJ)疑いがクロドロン酸群に1人みられた。本研究の限界としてはアドヒアランスが低いこと(実薬群で56%,プラセボ群60%)が挙げられる。
GAIN試験は腋窩リンパ節転移陽性乳癌患者を対象に,試験治療であるイバンドロン酸ナトリウム水和物(50 mg/日)内服2年と経過観察とを比較した8)。2004年8月~2008年7月に2,015人が登録された。中間解析の時点でイベント数が少なく,計画になかったfutility analysisを追加し途中終了,結果の公表が勧告された。フォローアップ期間中央値38.7カ月の時点での報告は,主要評価項目であるDFSではHR 0.945(p=0.589)と有意差がみられなかった。ONJがイバンドロン酸群で2人みられた。本研究の特徴は,化学療法の強度についての検討も行う2×2要因デザインである。本研究の最大の限界は途中終了である。
AZURE試験はStage Ⅱ-Ⅲ乳癌患者を対象に,試験治療であるゾレドロン酸4 mg点滴を5年(毎月半年,3カ月毎2年,半年毎2.5年)と経過観察とを比較した。2003年9月~2006年2月に3,360人が登録された9)。フォローアップ期間中央値84カ月の時点での報告では,主要評価項目であるDFS(ITT)ではHR 0.94(p=0.3)と有意差がみられなかった。サブ解析で閉経後ではIDFS(浸潤癌の無病生存期間)においてHR 0.77(0.63-0.96)と良い傾向がみられた。特に,閉経後5年以上経過した集団においてDFSでHR 0.77と良い傾向がみられた。ONJがゾレドロン酸群で26人(プラセボ群0人)にみられた。
ABCSG-12試験は閉経前Stage Ⅰ-Ⅱ乳癌でLH-RHアナログ+内分泌療法の投与を受けるERまたはPgR陽性,かつリンパ節転移個数10未満の患者を対象に,試験治療であるゾレドロン酸4 mg点滴を3年(半年毎)と経過観察とを比較した10)。1999年6月~2006年5月に1,803人が登録された。主要評価項目であるDFS(ITT)ではHR 0.77(p=0.042;ただし有意水準はα=0.025)と有意差を認めなかった。サブ解析で40歳より上ではDFSでHR 0.7(0.51-0.96)と良い傾向がみられた。ONJはみられなかった。本研究の特徴は内分泌療法の比較(タモキシフェン対アナストロゾール)も行う2×2要因デザインの試験であること,本研究の限界は腫瘍径の小さい(T1が約75%)腋窩リンパ節陰性(pN0が約2/3)の患者が多く含まれていることである。
GBG-36/ABCSG-29/NATAN試験はアンスラサイクリン+タキサン併用術前化学療法後に浸潤癌が残存した乳癌患者を対象に,試験治療であるゾレドロン酸4 mg点滴を5年(毎月半年,3カ月毎2年,半年毎2.5年)と経過観察とを比較した11)。2005年1月~2006年9月に693人が登録された。フォローアップ期間中央値54.7カ月の時点で,イベント数が想定より少なくfutility analysisを行ったところpositiveになる確率が15%未満と判断され,独立データモニタリング委員会(IDMC)から試験中止と結果の公表を勧告された。主要評価項目であるDFS(ITT)ではHR 0.96(p=0.789)と有意差を認めなかった。サブ解析で55歳より上ではDFSでHR 0.832と若干良い傾向がみられた。ONJはゾレドロン酸群で5人(プラセボ群0人)にみられた。本研究の限界は途中終了である。
HOBOE試験は閉経前ホルモン受容体乳癌でLH-RHアナログを投与される患者を対象に,試験治療であるゾレドロン酸点滴5年(半年毎)と経過観察とを比較した12)。2004年3月~2015年8月に1,065人が登録された。フォローアップ期間中央値64カ月の時点での解析で,主要評価項目であるDFS(ITT)はHR 0.70(p=0.12)と有意差を認めなかった。サブ解析はHER2に関するもののみ行われた。ONJはゾレドロン酸群で4人(プラセボ群0人)にみられた。本研究の限界は,当初骨密度の変化を主要評価項目として開始されたものを2009年にDFSを主要評価項目として登録患者を増やした点と,内分泌療法の比較も含む3群試験(タモキシフェンvsレトロゾールvsレトロゾール+ゾレドロン酸)である点が挙げられる。
ABCSG-18試験は閉経後ホルモン受容体陽性乳癌で化学療法終了後にアロマターゼ阻害薬内服中の患者を対象に,デノスマブ60 mg皮下注射を半年毎(アロマターゼ阻害薬内服中継続)とプラセボとを比較した5)。2006年12月~2013年7月に3,425人が登録された。フォローアップ期間中央値73カ月の解析で,副次評価項目であるDFS(ITT)はHR 0.82と有意差を認めた。サブ解析で60歳未満ではDFSでHR 0.64と特に良い傾向がみられた。ONJについて,確定例は認めなかったが,疑い例がデノスマブ群に20人,プラセボ群で11人にみられた。本研究の限界は,主要評価項目である骨折までの期間が2015年に報告された際にIDMCの勧告で盲検が解除されている点が挙げられる。
D-CARE試験はStage Ⅱ-Ⅲ乳癌を対象に,試験治療であるデノスマブ120 mg皮下注射を5年(毎月半年,3カ月毎4年半)とプラセボとを比較した6)。2010年6月~2012年8月に4,509人が登録された。フォローアップ期間中央値67.3カ月の時点での解析で,副次評価項目であるDFS(ITT)はHR 1.04(p=0.57)と有意差を認めなかった。サブ解析で50歳未満(HR 0.99),50歳以上(HR 1.09)のどちらでも良い傾向はみられていない。ONJ疑いはデノスマブ群で122名(5%),プラセボ群4人(<1%)であった。主要評価項目であるBMFSでもHR 0.97(p=0.7)と有意差は認めなかった。
これらの試験で,ABCSG-18試験以外は個々の試験はネガティブであり,サブ解析で閉経後や50歳以上など低エストロゲン状態と考え得る部分集団についてのみ有用性が示唆されている試験がいくつかみられた。また,介入も経口薬,ゾレドロン酸,デノスマブとばらつきがあり,ゾレドロン酸の投与スケジュールやデノスマブの投与量・投与スケジュールにもばらつきがみられている。
これら8試験を対象に,早期乳癌に対する再発予防を目的とした骨吸収抑制薬の有用性を検討するメタアナリシスを実施した。アウトカムとしてはDFS,OS,BMFS,有害事象(ONJ,腎障害,低カルシウム血症)を検討した。
骨吸収抑制薬の投与により,DFSイベントはわずかだが統計学的有意差をもって減少した(HR 0.92,95%CI 0.85-0.99)。死亡(HR 0.94,95%CI 0.85-1.02),または骨転移再発(HR 0.95,95%CI 0.83-1.08)については有意な改善を認めなかった。有害事象に関して,顎骨壊死は有意に増加した(RR 19.8,95%CI 8.94-43.85)。腎障害(RR 0.88,95%CI 0.73-1.06)と低カルシウム血症(RR 1.65,95%CI 0.69-3.9)は有意差を認めなかった。
益と害のバランスとしては,DFSはわずかに改善するが,OSやBMFSは改善しない。また,ONJは増加するため,確実とはいえない,とした。
患者の希望については,患者の嗜好性分析はないものの,治療効果が小さい一方で有害事象(ONJ)が増加するため,大きくばらつくと判断した。
本FRQは,原発乳癌に対する再発予防を目的とする術後薬物療法として骨吸収抑制薬(ビスホスホネート製剤,デノスマブ)は勧められるかを検討する新たなCQとして提案され,エビデンスの程度,益と害のバランス,患者希望などを勘案し,推奨文案は「早期乳癌に対する再発予防を目的とした骨吸収抑制薬の投与を弱く推奨する」として提示した。しかしながら,推奨決定会議の議論において,投与薬剤,投与量,投与期間などのばらつきが大きいことなどを理由に推奨決定は困難とされ,今回もFRQとして検討することになった。
検索キーワード・参考にした二次資料
PubMedで,“Breast Neoplasms”,“Diphosphonates/bisphosphonate/Denosumab/Bone density conservation agents”,“early”,“adjuvant”のキーワードを掛け合わせ検索した。PubMedから325編,Cochrane Libraryから126編,医中誌から168編が抽出された。一次スクリーニングで13編が抽出され,二次スクリーニングでさらにDFSを報告しているランダム化試験の文献に限定した結果,8編が抽出された。
参考文献
1)Early Breast Cancer Trialists’ Collaborative Group(EBCTCG). Adjuvant bisphosphonate treatment in early breast cancer:meta-analyses of individual patient data from randomised trials. Lancet. 2015;386(10001):1353-61. [PMID:26211824]
2)O’Carrigan B, Wong MH, Willson ML, Stockler MR, Pavlakis N, Goodwin A. Bisphosphonates and other bone agents for breast cancer. Cochrane Database Syst Rev. 2017;10(10):CD003474. [PMID:29082518]
3)Dhesy-Thind S, Fletcher GG, Blanchette PS, Clemons MJ, Dillmon MS, Frank ES, et al. Use of adjuvant bisphosphonates and other bone-modifying agents in breast cancer:a cancer care ontario and american society of clinical oncology clinical practice guideline. J Clin Oncol. 2017;35(18):2062-81. [PMID:28618241]
4)Cardoso F, Kyriakides S, Ohno S, Penault-Llorca F, Poortmans P, Rubio IT, et al;ESMO Guidelines Committee. Electronic address:clinicalguidelines@esmo.org. Early breast cancer:ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2019;30(8):1194-220. [PMID:31161190]
5)Gnant M, Pfeiler G, Steger GG, Egle D, Greil R, Fitzal F, et al;Austrian Breast and Colorectal Cancer Study Group. Adjuvant denosumab in postmenopausal patients with hormone receptor-positive breast cancer(ABCSG-18):disease-free survival results from a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2019;20(3):339-51. [PMID:30795951]
6)Coleman R, Finkelstein DM, Barrios C, Martin M, Iwata H, Hegg R, et al. Adjuvant denosumab in early breast cancer(D-CARE):an international, multicentre, randomised, controlled, phase 3 trial. Lancet Oncol. 2020;21(1):60-72. [PMID:31806543]
7)Paterson AH, Anderson SJ, Lembersky BC, Fehrenbacher L, Falkson CI, King KM, et al. Oral clodronate for adjuvant treatment of operable breast cancer(National Surgical Adjuvant Breast and Bowel Project protocol B-34):a multicentre, placebo-controlled, randomised trial. Lancet Oncol. 2012;13(7):734-42. [PMID:22704583]
8)von Minckwitz G, Möbus V, Schneeweiss A, Huober J, Thomssen C, Untch M, et al. German adjuvant intergroup node-positive study:a phase Ⅲ trial to compare oral ibandronate versus observation in patients with high-risk early breast cancer. J Clin Oncol. 2013;31(28):3531-9. [PMID:23980081]
9)Coleman R, Cameron D, Dodwell D, Bell R, Wilson C, Rathbone E, et al;AZURE investigators. Adjuvant zoledronic acid in patients with early breast cancer:final efficacy analysis of the AZURE(BIG 01/04)randomised open-label phase 3 trial. Lancet Oncol. 2014;15(9):997-1006. [PMID:25035292]
10)Gnant M, Mlineritsch B, Stoeger H, Luschin-Ebengreuth G, Knauer M, Moik M, et al;Austrian Breast and Colorectal Cancer Study Group, Vienna, Austria. Zoledronic acid combined with adjuvant endocrine therapy of tamoxifen versus anastrozol plus ovarian function suppression in premenopausal early breast cancer:final analysis of the Austrian Breast and Colorectal Cancer Study Group Trial 12. Ann Oncol. 2015;26(2):313-20. [PMID:25403582]
11)von Minckwitz G, Rezai M, Tesch H, Huober J, Gerber B, Zahm DM, et al;German Breast Group and Austrian Breast and Colon Cancer Study Group Investigators. Zoledronate for patients with invasive residual disease after anthracyclines-taxane-based chemotherapy for early breast cancer―The Phase Ⅲ NeoAdjuvant Trial Add-oN(NaTaN)study(GBG 36/ABCSG 29). Eur J Cancer. 2016;64:12-21. [PMID:27323347]
12)Perrone F, De Laurentiis M, De Placido S, Orditura M, Cinieri S, Riccardi F, et al. Adjuvant zoledronic acid and letrozole plus ovarian function suppression in premenopausal breast cancer:HOBOE phase 3 randomised trial. Eur J Cancer. 2019;118:178-186. [PMID:31164265]