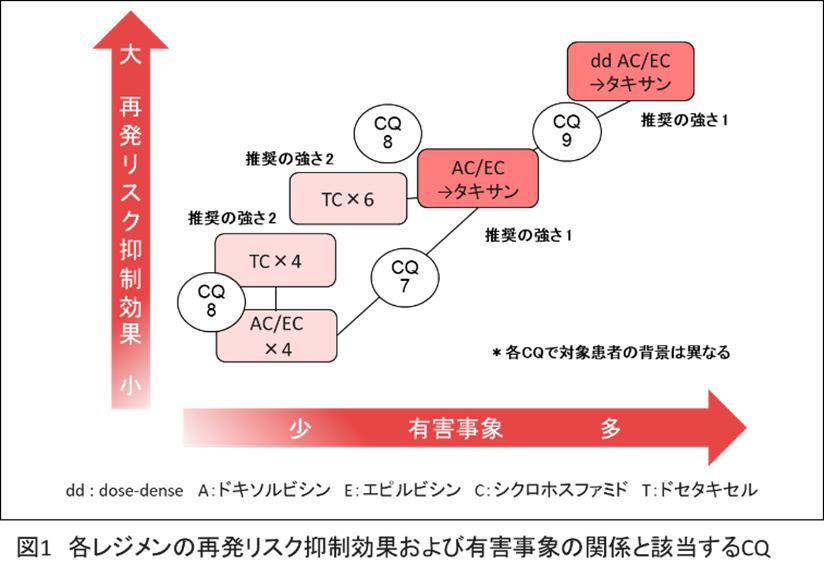
CQ7 化学療法を行うHER2陰性の早期乳癌に対して,アンスラサイクリンとタキサンの順次投与は勧められるか?
背 景・目 的
タキサンはアンスラサイクリンと交差耐性が少ないと考えられ,術後化学療法にタキサンを追加することで予後の改善が期待される。アンスラサイクリンを含んだ化学療法にタキサンを順次投与として併用することの意義を検討する。
解 説
アンスラサイクリンによる術後化学療法にタキサンを追加することの意義を検証した,2019年にコクランから出されたシステマティック・レビュー1)を利用した。同システマティック・レビューでは2018年7月16日までの文献が対象とされ,20件のランダム化比較試験(RCT)が抽出されていた。それ以降の文献検索も施行したが,本CQに合致するRCTは認めなかった。そこで,本CQでは先に述べたシステマティック・レビューに含まれる19件のRCTを対象とした2)~20)。19件のRCTのうち13件はリンパ節転移陽性のみを対象としており,1件のみがホルモン受容体陰性HER2陰性のみを対象としていた。
全生存期間(OS)の延長と無病生存期間(DFS)の延長は,コクランのシステマティック・レビューで報告されている。OSの延長は18件のRCTから24,764例を対象に評価され,ハザード比(HR)0.86(95%CI 0.81-0.91)と統計学的に有意にOSが改善され,そのイベント割合はタキサン非併用群で18.1%,タキサン併用群で15.3%であった。DFSの延長は,19件のRCTから26,866例が対象となる20個の比較がメタアナリシスで評価され,HR 0.86(95%CI 0.82-0.90)と統計学的に有意にDFSが改善され,そのイベント割合はタキサン非併用群で27.9%,タキサン併用群で24.1%であった。
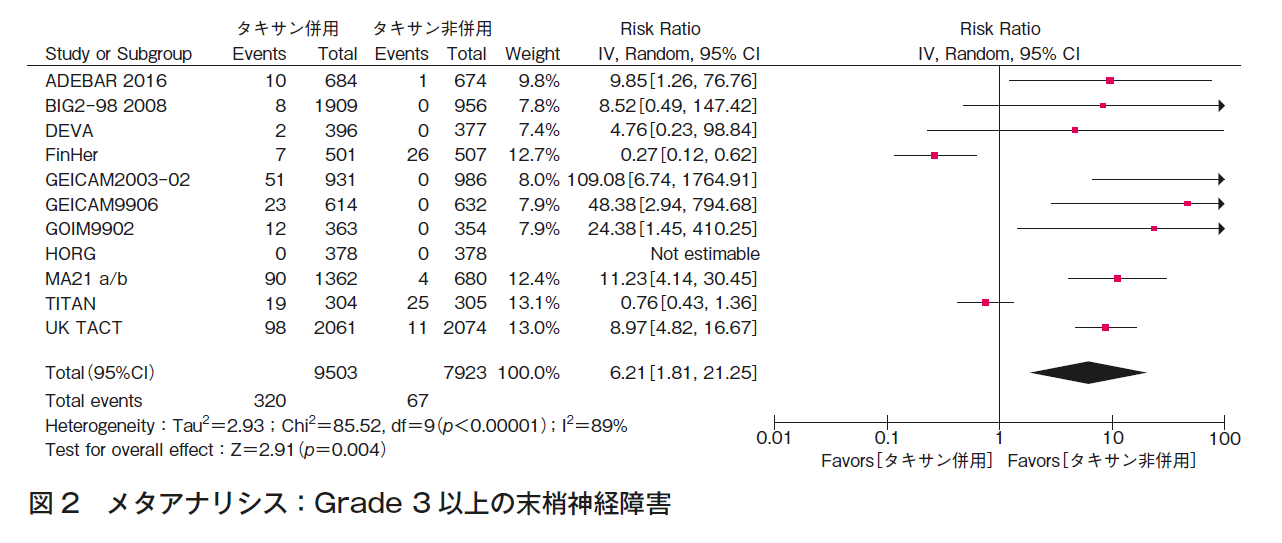
害について,QOLの評価は2件のRCTから356例を対象としたが,両試験で評価の方法が一致しておらず,統合解析はできなかった。2件のRCTともにそれぞれの評価でQOLの有意な低下を認めず,定性的な評価としてQOLが低下する可能性は低いと判断した。ただし,いずれの試験も非盲検であることや一部の症例での解析であることからバイアスリスクが高く,症例数が少ないことなどから,エビデンスの確実性は非常に低いと判断した。次に,Grade 3以上の末梢神経障害については11件のRCTから17,426例を対象に評価した。リスク比が6.21(95%CI 1.81-21.25)と統計学的に有意にリスクが増加していた(図2)。タキサン非併用群で0.8%,タキサン併用群で3.4%であり,併用により2.6%増加した。また,高い非一貫性が認められたが,対照群の化学療法が多様であった影響と考えられた。発熱性好中球減少症は10件のRCTから16,068例を対象に評価し,リスク比1.73(95%CI 0.90-3.33)と有意なリスクの増加は認めなかったが,増加の傾向は認められた。Grade 3以上の有害事象は3件のRCTから8,008例を対象に評価し,リスク比は1.03(95%CI 1.02-1.04,p<0.00001)と統計学的に有意に増加したが,絶対値の差はわずかであった。
益と害のバランスは,明確な益がある一方で,害の増加はあるものの軽微であることから,益が明らかに上回ると判断した。エビデンスの強さは質の高いRCTが複数あることから強いと判断した。患者の希望は,末梢神経障害などの有害事象が増加するが,高いエビデンスで予後の改善が示されていることから,タキサンの順次投与を併用する方針は多くの症例で一致すると考えた。また,前述のように19のRCTのうち13件はリンパ節転移陽性のみを対象としており,リンパ節転移陰性でのタキサン順次投与は適応を慎重に検討する必要がある。
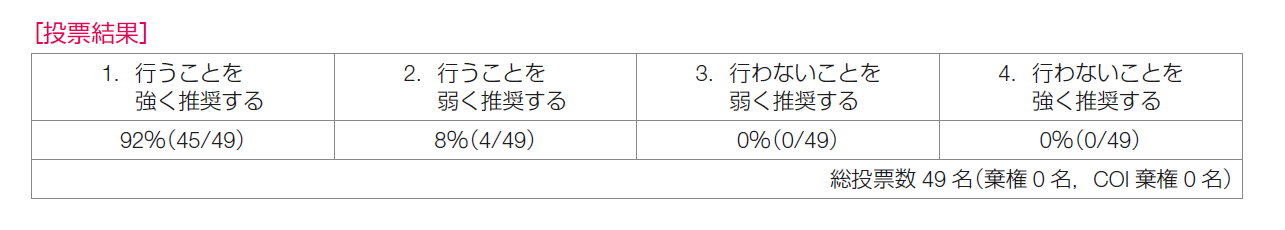
推奨決定会議の投票の結果は,「行うことを強く推奨する 45/49,合意率 92%」,「行うことを弱く推奨する 4/49」であり,推奨は「再発リスクが高い場合は,アンスラサイクリンとタキサンの順次投与を強く推奨する」とした。ただし,末梢神経障害などの有害事象が増加することに注意が必要である。
検索キーワード・参考にした二次資料
PubMed,医中誌,Cochrane Libraryで,#1(breast neoplasms)or(breast cancer*),#2((adjuvant or postoperative or preoperative or neoadjuvant)and(chemotherapy or(drug therapy))),#3(anthracyclines or doxorubicin or epirubicin or anthracyclines),#4(taxoids or paclitaxel or docetaxel or nab-paclitaxel)をキーワードとし,検索を行った。検索期間は2021年6月8日までとした。
その結果,1,570編の論文が抽出された。Cochrane(2019)が2018年7月18日までを検索期間としており,それ以降の論文を対象に一次・二次スクリーニングを行ったところ,本CQの主旨に合致する論文は認めなかった。
参考文献
1)Willson ML, Burke L, Ferguson T, Ghersi D, Nowak AK, Wilcken N. Taxanes for adjuvant treatment of early breast cancer. Cochrane Database Syst Rev. 2019;9(9):CD004421. [PMID:31476253]
2)Janni W, Harbeck N, Rack B, Augustin D, Jueckstock J, Wischnik A, et al. Randomised phase Ⅲ trial of FEC120 vs EC-docetaxel in patients with high-risk node-positive primary breast cancer:final survival analysis of the ADEBAR study. Br J Cancer. 2016;114(8):863-71. [PMID:27031854]
3)Francis P, Crown J, Di Leo A, Buyse M, Balil A, Andersson M, et al;BIG 02-98 Collaborative Group. Adjuvant chemotherapy with sequential or concurrent anthracycline and docetaxel:Breast International Group 02-98 randomized trial. J Natl Cancer Inst. 2008;100(2):121-33. [PMID:18182617]
4)Boccardo F, Amadori D, Guglielmini P, Sismondi P, Farris A, Agostara B, et al. Epirubicin followed by cyclophosphamide, methotrexate and 5-fluorouracil versus paclitaxel followed by epirubicin and vinorelbine in patients with high-risk operable breast cancer. Oncology. 2010;78(3-4):274-81. [PMID:20530973]
5)Henderson IC, Berry DA, Demetri GD, Cirrincione CT, Goldstein LJ, Martino S, et al. Improved outcomes from adding sequential paclitaxel but not from escalating doxorubicin dose in an adjuvant chemotherapy regimen for patients with node-positive primary breast cancer. J Clin Oncol. 2003;21(6):976-83. [PMID:12637460]
6)Coombes RC, Bliss JM, Espie M, Erdkamp F, Wals J, Tres A, et al. Randomized, phase Ⅲ trial of sequential epirubicin and docetaxel versus epirubicin alone in postmenopausal patients with node-positive breast cancer. J Clin Oncol. 2011;29(24):3247-54. [PMID:21768453]
7)Joensuu H, Bono P, Kataja V, Alanko T, Kokko R, Asola R, et al. Fluorouracil, epirubicin, and cyclophosphamide with either docetaxel or vinorelbine, with or without trastuzumab, as adjuvant treatments of breast cancer:final results of the FinHer Trial. J Clin Oncol. 2009;27(34):5685-92. [PMID:19884557]
8)Martín M, Ruiz A, Ruiz Borrego M, Barnadas A, González S, Calvo L, et al. Fluorouracil, doxorubicin, and cyclophosphamide(FAC)versus FAC followed by weekly paclitaxel as adjuvant therapy for high-risk, node-negative breast cancer:results from the GEICAM/2003-02 study. J Clin Oncol. 2013;31(20):2593-9. [PMID:23733779]
9)Martín M, Rodríguez-Lescure A, Ruiz A, Alba E, Calvo L, Ruiz-Borrego M, et al. Molecular predictors of efficacy of adjuvant weekly paclitaxel in early breast cancer. Breast Cancer Res Treat. 2010;123(1):149-57. [PMID:20037779]
10)Vici P, Brandi M, Giotta F, Foggi P, Schittulli F, Di Lauro L, et al. A multicenter phase Ⅲ prospective randomized trial of high-dose epirubicin in combination with cyclophosphamide(EC)versus docetaxel followed by EC in node-positive breast cancer. GOIM(Gruppo Oncologico Italia Meridionale)9902 study. Ann Oncol. 2012;23(5):1121-9. [PMID:21965475]
11)Fountzilas G, Skarlos D, Dafni U, Gogas H, Briasoulis E, Pectasides D, et al. Postoperative dose-dense sequential chemotherapy with epirubicin, followed by CMF with or without paclitaxel, in patients with high-risk operable breast cancer:a randomized phase Ⅲ study conducted by the Hellenic Cooperative Oncology Group. Ann Oncol. 2005;16(11):1762-71. [PMID:16148021]
12)Polyzos A, Malamos N, Boukovinas I, Adamou A, Ziras N, Kalbakis K, et al. FEC versus sequential docetaxel followed by epirubicin/cyclophosphamide as adjuvant chemotherapy in women with axillary node-positive early breast cancer:a randomized study of the Hellenic Oncology Research Group(HORG). Breast Cancer Res Treat. 2010;119(1):95-104. [PMID:19636702]
13)Mamounas EP, Bryant J, Lembersky B, Fehrenbacher L, Sedlacek SM, Fisher B, et al. Paclitaxel after doxorubicin plus cyclophosphamide as adjuvant chemotherapy for node-positive breast cancer:results from NSABP B-28. J Clin Oncol. 2005;23(16):3686-96. [PMID:15897552]
14)Coudert B, Asselain B, Campone M, Spielmann M, Machiels JP, Pénault-Llorca F, et al;UNICANCER Breast Group. Extended benefit from sequential administration of docetaxel after standard fluorouracil, epirubicin, and cyclophosphamide regimen for node-positive breast cancer:the 8-year follow-up results of the UNICANCER-PACS01 trial. Oncologist. 2012;17(7):900-9. [PMID:22610153]
15)Roy C, Choudhury KB, Pal M, Saha A, Bag S, Banerjee C. Adjuvant chemotherapy with six cycles of AC regimen versus three cycles of AC regimen followed by three cycles of Paclitaxel in node-positive breast cancer. Indian J Cancer. 2012;49(3):266-71. [PMID:23238142]
16)Sakr H, Hamed RH, Anter AH, Yossef T. Sequential docetaxel as adjuvant chemotherapy for node-positive or/and T3 or T4 breast cancer:clinical outcome(Mansoura University). Med Oncol. 2013;30(1):457. [PMID:23322524]
17)Forestieri V. Docetaxel in adjuvant therapy of breast cancer:results of the TAXIT 216 multicenter phase Ⅲ trial. Naples, University of Naples Federico II, 2008.
18)Yardley DA, Arrowsmith ER, Daniel BR, Eakle J, Brufsky A, Drosick DR, et al. TITAN:phase Ⅲ study of doxorubicin/cyclophosphamide followed by ixabepilone or paclitaxel in early-stage triple-negative breast cancer. Breast Cancer Res Treat. 2017;164(3):649-58. [PMID:28508185]
19)Ellis P, Barrett-Lee P, Johnson L, Cameron D, Wardley A, O’Reilly S, et al;TACT Trial Management Group;TACT Trialists. Sequential docetaxel as adjuvant chemotherapy for early breast cancer(TACT):an open-label, phase Ⅲ, randomised controlled trial. Lancet. 2009;373(9676):1681-92. [PMID:19447249;PMCID:PMC2687939]
20)Burnell M, Levine MN, Chapman JA, Bramwell V, Gelmon K, Walley B, et al. Cyclophosphamide, epirubicin, and fluorouracil versus dose-dense epirubicin and cyclophosphamide followed by paclitaxel versus doxorubicin and cyclophosphamide followed by paclitaxel in node-positive or high-risk node-negative breast cancer. J Clin Oncol. 2010;28(1):77-82. [PMID:19901117]