CQ4 浸潤性乳癌に対して,術後5年間の内分泌療法後に内分泌療法の追加投与は勧められるか?
背 景・ 目 的
ホルモン受容体陽性乳癌の術後内分泌療法として,タモキシフェンおよびアロマターゼ阻害薬(閉経後)が推奨される(☞薬物CQ2,3参照)が,本CQでは,その至適治療期間として,5年を超えた延長投与について検討した。
解 説
1)タモキシフェン5年投与後,タモキシフェン5年追加投与
タモキシフェン5年投与後の延長投与を検討した試験として5試験(ATLAS試験1),NSABP B-14試験2),Scottish試験3),ECOG試験4),aTTom試験5))が同定された。
このうち,aTTom試験は,大規模試験であるが論文化されていないためメタアナリシスから除外し,ATLAS試験,NSABP B-14試験,Scottish試験,ECOG試験についてメタアナリシスを行った結果,タモキシフェン10年投与によりタモキシフェン5年投与と比べ,無病生存期間(DFS)〔n=8,480,ハザード比(HR)0.95,95%CI 0.68-1.32,p=0.75〕,全生存期間(OS)(n=8,533,HR 1.10,95%CI 0.82-1.47,p=0.51)に有意な改善を認めなかった。NSABP B-14試験は,リンパ節転移陰性症例のみが対象であり,intention to treat(ITT)解析ではないこと,Scottish試験,ECOG試験は,ホルモン受容体陽性症例に限らず対象としていること,また大規模なaTTom試験を統合解析できなかったことから,この解析のバイアスリスクは非常に深刻であると判断した。
ATLAS試験は,オープンラベルのランダム化第Ⅲ相試験で,タモキシフェン5年投与終了後の早期乳癌症例を対象に,タモキシフェン5年追加投与群と経過観察群とにランダム化し,再発率,乳癌死亡率,有害事象を検討した大規模な試験である。ホルモン受容体陽性乳癌における結果(n=6,846)が報告されている1)。再発率はリスク比(RR)0.84(95%CI 0.76-0.94,p=0.002)と追加投与による有意なリスク減少を認めた。特に術後10年以降では再発リスクを25%減少する効果を認めた。乳癌死亡率もRR 0.87(95%CI 0.78-0.97,p=0.01)と有意なリスク減少を認めた。
aTTom試験はまだ論文化されていないが,aTTom試験とATLAS試験の統合解析(n=17,477)の報告では,乳癌死亡率はタモキシフェン5年追加投与により減少した(RR 0.85,95%CI 0.77-0.94,p=0.001)6)。この傾向は,5~9年(RR 0.97,95%CI 0.84-1.15)よりも10年以降でより顕著に認められた(RR 0.75,95%CI 0.65-0.86,p=0.00004)。タモキシフェン5年追加投与により子宮体癌の発症(RR 1.74,95%CI 1.30-2.34),静脈血栓症・肺血栓塞栓症(RR 1.87,95%CI 1.13-3.07)のリスク上昇を認めた(タモキシフェンによる子宮体癌のリスクについては薬物BQ2を参照)。
最も大規模な試験であり,バイアスリスクの低いaTTom試験とATLAS試験の統合解析の結果に基づくと,タモキシフェン5年追加投与は,乳癌死亡を減少する。一方で,害として子宮体癌,静脈血栓症・肺血栓塞栓症の発症リスクは上昇することから,益として期待される絶対的リスク減少効果の大小により益と害のバランスは変わり得る。リンパ節転移陰性など再発リスクの低い早期癌では,タモキシフェン5年追加投与による再発・死亡リスクの絶対的リスク減少効果が大きくはないため,害とのバランスを十分に考慮して適応を判断すべきである。一方,再発リスクが高いと考えられる場合は,益が害を上回ると考えられる。
患者希望については,再発リスクの低い早期乳癌患者では,益としての再発リスク減少に対する期待と,長期に及ぶ有害事象による害とのバランスについて,捉え方が一貫しないと考えられる。再発リスクの高い乳癌患者においては,患者の希望のばらつきは少ないと考える。
推奨決定会議においては,エビデンスの強さ,乳癌死亡の改善の程度,有害事象などが議論され,投票が行われた。タモキシフェン5年投与後にタモキシフェン5年追加投与を行うことについては,行うこと自体は推奨で一致したものの,3回投票を行ったが「推奨の強さ」を決定することはできなかった。3回の投票の結果は下記の通りであった。
1回目は「行うことを強く推奨する」は,29/47(62%),「行うことを弱く推奨する」18/47(38%)であり,さらに議論を重ねたのちに行った2回目の投票では,「行うことを強く推奨する」は,23/47(49%),「行うことを弱く推奨する」24/47(51%)であった。3回目の投票では,「行うことを強く推奨する」20/47(43%),「行うことを弱く推奨する」27/47(57%)であった。最終的に,推奨決定会議において「推奨の強さ」は決定できなかった。
2)内分泌療法5年投与終了後,アロマターゼ阻害薬2~5年追加投与
内分泌療法投与終了後にアロマターゼ阻害薬の追加投与を検討した試験として,MA.17試験7),NSABP B-33試験8),ANZ0501-LATER試験9),MA.17R試験10),NSABP B-42試験11),AERAS試験12),ABCSG 6a試験13),DATA試験14),GIM-4試験15)がある。また,ABCSG B16/SALSA試験16)やIDEAL試験17)では,アロマターゼ阻害薬2(~3)年追加と5年追加が比較されている。
メタアナリシスの結果,内分泌療法5年投与終了後,アロマターゼ阻害薬2~5年追加投与により,DFS(HR 0.65,95%CI 0.57-0.74,p<0.00001)は有意に改善し,OSも改善傾向を認めた(HR 0.85,95%CI 0.71-1.04,p=0.11)が有意差は認めなかった(図1)。
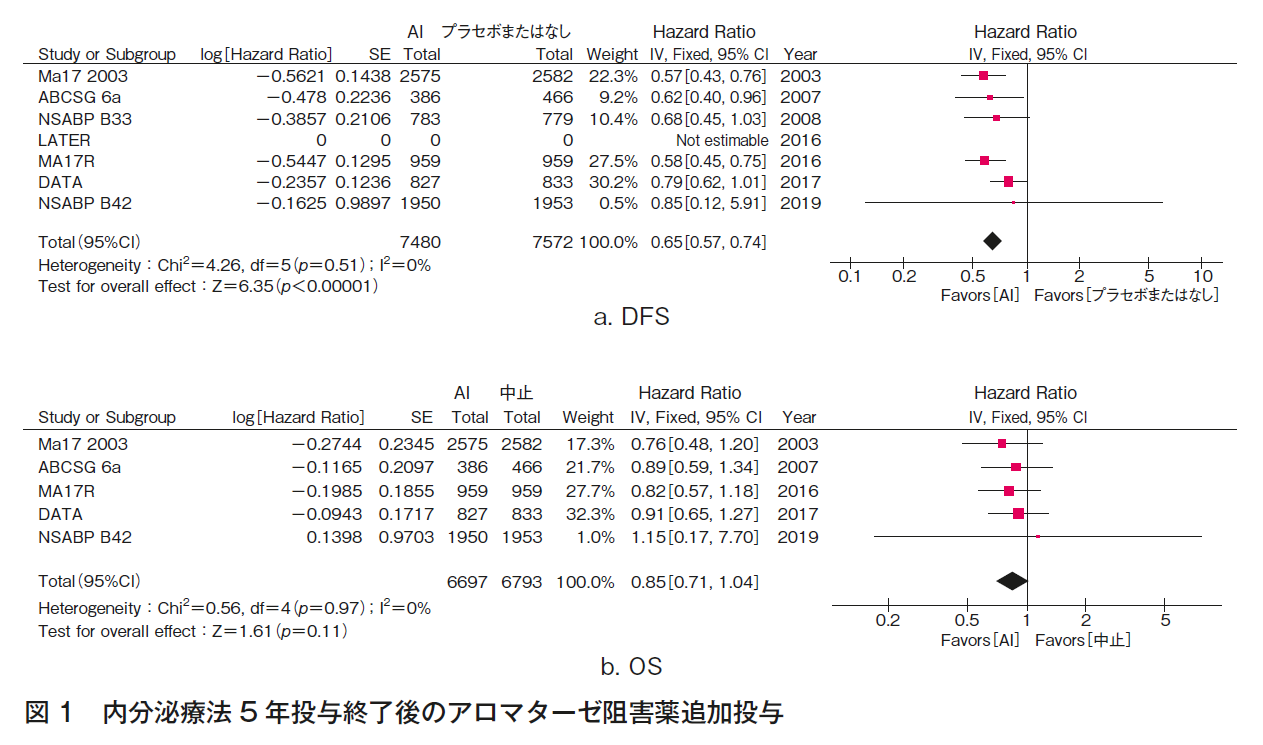
また,学会発表ではあるものの,5年以上の内分泌療法後に,アロマターゼ阻害薬の追加投与を検討したEBCTCGによるメタアナリシスの結果でも,アロマターゼ阻害薬の追加投与により再発の減少が認められている(n=22,192,RR 0.764,95%CI 0.700-0.835,p<0.00001)18)。この解析では,アロマターゼ阻害薬追加前の内分泌療法がタモキシフェンの場合(n=7,483,RR 0.67,95%CI 0.55-0.83),アロマターゼ阻害薬の場合(n=3,322,RR 0.76,95%CI 0.56-1.02),タモキシフェンからアロマターゼ阻害薬へ切り替えた場合(n=11,387,RR 0.82,95%CI 0.70-0.97)のいずれにおいても有効性が示唆されている。
有害事象については,骨痛,骨粗鬆症,骨折,心血管イベントについてメタアナリシスを行った。骨痛(RR 1.22,95%CI 1.10-1.35),骨粗鬆症(RR 1.21,95%CI 1.10-1.33)のリスク上昇が認められた。骨折(RR 1.15,95%CI 0.99-1.34),心血管イベント(RR 1.17,95%CI 0.99-1.38)については増加傾向が認められたが有意差には至らなかった。
いずれも質の高いランダム化比較試験に基づく結果であり,エビデンスの強さは「強」とした。
益と害のバランスについては,再発リスクの大きさと再発抑制効果,有害事象により異なると考えられる。再発リスクが高い場合については,益が害に勝ると考えられるが,再発リスクが低い場合については,長期の内分泌療法による有害事象も加味すると,患者の希望についてもばらつきが予測される。
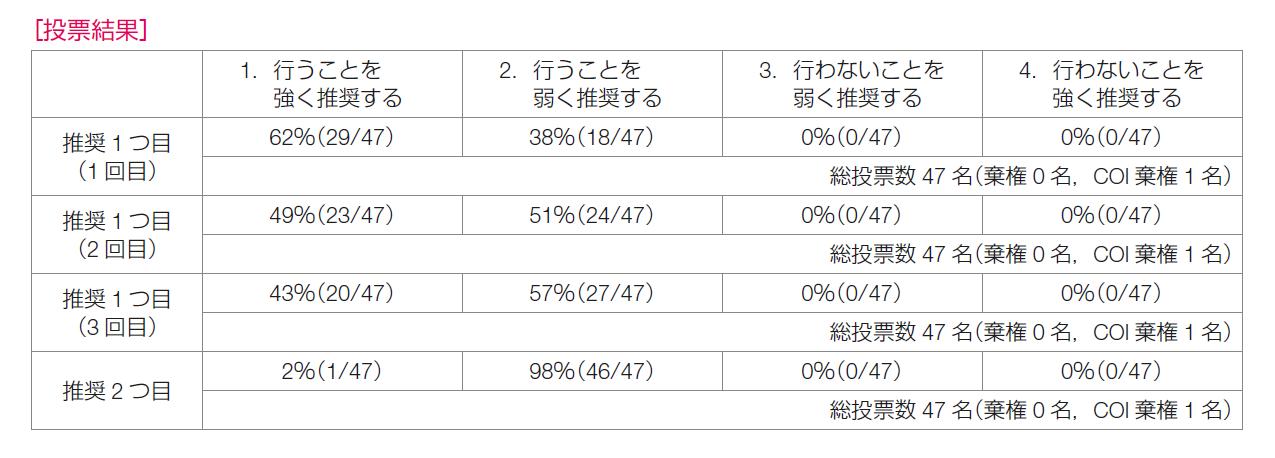
推奨決定会議の投票の結果は,「行うことを強く推奨する」が1/47(2%),「行うことを弱く推奨する」が46/47(98%)であり,推奨は「内分泌療法5年投与終了後にアロマターゼ阻害薬2~5年追加投与を行うことを弱く推奨する」とした。
2023年11月改訂時に,2022年版作成時のメタアナリシスに含まれていなかったAERAS試験(n=1,697)12)及びGIM4試験(n=2,056)15)を含めて再解析を実施した。再解析においてもアロマターゼ阻害薬2~5年追加投与によるDFSの改善が見られたが(介入群のイベント発生率 10.2% vs. 対象群のイベント発生率 13.4%,HR 0.72,95%CI 0.64 - 0.82, p<0.00001),OS に有意な差は見られないままであった(6.3% vs. 6.7%,HR 0.94,95%CI 0.82 - 1.08, p=0.37) 。有害事象については、アロマターゼ阻害薬2~5年追加投与により骨痛(11.9% vs. 9.8%, RR 1.23,95%CI 1.14-1.33, p<0.0001),骨粗鬆症(15.0% vs. 12.1%,RR 1.39,95%CI 1.11-1.73, p=0.004)、骨折(5.1% vs. 3.9%,RR 1.32,95%CI 1.15-1.51, p<0.0001)の有意なリスク増加が見られた。
術後アロマターゼ阻害薬の投与期間について検討したメタアナリシスの報告では,内分泌療法10年と7~8年の比較(ABCSG B16/SALSA試験,IDEAL試験)では,DFS(HR 0.98,95%CI 0.87-1.11)に有意な差を認めない19)。一方,内分泌療法5年との比較では,10年投与(AERAS試験,MA.17試験,NSABP B-33試験,NSABP B-42試験)ではDFSは有意に改善し,その程度(HR 0.67,95%CI 0.52-0.85)は7~8年投与(ABCSG 6a試験,DATA試験,GIM-4試験)におけるDFSの改善(HR 0.79,95%CI 0.69-0.91)よりも大きい可能性があり,10年投与に対して7~8年投与が非劣性であるとは証明されていない。一方,ABCSG B16/SALSA試験では,10年投与により骨折が増加した(HR 1.35,95%CI 1.00-1.84)。
以上より,アロマターゼ阻害薬の追加期間については,再発リスクと有害事象を検討し,2~3年とするか5年とするかを判断することが勧められる。
[投票結果]
検索キーワード・参考にした二次資料
PubMedで,“Breast Neoplasms”,“Chemotherapy, Adjuvant”,“Drug administration schedule”,“Antineoplastic Agents, Hormonal”,“Tamoxifen”,“Gonadotropin-Releasing Hormone”,“Estrogen Antagonists”,“Receptors, Estrogen”,“Aromatase Inhibitors”のキーワードと同義語で検索した。医中誌・Cochrane Libraryも同等のキーワードで検索した。検索期間は2018年11月までとし,PubMedから631編,Cochraneから47編,医中誌から5編,ハンドサーチにて2編を抽出した。一次スクリーニングにて22編を抽出し,二次スクリーニングとして14編を抽出した。
ガイドライン改訂に際して,検索期間を2021年3月までとして検索を追加し,PubMedから72編,Cochrane Libraryから132編,医中誌から1編が追加で抽出され,それ以外にハンドサーチで9編の論文が追加された。一次スクリーニングで34編の論文が追加され,二次スクリーニングで29編の論文が抽出された。
全生存期間,無再発生存期間,治療関連有害事象に関してシステマティック・レビューを行った。
参考文献
1)Davies C, Pan H, Godwin J, Gray R, Arriagada R, Raina V, et al;Adjuvant Tamoxifen:Longer Against Shorter(ATLAS)Collaborative Group. Long-term effects of continuing adjuvant tamoxifen to 10 years versus stopping at 5 years after diagnosis of oestrogen receptor-positive breast cancer:ATLAS, a randomised trial. Lancet. 2013;381(9869):805-16. [PMID:23219286]
2)Fisher B, Dignam J, Bryant J, DeCillis A, Wickerham DL, Wolmark N, et al. Five versus more than five years of tamoxifen therapy for breast cancer patients with negative lymph nodes and estrogen receptor-positive tumors. J Natl Cancer Inst. 1996;88(21):1529-42. [PMID:8901851]
3)Stewart HJ, Forrest AP, Everington D, McDonald CC, Dewar JA, Hawkins RA, et al. Randomised comparison of 5 years of adjuvant tamoxifen with continuous therapy for operable breast cancer. The Scottish Cancer Trials Breast Group. Br J Cancer. 1996;74(2):297-9. [PMID:8688340]
4)Tormey DC, Gray R, Falkson HC. Postchemotherapy adjuvant tamoxifen therapy beyond five years in patients with lymph node-positive breast cancer. Eastern Cooperative Oncology Group. J Natl Cancer Inst. 1996;88(24):1828-33. [PMID:8961972]
5)Gray RG, Rea D, Handley K, Bowden SJ, Perry P, Earl HM, et al. aTTom:long-term effects of continuing adjuvant tamoxifen to 10 years versus stopping at 5 years in 6,953 women with early breast cancer. J Clin Oncol. 2013;31(18_suppl):5.
6)Schiavon G, Smith IE. Status of adjuvant endocrine therapy for breast cancer. Breast Cancer Res. 2014;16(2):206. [PMID:25032258]
7)Goss PE, Ingle JN, Martino S, Robert NJ, Muss HB, Piccart MJ, et al. Randomized trial of letrozole following tamoxifen as extended adjuvant therapy in receptor-positive breast cancer:updated findings from NCIC CTG MA.17. J Natl Cancer Inst. 2005;97(17):1262-71. [PMID:16145047]
8)Mamounas EP, Jeong JH, Wickerham DL, Smith RE, Ganz PA, Land SR, et al. Benefit from exemestane as extended adjuvant therapy after 5 years of adjuvant tamoxifen:intention-to-treat analysis of the National Surgical Adjuvant Breast and Bowel Project B-33 trial. J Clin Oncol. 2008;26(12):1965-71. [PMID:18332472]
9)Zdenkowski N, Forbes JF, Boyle FM, Kannourakis G, Gill PG, Bayliss E, et al;Australia and New Zealand Breast Cancer Trials Group. Observation versus late reintroduction of letrozole as adjuvant endocrine therapy for hormone receptor-positive breast cancer(ANZ0501 LATER):an open-label randomised, controlled trial. Ann Oncol. 2016;27(5):806-12. [PMID:26861603]
10)Goss PE, Ingle JN, Pritchard KI, Robert NJ, Muss H, Gralow J, et al. Extending aromatase-inhibitor adjuvant therapy to 10 years. N Engl J Med. 2016;375(3):209-19. [PMID:27264120]
11)Mamounas EP, Bandos H, Lembersky BC, Jeong JH, Geyer CE Jr, Rastogi P, et al. Use of letrozole after aromatase inhibitor-based therapy in postmenopausal breast cancer(NRG Oncology/NSABP B-42):a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2019;20(1):88-99. [PMID:30509771]
12)Iwase, T., Saji S., Iijima K., Higaki K., Ohtani S. et al; Postoperative Adjuvant Anastrozole for 10 or 5 Years in Patients With Hormone Receptor-Positive Breast Cancer: AERAS, a Randomized Multicenter Open-Label Phase III Trial. J Clin Oncol 2023; 41(18): 3329-3338. [PMID:37079878]
13)Jakesz R, Greil R, Gnant M, Schmid M, Kwasny W, Kubista E, et al;Austrian Breast and Colorectal Cancer Study Group. Extended adjuvant therapy with anastrozole among postmenopausal breast cancer patients:results from the randomized Austrian Breast and Colorectal Cancer Study Group Trial 6a. J Natl Cancer Inst. 2007;99(24):1845-53. [PMID:18073378]
14)Tjan-Heijnen VCG, van Hellemond IEG, Peer PGM, Swinkels ACP, Smorenburg CH, van der Sangen MJC, et al;Dutch Breast Cancer Research Group(BOOG)for the DATA Investigators. Extended adjuvant aromatase inhibition after sequential endocrine therapy(DATA):a randomised, phase 3 trial. Lancet Oncol. 2017;18(11):1502-11. [PMID:29031778]
15)Del Mastro L, Mansutti M, Bisagni G, Ponzone R, Durando A, Amaducci L, et al;Gruppo Italiano Mammella investigators. Extended therapy with letrozole as adjuvant treatment of postmenopausal patients with early-stage breast cancer:a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol. 2021;22(10):1458-67. [PMID:34543613]
16)Gnant M, Fitzal F, Rinnerthaler G, Steger GG, Greil-Ressler S, Balic M, et al;Austrian Breast and Colorectal Cancer Study Group. Duration of adjuvant aromatase-inhibitor therapy in postmenopausal breast cancer. N Engl J Med. 2021;385(5):395-405. [PMID:34320285]
17)Blok EJ, Kroep JR, Meershoek-Klein Kranenbarg E, Duijm-de Carpentier M, Putter H, van den Bosch J, et al;IDEAL Study Group. Optimal duration of extended adjuvant endocrine therapy for early breast cancer;results of the IDEAL trial(BOOG 2006-05). J Natl Cancer Inst. 2018;110(1). [PMID:28922787]
18)R Gray;Early Breast Cancer Trialists’ Collaborative Group. Effects of prolonging adjuvant aromatase inhibitor therapy beyond five years on recurrence and cause-specific mortality:an EBCTCG meta-analysis of individual patient data from 12 randomised trials including 24,912 women. Cancer Res 2019;79(4 Suppl):Abstract nr GS3-03.
19)Chen J, Zhang X, Lu Y, Zhang T, Ouyang Z, Sun Q. Optimal duration of endocrine therapy with extended aromatase inhibitors for postmenopausal patients with hormone receptor-positive breast cancer:a meta-analysis. Breast Cancer. 2021;28(3):630-43. [PMID:33387283]