CQ22 閉経後ホルモン受容体陽性HER2陰性転移・再発乳癌に対する三次治療以降の内分泌療法として,何が推奨されるか?
背 景・目 的
閉経後ホルモン受容体陽性転移・再発乳癌に対しては,生命を脅かす病変がない場合,病状コントロールと延命効果に期待した薬物療法として,化学療法と比較して副作用がより少ない内分泌療法が推奨される1)。三次治療以降も内分泌療法抵抗性と判断するまでは内分泌療法を継続することを検討する2)。三次治療以降の内分泌療法として最適な選択肢を検討した。
解 説
1)非ステロイド性アロマターゼ阻害薬耐性の場合のエキセメスタン+エベロリムス併用療法について
BOLERO-2試験において,非ステロイド性アロマターゼ阻害薬(AI)既治療例の二次治療以降の内分泌療法として,エベロリムスとエキセメスタン併用とエキセメスタン単剤療法が比較された3)~5)。併用群は全体集団の無増悪生存期間(PFS)を有意に延長〔ハザード比(HR)0.43,95%CI 0.35-0.54,p<0.001〕しており,三次治療以降の症例におけるサブグループ解析結果も同様の傾向を認めた。全体集団で全奏効割合(ORR),クリニカルベネフィット率(CBR)は併用群で良好であり,全生存期間(OS)は有意差を認めなかったが,治療ラインごとの比較はなされていない(☞薬物CQ21参照)。以上より,1つの質の高いランダム化比較試験(RCT)があるが,サブグループ解析のみであり,エビデンスの強さは「弱」とした。
全体集団では,Grade 3以上の有害事象が,エキセメスタン単剤では8.4%であるのに対して,エベロリムスとエキセメスタン併用療法では40.9%と,高い頻度で認めた。生活の質(QOL)について,EORTC QLQ-C30スコアが5%以上低下するまでの期間(TDD)は併用群のほうが長かった(8.3カ月vs 5.8カ月,p=0.0084)6)。
三次治療以降の症例のみでのサブグループ解析結果は報告されていないが,益が害を上回る可能性がある。
1つのRCTのサブグループ解析の結果であることや有害事象の増加を加味すると,患者の希望はばらつきがあると判断した。
三次治療以降にエキセメスタンと併用した場合のエベロリムスの医療コストについて,日本の患者負担分を想定した費用対効果分析はなされていない。高額療養費制度の適用となる薬剤費と想定される。以上より,費用負担が患者の希望に影響する可能性がある。
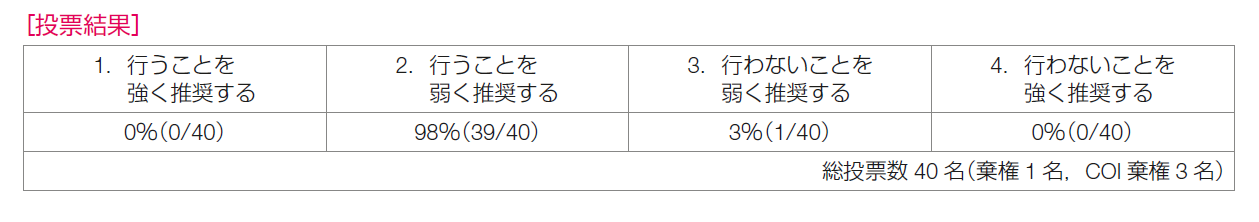
推奨決定会議の投票では,「行うことを弱く推奨する」が98%,「行わないことを弱く推奨する」が3%であった。
以上より,エビデンスの強さ,益と害のバランス,患者希望などを勘案し,推奨は「非ステロイド性アロマターゼ阻害薬耐性の場合,エキセメスタン+エベロリムス併用療法を行うことを弱く推奨する」とした。
2)未使用の内分泌療法薬,分子標的治療薬について
PALOMA-3試験では,三次治療以降の症例が35%登録されており,サブグループ解析では,PFS,OSとも全体集団と同様の傾向であった(☞薬物CQ21参照)7)~9)。サイクリン依存性キナーゼ(CDK)4/6阻害薬未使用の場合は,内分泌療法薬にCDK4/6阻害薬を併用することを検討する。1つのRCTのサブグループ解析であり,エビデンスの強さは「弱」とした。
三次治療以降において,内分泌療法薬単剤で,Best Supportive Care,化学療法と比較して有意に予後が改善した治療は存在しない。また,CDK4/6阻害薬やエベロリムスに抵抗性となった後の内分泌療法薬単剤の治療効果は検討されていない。
タモキシフェン治療後の二次治療以降の症例において第三世代AI(アナストロゾール,レトロゾール,エキセメスタン)とプロゲステロン製剤(酢酸メゲステロール,酢酸メドロキシプロゲステロン)を比較したメタアナリシスでは,第三世代AIがOSを延長したが(HR 0.86,95%CI 0.79-0.94),三次治療以降の症例は少数のみであった10)。
非ステロイド性AI既治療例を対象としたRCTであるEFECT試験では,エキセメスタンとフルベストラント250 mgが比較され,全体集団では無増悪期間(TTP),ORR,CBRに有意差を認めず(☞薬物CQ21参照),サブグループ解析の三次治療以降の症例においてもTTPは同様の傾向であった11)。
非ステロイド性AI既治療例を対象としてエキセメスタンとトレミフェン120 mgを比較したRCTでは,エキセメスタン群の71%,トレミフェン群の74%が三次治療以降の症例であった12)。全体集団の解析では,主要評価項目であるCBR,および副次評価項目であるORR,OSは有意差を認めなかったが,PFSはトレミフェン群で良好であった(HR 0.61,95%CI 0.38-0.99,p=0.0045)。サブグループ解析の三次治療以降の症例においても,CBRは同様の傾向であった。
エストロゲン療法については,一次内分泌療法143例を対象としたRCTでジエチルスチルベストロール(diethylstilbestrol;DES)とタモキシフェンのORRに有意差は認めなかったが(41% vs 33%,p=0.37),追跡報告ではDES群のOS中央値が良好であった(3.0年vs 2.4年,p=0.034)。しかしながら,DES群は有害事象が多く,12%が有害事象のために治療を中止した13)14)。また,AI既治療例66例を対象に高用量(30 mg)と低用量(6 mg)エストラジオールを比較したRCTでは,主要評価項目のCBRに差は認めず(28% vs 29%),Grade 3以上の有害事象は低用量群で有意に少なかった(34% vs 18%,p=0.03)15)。
以上より,内分泌療法薬単剤のRCTは複数あるものの,三次治療以降のデータは乏しく,エビデンスの強さは「非常に弱い」とした。
各薬剤の優先順位を決定することは困難であり,前治療薬の作用機序を考慮して,未使用の内分泌療法薬(フルベストラント,アロマターゼ阻害薬,トレミフェン,タモキシフェン)を選択することが妥当である。酢酸メドロキシプロゲステロンは血栓症や体重増加,エストラジオールは血栓症や腟出血などの有害事象の面から後期ラインで使用する。
CDK4/6阻害薬は一次治療あるいは二次治療までに使用することが強く推奨され,分子標的治療薬使用後の内分泌療法薬単剤の有効性は不確定であるため,推奨は記載しなかった。
検索キーワード・参考にした二次資料
PubMedで,“Breast Neoplasms”,“Antineoplastic Agents, Hormonal”,“Estrogen Antagonists”,“Gonadotropin-Releasing Hormone”,“Aromatase Inhibitors”,“Receptor, ErbB-2”,“Cyclin-Dependent Kinases”,“Protein Kinase Inhibitors”,“Everolimus”,“Receptors, Estrogen”のキーワードと,“Postmenopause”の同義語で検索した。医中誌・Cochrane Libraryも同等のキーワードで検索した。検索期間は2016年11月までとし,1,334件がヒットした。
さらに2021年3月までの期間で追加検索を行った。PubMedで,“Breast Neoplasms”,“Advanced”,“Antineoplastic Agents, Hormonal”,“Cyclin-Dependent Kinases”の同義語,“P13K Inhibitors”の同義語のキーワードで検索し,医中誌・Cochrane Libraryも同等のキーワードで検索した。743件がヒットし,ハンドサーチで3件の文献を追加した。
参考文献
1)Cardoso F, Paluch-Shimon S, Senkus E, Curigliano G, Aapro MS, André F, et al. 5th ESO-ESMO international consensus guidelines for advanced breast cancer(ABC 5). Ann Oncol. 2020;31(12):1623-49. [PMID:32979513]
2)Hortobagyi GN. Treatment of breast cancer. N Engl J Med. 1998;339(14):974-84. [PMID:9753714]
3)Baselga J, Campone M, Piccart M, Burris HA 3rd, Rugo HS, Sahmoud T, et al. Everolimus in postmenopausal hormone-receptor-positive advanced breast cancer. N Engl J Med. 2012;366(6):520-9. [PMID:22149876]
4)Yardley DA, Noguchi S, Pritchard KI, Burris HA 3rd, Baselga J, Gnant M, et al. Everolimus plus exemestane in postmenopausal patients with HR(+)breast cancer:BOLERO-2 final progression-free survival analysis. Adv Ther. 2013;30(10):870-84. [PMID:24158787]
5)Piccart M, Hortobagyi GN, Campone M, Pritchard KI, Lebrun F, Ito Y, et al. Everolimus plus exemestane for hormone-receptor-positive, human epidermal growth factor receptor-2-negative advanced breast cancer:overall survival results from BOLERO-2. Ann Oncol. 2014;25(12):2357-62. [PMID:25231953]
6)Burris HA 3rd, Lebrun F, Rugo HS, Beck JT, Piccart M, Neven P, et al. Health-related quality of life of patients with advanced breast cancer treated with everolimus plus exemestane versus placebo plus exemestane in the phase 3, randomized, controlled, BOLERO-2 trial. Cancer. 2013;119(10):1908-15. [PMID:23504821]
7)Turner NC, Ro J, André F, Loi S, Verma S, Iwata H, et al;PALOMA3 Study Group. Palbociclib in hormone-receptor-positive advanced breast cancer. N Engl J Med. 2015;373(3):209-19. [PMID:26030518]
8)Cristofanilli M, Turner NC, Bondarenko I, Ro J, Im SA, Masuda N, et al. Fulvestrant plus palbociclib versus fulvestrant plus placebo for treatment of hormone-receptor-positive, HER2-negative metastatic breast cancer that progressed on previous endocrine therapy(PALOMA-3):final analysis of the multicentre, double-blind, phase 3 randomised controlled trial. Lancet Oncol. 2016;17(4):425-39. [PMID:26947331]
9)Turner NC, Slamon DJ, Ro J, Bondarenko I, Im SA, Masuda N, et al. Overall survival with palbociclib and fulvestrant in advanced breast cancer. N Engl J Med. 2018;379(20):1926-36. [PMID:30345905]
10)Mauri D, Pavlidis N, Polyzos NP, Ioannidis JP. Survival with aromatase inhibitors and inactivators versus standard hormonal therapy in advanced breast cancer:meta-analysis. J Natl Cancer Inst. 2006;98(18):1285-91. [PMID:16985247]
11)Chia S, Gradishar W, Mauriac L, Bines J, Amant F, Federico M, et al. Double-blind, randomized placebo controlled trial of fulvestrant compared with exemestane after prior nonsteroidal aromatase inhibitor therapy in postmenopausal women with hormone receptor-positive, advanced breast cancer:results from EFECT. J Clin Oncol. 2008;26(10):1664-70. [PMID:18316794]
12)Yamamoto Y, Ishikawa T, Hozumi Y, Ikeda M, Iwata H, Yamashita H, et al. Randomized controlled trial of toremifene 120 mg compared with exemestane 25 mg after prior treatment with a non-steroidal aromatase inhibitor in postmenopausal women with hormone receptor-positive metastatic breast cancer. BMC Cancer. 2013;13:239. [PMID:23679192]
13)Ingle JN, Ahmann DL, Green SJ, Edmonson JH, Bisel HF, Kvols LK, et al. Randomized clinical trial of diethylstilbestrol versus tamoxifen in postmenopausal women with advanced breast cancer. N Engl J Med. 1981;304(1):16-21. [PMID:7001242]
14)Peethambaram PP, Ingle JN, Suman VJ, Hartmann LC, Loprinzi CL. Randomized trial of diethylstilbestrol vs. tamoxifen in postmenopausal women with metastatic breast cancer. An updated analysis. Breast Cancer Res Treat. 1999;54(2):117-22. [PMID:10424402] 15)Ellis MJ, Gao F, Dehdashti F, Jeffe DB, Marcom PK, Carey LA, et al. Lower-dose vs high-dose oral estradiol therapy of hormone receptor-positive, aromatase inhibitor-resistant advanced breast cancer:a phase 2 randomized study. JAMA. 2009;302(7):774-80. [PMID:19690310]