CQ18 閉経前ホルモン受容体陽性HER2陰性転移・再発乳癌に対する一次内分泌療法として,何が推奨されるか?
背 景・目 的
閉経前ホルモン受容体陽性HER2陰性転移・再発乳癌に対して,生命に差し迫った状況でない場合には,卵巣機能抑制を行い,内分泌療法(分子標的薬を含む)を考慮すべきである。前治療の有無,術後薬物療法終了からの期間等を考慮し,一次治療の手段としてどのような治療が推奨されるか検証した。一次内分泌療法の定義については,治療編 総説V.4.a.a-1.1)を参照のこと。なお,卵巣機能抑制方法は一般的にLH-RHアゴニストが用いられているが,他に手術療法などの選択肢もあるため,それぞれの合併症や治療期間,コストなどを患者と話し合って決めるべきである。
解 説
1)卵巣機能抑制を行い,CDK4/6阻害薬と非ステロイド性アロマターゼ阻害薬の併用療法(添付文書上は保険適用外)を行うことについて
閉経前ホルモン受容体陽性HER2陰性転移・再発乳癌患者における一次内分泌療法でのCDK4/6阻害薬の有効性を検証した試験はMONALEESA-7試験のみである。タモキシフェン,レトロゾールもしくはアナストロゾールのいずれか一剤とゴセレリンの併用に対して,CDK4/6阻害薬であるribociclib(未承認)上乗せの有効性が検証され,ribociclib併用群で無増悪生存期間(PFS)の有意な延長と(ribociclib群:23.8カ月,プラセボ群:13.0カ月,ハザード比(HR)0.55,95%CI 0.44-0.69,p<0.0001)1),全生存期間(OS)の有意な延長が示されている(ribociclib群:not reached,プラセボ群:40.9カ月,HR 0.71,95%CI 0.54-0.95,p<0.00973)2)。その後のプロトコール規定外のOS解析(観察期間中央値53.5カ月)で、ribociclib群:58.7カ月,プラセボ群:48.0カ月,HR 0.76,95%CI 0.61-0.96と報告された3)。さらに,患者報告によるQOLの評価(EORTC QLQ-C30,global HRQOL)では,10%以上の低下が起こるまでの期間がribociclib群で有意に長かった(HR 0.67,95%CI 0.52-0.86)4)。Ribociclibの副作用にQTcの延長があるが,本試験ではタモキシフェンとの併用時に,より高い発生率であることが報告された〔QTcの60 ms以上の延長:タモキシフェン併用時16%,非ステロイド性アロマターゼ阻害薬(NSAI)併用時7%〕。FDAやEMAにおけるribociclibの承認においては,ribociclibとの併用内分泌療法としてタモキシフェンは認められておらず,閉経前患者でのribociclib使用時はNSAI+LH-RHアゴニストとの併用となる。
前述のように,閉経前の一次内分泌療法においてCDK4/6阻害薬(ribociclib)は生存期間の改善を含めた有効性が示されているが,わが国で承認済のパルボシクリブとアベマシクリブに関しては,閉経前一次内分泌療法での臨床試験が欠如しており明確なエビデンスはない。しかし,ホルモン受容体陽性HER2陰性転移・再発乳癌に対するCDK4/6阻害薬の臨床試験における有効性は,閉経後一次内分泌療法,閉経前,閉経後二次内分泌療法を対象とした第Ⅲ相比較試験において,OSについては臨床試験ごとに結果が異なるものの,PFSについてはパルボシクリブ,アベマシクリブ,ribociclibの3剤に共通して一貫した延長効果が示されている。これらのエビデンスから,閉経前一次内分泌療法だけが「臨床試験の欠如」を原因として治療適応から外れる状況は該当患者にとって不利益が大きいと考えられた。本ガイドラインでは,閉経前一次内分泌療法においてもCDK4/6阻害薬の併用を推奨する。なお,CDK4/6阻害薬と併用する内分泌療法は,MONALEESA-7の有効性,安全性の結果からNSAI+LH-RHアゴニストが推奨される。
CDK4/6阻害薬の併用による有害事象の増加があり(☞薬物CQ19,20,21参照),患者の希望にはばらつきが予想される。高額療養費制度を考慮した医療費の自己負担の差は,他の治療選択肢と比較し限定的である。
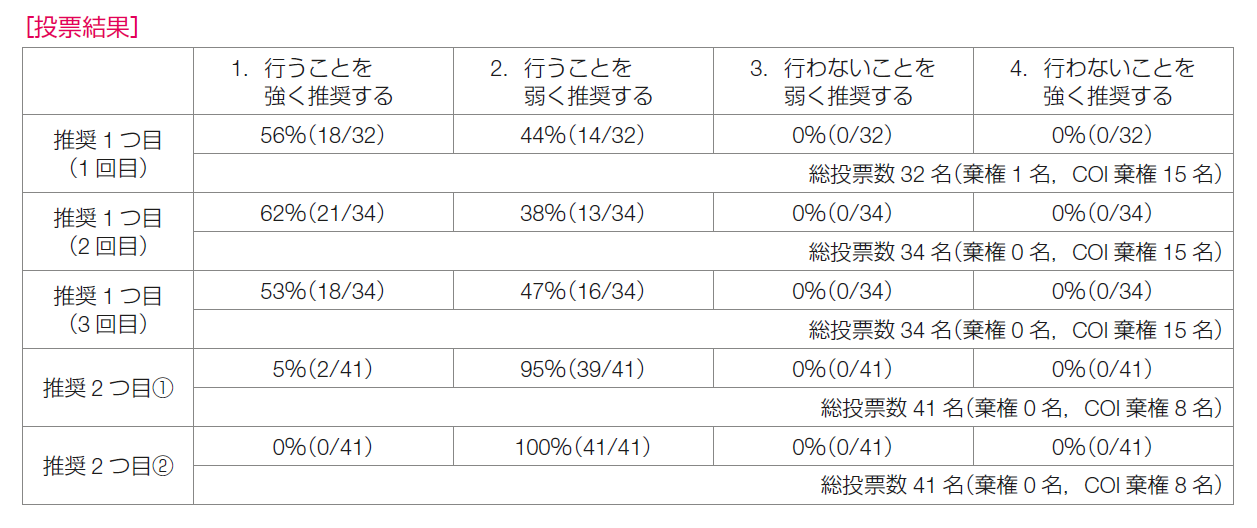
推奨決定会議では,1回目の投票で,CDK4/6阻害薬の併用を「行うことを強く推奨する」が56%,「行うことを弱く推奨する」が44%であり,決定基準の70%合意に達しなかった。その後,2回目は62%と38%,3回目は53%と47%の結果であり,推奨の強さは決定できなかった。
一次内分泌療法と二次内分泌療法でのCDK4/6阻害薬併用の有用性を比較したSONIA試験については薬物CQ20参照のこと。
2)卵巣機能抑制を行い,内分泌療法(単独)を行うことについて
現在,内分泌療法単独治療がより推奨される患者群を識別するバイオマーカーはなく,閉経前一次内分泌療法においてもCDK4/6阻害薬の併用は選択肢として患者に提示されるべきである。しかし,合併症や患者の希望などによっては,内分泌療法単独が推奨される。
(1)卵巣機能抑制とタモキシフェンの併用療法を行うことについて
閉経前ホルモン受容体陽性HER2陰性転移・再発乳癌に対する一次内分泌療法として,タモキシフェン,卵巣機能抑制,およびその両者併用の治療法を比較した小規模のランダム化比較試験やそれらのメタアナリシスが行われている。
タモキシフェンと卵巣機能抑制を比較した4試験のランダム化比較試験のメタアナリシス(n=220)では,両群の効果に関して有意な差を認めなかった5)。
LH-RHアゴニスト単独,タモキシフェン単独およびその併用とのランダム化比較試験(n=161)において,併用群が各単独投与に比べ生存期間の有意な延長を示した(生存期間中央値:LH-RHアゴニスト単独2.5年,タモキシフェン単独2.9年,併用群3.7年,p=0.01)。併用群に対する各単独群の死亡HRは,LH-RHアゴニスト単独群HR 1.95,95%CI 1.23-3.10,タモキシフェン単独群HR 1.63,95%CI 1.03-2.59であった6)。同試験からの副作用報告では,LH-RHアゴニスト単独,もしくは併用群で,タモキシフェン単独と比べ,ホットフラッシュの増加(全Grade)が報告されているが,Grade 3~4の有害事象増加の報告はない。
LH-RHアゴニストとタモキシフェンの併用とLH-RHアゴニスト単独を比較した4試験のランダム化比較試験のメタアナリシス(n=506)では,併用群において生存期間の延長を認めた(生存期間中央値:単独群:2.5年,併用群:2.9年,HR 0.78,95%CI 0.63-0.96,p=0.02)7)。メタアナリシスでは有害事象は検討されなかったが,解析に含まれたうち最大の試験(n=318)からは,ホットフラッシュなど有害事象に関する差は報告されていない8)。
これらの試験の結果より,ホットフラッシュが増加する可能性はあるものの,生存期間の延長が得られることから,LH-RHアゴニスト単独もしくはタモキシフェン単独と比較し,卵巣機能抑制とタモキシフェン併用による益は害に勝ると考えられる。
LH-RHアゴニストとタモキシフェンの有効性は示されているが,CDK4/6阻害薬という,より有効性の高い治療選択が登場しており,患者の希望にはばらつきがあると考えられる。
推奨決定会議での投票では,「行うことを強く推奨する」が5%,「行うことを弱く推奨する」が95%であった。
以上より,エビデンスの程度,益と害のバランス,患者の希望,またCDK4/6阻害薬併用の選択肢を考慮し,推奨は,「卵巣機能抑制とタモキシフェンの併用療法を行うことを弱く推奨する」とした。
(2)卵巣機能抑制と非ステロイド性アロマターゼ阻害薬の併用療法を行うことについて
LH-RHアゴニストとNSAIの併用療法は,わが国においても実臨床で使用されている治療選択肢の一つである。しかしながら,同治療法の有効性を検証したランダム化比較試験はなく,これまでの報告は少数例の単群試験のみである。
以下,ホルモン受容体陽性HER2陰性転移・再発乳癌の一次内分泌療法として,NSAIとゴセレリンの併用を検討した試験に関して記載する。Carlsonらは,一次内分泌療法としてアナストロゾールとゴセレリンの併用療法について前向き第Ⅱ相の単アーム試験(n=35)を実施し,奏効率(ORR)37.5%(95%CI 21-56%),クリニカルベネフィット率(CBR)71.9%(95%CI 53-86%),進行までの期間(TTP)8.3カ月(2.1~63カ月)と報告した9)。Parkらによる,一次内分泌療法患者を対象とした非ランダム化第Ⅱ相試験では,閉経前患者(35人)におけるレトロゾール+LH-RHアゴニストと閉経後患者(38人)におけるレトロゾールの有効性が検討された10)。ORRは閉経前46% vs閉経後27%,p=0.09,CBRは閉経前77% vs閉経後74%(p=0.77),TTPは閉経前9.5カ月vs閉経後8.9カ月であり,両群間に差は認められなかった。Liuらは,35歳以下の患者35人に対して,一次内分泌療法におけるレトロゾールとゴセレリンの併用を検討し,ORR 25.7%,CBR 65.7%,PFSは9.6カ月と報告した11)。これら試験において,NSAIとLH-RHアゴニストと併用による重篤な毒性は報告されていないが,骨密度の有意な低下が報告されている。
なお,現在参考となり得る最大のデータは,MONALEESA-7試験のコントロールアームにおけるLH-RHアゴニスト+NSAI群の治療成績である。同試験からは併用内分泌療法別のサブグループ解析が報告されている。コントロールアームのうち,LH-RHアゴニスト+タモキシフェン群(n=90)はPFS 11カ月(9.1~16.4カ月),LH-RHアゴニスト+NSAI群(n=247)は13.8カ月(12.6~17.4)と報告され,閉経後一次内分泌療法の諸試験におけるNSAI単剤のPFSと類似の結果であった。
エビデンスは少なく,LH-RHアゴニストとタモキシフェンの併用よりも優先される治療ではないが,一定の有効性が示されていること,すでに実臨床で広く使用されている状況を鑑み,LH-RHアゴニスト+NSAIは閉経前一次内分泌療法の治療選択となり得る,とした。有害事象の増加は小さく,LH-RHアゴニスト+タモキシフェンと比較し,コスト負担の増加も限定的であるが,CDK4/6阻害薬併用という選択肢もあり,患者の希望はばらつくものと考える。
推奨決定会議での投票では,「行うことを弱く推奨する」が100%で一致した。
以上より,推奨は,閉経前一次内分泌療法として「卵巣機能抑制と非ステロイド性アロマターゼ阻害薬の併用療法を行うことを弱く推奨する」とした。
なお,術後内分泌療法中,もしくは終了後12カ月以内に再発した患者に対する一次内分泌療法に関しては,過去の多くの試験において二次内分泌療法の患者とともに治療効果を評価されている。このため原則として薬物CQ19の推奨に準ずることとする(☞治療編 総説.Ⅴ.4.a.a-1.参照)。
検索キーワード・参考にした二次資料
薬物CQ18~22の共通の検索として,PubMedで,“Breast Neoplasms”,“Neoplasm Metastasis”,“Neoplasm Recurrence, Local”,“Endocrine therapy”,“tamoxifen”,“toremifene”,“Fulvestrant”,“Aromatase Inhibitor”,“CDK4/6 inhibitor”,“everolimus”,“Buparlisib”,“pictilisib”,“alpelisib”,“AKT inhibitor”のキーワードとその同義語で検索した。医中誌・Cochrane Libraryも同等のキーワードで検索した。検索期間は2016年1月~2021年3月とし,共通の検索結果として1,370件がヒットした。LH-RHアゴニスト+AI,また新たなガイドラインなどに関してはハンドサーチを行った。一次,二次スクリーニングを行い,MONALEESA-7のQOL報告,またLH-RHアゴニスト+AIに関する2編などを新たに採用した。
参考文献
1)Tripathy D, Im SA, Colleoni M, Franke F, Bardia A, Harbeck N, et al. Ribociclib plus endocrine therapy for premenopausal women with hormone-receptor-positive, advanced breast cancer(MONALEESA-7):a randomised phase 3 trial. Lancet Oncol. 2018;19(7):904-15. [PMID:29804902]
2)Im SA, Lu YS, Bardia A, Harbeck N, Colleoni M, Franke F, et al. Overall survival with ribociclib plus endocrine therapy in breast cancer. N Engl J Med. 2019;381(4):307-16. [PMID:31166679]
3)Lu YS, Im SA, Colleoni M, Franke F, Bardia A, Cardoso F, et al.. Updated Overall Survival of Ribociclib plus Endocrine Therapy versus Endocrine Therapy Alone in Pre- and Perimenopausal Patients with HR+/HER2- Advanced Breast Cancer in MONALEESA-7: A Phase III Randomized Clinical Trial. Clin Cancer Res. 2022 Mar 1;28(5):851-859. [PMID: 34965945]
4)Harbeck N, Franke F, Villanueva-Vazquez R, Lu YS, Tripathy D, Chow L, et al. Health-related quality of life in premenopausal women with hormone-receptor-positive, HER2-negative advanced breast cancer treated with ribociclib plus endocrine therapy:results from a phase Ⅲ randomized clinical trial(MONALEESA-7). Ther Adv Med Oncol. 2020;12:1758835920943065. [PMID:32782490]
5)Crump M, Sawka CA, DeBoer G, Buchanan RB, Ingle JN, Forbes J, et al. An individual patient-based meta-analysis of tamoxifen versus ovarian ablation as first line endocrine therapy for premenopausal women with metastatic breast cancer. Breast Cancer Res Treat. 1997;44(3):201-10. [PMID:9266099]
6)Klijn JG, Beex LV, Mauriac L, van Zijl JA, Veyret C, Wildiers J, et al. Combined treatment with buserelin and tamoxifen in premenopausal metastatic breast cancer:a randomized study. J Natl Cancer Inst. 2000;92(11):903-11. [PMID:10841825]
7)Klijn JG, Blamey RW, Boccardo F, Tominaga T, Duchateau L, Sylvester R;Combined Hormone Agents Trialists’ Group and the European Organization for Research and Treatment of Cancer. Combined tamoxifen and luteinizing hormone-releasing hormone(LHRH)agonist versus LHRH agonist alone in premenopausal advanced breast cancer:a meta-analysis of four randomized trials. J Clin Oncol. 2001;19(2):343-53. [PMID:11208825]
8)Jonat W, Kaufmann M, Blamey RW, Howell A, Collins JP, Coates A, et al. A randomised study to compare the effect of the luteinising hormone releasing hormone(LHRH)analogue goserelin with or without tamoxifen in pre- and perimenopausal patients with advanced breast cancer. Eur J Cancer. 1995;31A(2):137-42. [PMID:7718316]
9)Carlson RW, Theriault R, Schurman CM, Rivera E, Chung CT, Phan SC, et al. Phase Ⅱ trial of anastrozole plus goserelin in the treatment of hormone receptor-positive, metastatic carcinoma of the breast in premenopausal women. J Clin Oncol. 2010;28(25):3917-21. [PMID:20679610]
10)Park IH, Ro J, Lee KS, Kim EA, Kwon Y, Nam BH, et al. Phase Ⅱ parallel group study showing comparable efficacy between premenopausal metastatic breast cancer patients treated with letrozole plus goserelin and postmenopausal patients treated with letrozole alone as first-line hormone therapy. J Clin Oncol. 2010;28(16):2705-11. [PMID:20421538]
11)Liu X, Qu H, Cao W, Wang Y, Ma Z, Li F, et al. Efficacy of combined therapy of goserelin and letrozole on very young women with advanced breast cancer as first-line endocrine therapy. Endocr J. 2013;60(6):819-28. [PMID:23714650]