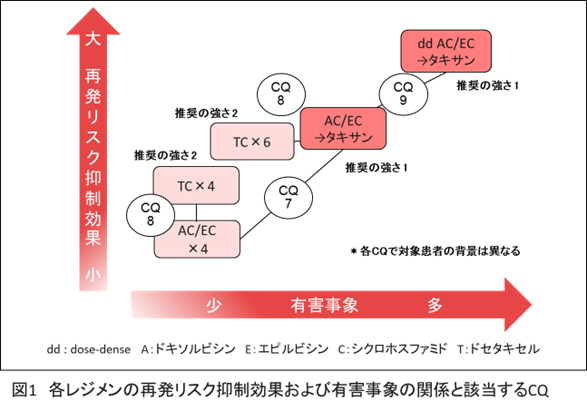
CQ9 化学療法を行う早期乳癌に対して,dose-dense化学療法は勧められるか?
背 景・目 的
Norton—Simonの仮説1)に基づき化学療法の投与間隔を短縮したdose-dense化学療法が,周術期化学療法において有用であるか検討した。
解 説
周術期dose-dense化学療法に関する比較試験は複数報告されている。Dose-dense化学療法は,広義には,G-CSFの併用なしに薬剤量を減らし,投与間隔を短縮したものも含まれるが,狭義には,薬剤の種類や投与量が同じでG-CSF併用で投与間隔を短くした方法である。本CQにおいては,化学療法の投与期間短縮の有用性を適切に評価することを目的に,対照群と介入群で同じ薬剤が同量投与されているランダム化比較試験(RCT)を用いてシステマチックレビュー行った。
該当した5つのRCTのうち4件は術後化学療法2)~7),1件は術前および術後化学療法8)を対象とした試験であった。化学療法は,2つの試験ではアンスラサイクリン系薬剤とタキサン系薬剤の両方がdose-denseであり4)~6),2つの試験でアンスラサイクリン系薬剤とタキサン系以外のレジメンが順次投与されており7)8),1つは両方のレジメンがdose-denseとされ8),1つはアンスラサイクリン系薬剤を含むレジメンのみがdose-denseとされていた8)。残る1つの試験ではアンスラサイクリン系薬剤を含むレジメンのdose-denseが用いられていた2)3)。
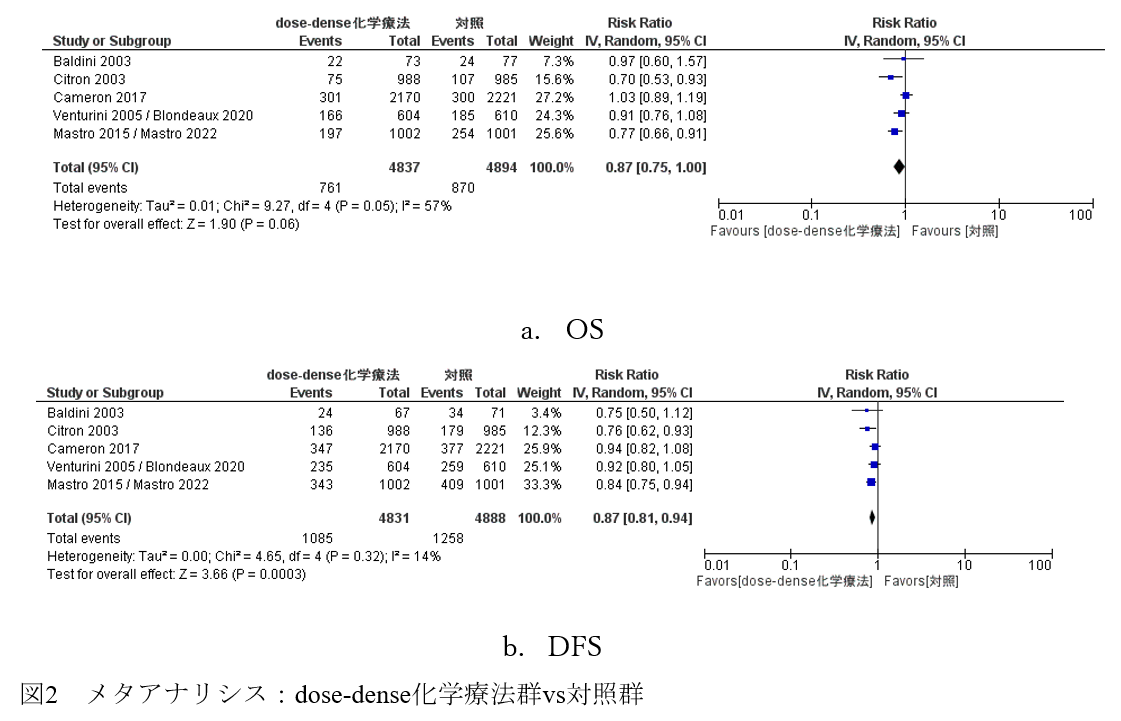
全生存期間(OS)は5件のRCTから9,731人を対象とし解析を行い,イベントの割合はdose-dense群が15.7%で対照群が17.8%であり,リスク比(RR)0.87(95%CI 0.75-1.00)と統計学的有意差は認めていないが,dose-denseによって改善する傾向を認めた(図2a)。無病生存期間(DFS)は,同じく5件のRCTから9,719人を対象として解析を行い,イベントの割合はdose-dense群が22.5%で対照群が25.7%であり,RR 0.87(95%CI 0.81-0.94)と統計学的に有意な改善が示された(図2b)。
QOLについて術前化学療法でdose-dense化学療法を行った1つのRCTにおいて評価されている7)。EORTC QLQ-C30 GHS/QOLの10ポイント以上の低下をイベントとした。QOLの低下は,アンスラサイクリン系抗がん剤治療終了時点には対照群で57.4%,dose-dense群で67.0%と、dose-dense群に多く認められた(p=0.00012)が,治療開始後24カ月までの期間通した解析においては有意差を認めなかった(p=0.96)。
その他の害に関するアウトカムとして,有害事象は対象としたRCTごとに報告されている内訳が異なっていた。貧血は2件のRCTから4,172人を対象に解析した5)~7)。全Gradeでは対照群で37.1%、dose-dense群で53.4%と増加していた(risk difference(RD) 0.17,95%CI 0.14-0.20)。しかし,G3以上の貧血に限定すると,対照群で0.09%,dose-dense群で0.7%と有意な増加は認めなかった(RD 0.01,95%CI -0.01-0.02)。発熱性好中球減少症の評価は1件のRCT,2,155人を対象とした7)。発熱性好中球減少症は,対照群で3.6%,dose-dense群で1.4%とdose-dense化学療法群でリスクが低下することが示された(RD -0.02,95%CI -0.03--0.01)。Dose-dense化学療法でG-CSFの一次予防が必須とされていたためと考えられた。Grade 3以上の悪心・嘔吐の頻度は2件のRCTから4,172人を対象に評価し,対照群で4.6%,dose-dense群で5.5%と有意な増加は認めなかった(RD 0.01,95%CI -0.01-0.02)5)~7)。
益としては,DFSの一貫した有意な延長とOS延長の傾向が,高いエビデンスの確実性をもって認められている。一方,害としては,QOL低下の可能性はあるがエビデンスの確実性が低く,貧血の増加があるものの重篤な貧血の頻度は少ない。このことから益と害のバランスは益が害を上回ると考えられる。エビデンスの強さは,複数の適切に管理されたRCTがあるので「強」とした。患者希望については,貧血が増加することやペグフィルグラスチム併用が必須となることを考えると必ずしも一貫するとはいえないが,予後改善の益から多くの場合でdose-dense化学療法が希望されると判断した。
適応に関する検討事項として,本CQで採用した5つのRCTでは再発リスクが低い症例は除外されている。またGIM2試験の探索的解析として,ホルモン受容体陽性かつKi67低値の場合はdose-dense化学療法の予後改善効果が乏しいことが報告されている9)。以上から再発リスクが低い場合やいわゆるluminal A-likeのサブタイプの場合はdose-dense化学療法の適応を特に慎重に検討する必要がある。
推奨決定会議の投票の結果は,「行うことを強く推奨する 66/77,合意率 86%」,「行うことを弱く推奨する 10/77」,「行わないことを弱く推奨する 1/77」であり,推奨は「再発リスクが高い場合は,dose-dense化学療法を行うことを強く推奨する」とした。

検索キーワード・参考にした二次資料
PubMed・医中誌・Cochrane Libraryで,#1(breast neoplasms)or(breast cancer*),#2(dose dense)をキーワードとして検索を行った。検索期間は2021年6月4日までとした。
その結果,430編の論文が抽出された。一次・二次スクリーニングを行ったところ,2件のシステマティック・レビューを含む6編の論文が残った。2つのシステマティック・レビューのうち1編が本CQと合致し,AMSTAR基準を満たしており,採用した。そこで,同研究で用いられている5編のRCTを利用した10)。 Web改訂版作成のため追加で2023年1月までの期間ハンドサーチを行い,新たに2編を追加した。
参考文献
1)Norton L, Simon R. Tumor size, sensitivity to therapy, and design of treatment schedules. Cancer Treat Rep. 1977;61(7):1307-17. [PMID:589597]
2)Venturini M, Del Mastro L, Aitini E, Baldini E, Caroti C, Contu A, et al. Dose-dense adjuvant chemotherapy in early breast cancer patients:results from a randomized trial. J Natl Cancer Inst. 2005;97(23):1724-33. [PMID:16333028]
3)Blondeaux E, Lambertini M, Michelotti A, Conte B, Benasso M, Dellepiane C, et al. Dose-dense adjuvant chemotherapy in early breast cancer patients: 15-year results of the Phase 3 Mammella InterGruppo (MIG)-1 study. Br J Cancer. 2020 ;122(11):1611-17. [PMID:32231293]
4)Citron ML, Berry DA, Cirrincione C, Hudis C, Winer EP, Gradishar WJ, et al. Randomized trial of dose-dense versus conventionally scheduled and sequential versus concurrent combination chemotherapy as postoperative adjuvant treatment of node-positive primary breast cancer:first report of Intergroup Trial C9741/Cancer and Leukemia Group B Trial 9741. J Clin Oncol. 2003;21(8):1431-9. [PMID:12668651]
5)Del Mastro L, De Placido S, Bruzzi P, De Laurentiis M, Boni C, Cavazzini G, et al;Gruppo Italiano Mammella(GIM)investigators. Fluorouracil and dose-dense chemotherapy in adjuvant treatment of patients with early-stage breast cancer:an open-label, 2×2 factorial, randomised phase 3 trial. Lancet. 2015;385(9980):1863-72. [PMID:25740286]
6)Mastro L, Poggio F, Blondeaux E, Placido S, Giuliano M, Forestieri V, et al;Fluorouracil and dose-dense adjuvant chemotherapy in patients with early-stage breast cancer (GIM2): end-of-study results from a randomised, phase 3 trial. Lancet Oncol. 2022 ;23(12):1571-82. [PMID:36370716]
7)Cameron D, Morden JP, Canney P, Velikova G, Coleman R, Bartlett J, et al;TACT2 Investigators. Accelerated versus standard epirubicin followed by cyclophosphamide, methotrexate, and fluorouracil or capecitabine as adjuvant therapy for breast cancer in the randomised UK TACT2 trial(CRUK/05/19):a multicentre, phase 3, open-label, randomised, controlled trial. Lancet Oncol. 2017;18(7):929-45. [PMID:28600210]
8)Baldini E, Gardin G, Giannessi PG, Evangelista G, Roncella M, Prochilo T, et al. Accelerated versus standard cyclophosphamide, epirubicin and 5-fluorouracil or cyclophosphamide, methotrexate and 5-fluorouracil:a randomized phase Ⅲ trial in locally advanced breast cancer. Ann Oncol. 2003;14(2):227-32. [PMID:12562649]
9)Conte B, Bruzzone M, Lambertini M, Poggio F, Bighin C, Blondeaux E, et al;GIM2 Investigators. Effect of dose-dense adjuvant chemotherapy in hormone receptor positive/HER2-negative early breast cancer patients according to immunohistochemically defined luminal subtype:an exploratory analysis of the GIM2 trial. Eur J Cancer. 2020;136:43-51. [PMID:32634760]
10)Zhou W, Chen S, Xu F, Zeng X. Survival benefit of pure dose-dense chemotherapy in breast cancer:a meta-analysis of randomized controlled trials. World J Surg Oncol. 2018;16(1):144. [PMID:30007402]