CQ29 HER2陽性・ホルモン受容体陽性転移・再発乳癌に対して内分泌療法単独や抗HER2療法と内分泌療法併用は勧められるか?
背 景・目 的
HER2陽性かつホルモン受容体陽性転移・再発乳癌において,脱毛など化学療法の有害事象を許容できない患者や,全身状態が悪い患者において内分泌療法は選択肢の一つである。本CQでは,HER2陽性かつホルモン受容体陽性転移・再発乳癌に対する内分泌療法単独と抗HER2療法と内分泌療法併用の効果・安全性について検証した。
解 説
内分泌療法単独 vs 抗HER2療法+内分泌療法併用
HER2陽性・ホルモン受容体陽性転移・再発乳癌(閉経後)に対する一次治療として,内分泌療法単独 vs 抗HER2療法(トラスツズマブ,もしくはラパチニブ)と内分泌療法併用の比較試験が,本CQの文献として3編抽出された(TAnDEM試験1),eLEcTRA試験2),EGF 30008試験3))。これらに対して定量的システマティック・レビューを行った結果,内分泌療法単独に対して,抗HER2療法と内分泌療法併用は無増悪生存期間(PFS)〔ハザード比(HR)0.67,95%CI 0.55-0.81〕を延長させ,奏効率(ORR)〔リスク比(RR)2.11,95%CI 1.37-3.26〕とクリニカルベネフィット率(CBR)(RR 1.50,95%CI 1.21-1.87)を改善させた。全生存期間(OS)についてはTAnDEM試験しか報告がないが,有意な差を認めていない(中央値28.5カ月vs 23.9カ月,p=0.325)。
有害事象に関しては,抗HER2療法と内分泌療法併用により,心疾患(RR 2.66,95%CI 0.66-10.76),Grade 3以上の非血液毒性(RR 1.60,95%CI 0.81-3.17)とも増加する傾向であった。特にラパチニブを併用した場合には,下痢の発生が高くなる結果(RR 5.12,95%CI 1.96-13.36)であった。QOLに関する報告はEGF 30008試験のみで,FACT-Bを用いて評価されているが4),ラパチニブ+レトロゾール群とプラセボ+レトロゾール群で,ベースラインから48週目までの変化に有意な差は認めなかった。
益としては, HER2陽性・ホルモン受容体陽性転移・再発乳癌(閉経後)に対する一次治療として,内分泌療法単独 vs 抗HER2療法と内分泌療法併用の比較試験3つの定量的システマティックレビューで, 抗HER2療法の併用によってPFS, ORR, CBRのいずれについても有意な延長が示された。しかし, 害としては, 心機能低下, 非血液毒性や下痢といった併用する抗HER2療法に伴う有害事象が増えるものの, エビデンスの確実性は低いがQOLの低下は少ないと考えられた。このことから, 益と害のバランスは, 益が害を上回ると考えられる。エビデンスの強さは, OSについてはTAnDEM試験の一報しかないため, 「中」とした。患者希望については, 有害事象の増加があるため必ずしも一貫するとは言えないが, 予後改善の益から多くの場合で抗HER2療法を希望されると判断した。
以下, 本CQのスコープからは外れるが, HER2陽性・ホルモン受容体陽性転移・再発乳癌に対する内分泌療法を考慮する上で重要な3つの試験(ALTERNATIVE試験5), PERTAIN試験6), SYSUCC-002試験7))について言及する。
Dual HER2-blockade+アロマターゼ阻害薬
Dual HER2-blockade+アロマターゼ阻害薬の試験としてALTERNATIVE試験5)とPERTAIN試験6)があるが,いずれも内分泌療法単独のコントロール群は存在せず,これらについて定性的システマティック・レビューを行った。
ALTERNATIVE試験はHER2陽性・ホルモン受容体陽性転移・再発乳癌(閉経後)に対する,ラパチニブ+トラスツズマブ+アロマターゼ阻害薬併用療法,トラスツズマブ+アロマターゼ阻害薬併用療法,ラパチニブ+アロマターゼ阻害薬併用療法の第Ⅲ相3群比較試験である。3剤併用群はトラスツズマブ+アロマターゼ阻害薬併用療法に比し,PFS(中央値11カ月vs 5.6カ月,HR 0.62,95%CI 0.45-0.88,p=0.0063)を延長した。ラパチニブ+アロマターゼ阻害薬併用療法群のPFS中央値は8.3カ月であり,トラスツズマブ+アロマターゼ阻害薬併用療法と有意な差はなかった(HR 0.85,95%CI 0.62-1.17,p=0.3159)。また,3剤併用群のORRとCBRはそれぞれ,31.7%,40%であり,PFSと同様に2剤併用群より良好な傾向であった。有害事象については3剤併用群で下痢(69%),発疹(36%),嘔気(22%)と他の2群に比べて高い傾向にあったが,重篤な有害事象は3群いずれも稀であり,有害事象による治療中止割合も低率であった。OSはimmatureなデータではあるが,3剤併用群がトラスツズマブ+アロマターゼ阻害薬併用群より延長する傾向にあった(OS中央値46.0カ月vs 40カ月,HR 0.60,95%CI 0.35-1.04)。なお,わが国では,EGF 30008試験の結果を受けてラパチニブ+アロマターゼ阻害薬併用療法は保険承認されているが,トラスツズマブを加えた3剤併用療法は承認されていない。
PERTAIN試験は,HER2陽性・ホルモン受容体陽性の転移もしくは局所進行乳癌(閉経後)に対する一次治療としてトラスツズマブ+ペルツズマブ+アロマターゼ阻害薬の3剤併用療法とトラスツズマブ+アロマターゼ阻害薬併用療法を比較したオープンラベルのランダム化第Ⅱ相試験である。ランダム化後に主治医判断で,アロマターゼ阻害薬前の導入化学療法としてドセタキセルもしくはパクリタキセルを18~24週投与することを許容している(導入化学療法の割合はペルツズマブ併用群と非併用群でそれぞれ58.1%,55%)。PFS中央値はペルツズマブ併用群で18.89カ月に対し非併用群が15.80カ月と有意に併用群で延長していた(HR 0.65,95%CI 0.48-0.89,p=0.0070)。導入化学療法の有無によるサブグループ解析では,導入化学療法ありにおいてペルツズマブ併用群vs非併用群のPFSに差はなく(中央値16.89カ月vs 16.65カ月,HR 0.75,95%CI 0.50-1.13,p=0.1633),導入化学療法なしではペルツズマブ用群のPFSが延長していた(中央値21.72カ月vs 12.45カ月,HR 0.55,95%CI 0.34-0.88,p=0.0111)。ORRは併用群63.3%,非併用群55.7%と有意差はなかった。主な有害事象としては,下痢がペルツズマブ併用群55.1%,非併用群36.3%と併用群で多かった。重篤な有害事象はペルツズマブ併用群33.1%,非併用群19.4%であり,ペルツズマブによる治療中止割合は10.2%であった。
抗HER2療法+内分泌療法併用 vs 抗HER2療法+化学療法併用
HER2陽性・ホルモン受容体陽性転移・再発乳癌(閉経後)に対する一次治療として, 抗HER2療法+内分泌療法併用 vs 抗HER2療法+化学療法併用の比較試験には, SYSUCC-002試験の1編が報告されている7)。SYSUCC-002試験は, トラスツズマブ+内分泌療法併用のトラスツズマブ+化学療法併用に対する非劣性を検証したランダム化第Ⅲ相試験である。併用する内分泌療法はアロマターゼ阻害薬, タモキシフェン, トレミフェンが, 化学療法はタキサン, カペシタビン, ビノレルビンが許容されていた。PFS中央値は, 内分泌療法併用群で19.2ヶ月に対して化学療法併用群が14.8ヶ月と非劣性が示された(HR:0.88, 95%CI:0.71-1.09)。OSについても中央値は, 内分泌療法併用群で33.9ヶ月に対して化学療法併用群が32.5ヶ月と非劣性が示された(HR:0.82, 95%CI:0.65-1.04)。有害事象は, 内分泌療法併用群に比較して化学療法併用群で血液毒性や消化器毒性を中心にGrade 3-4が多くみられた(内分泌療法群 3.1% vs 化学療法併用群 51.0%)。
HER2陽性進行・再発乳癌の一次治療に関しては,CLEOPATRA試験などの結果から,基本的にはトラスツズマブ+ペルツズマブ+タキサンが標準治療である(☞薬物CQ26参照)。メタアナリシスを行った3試験を含み, 本CQで解説した試験はいずれも現在の標準治療(トラスツズマブ+ペルツズマブ+タキサン)と比較したものではないことに留意が必要である。抗HER2療法・内分泌療法併用は脱毛をはじめとする有害事象が少ないことが大きな特徴であるが,OSやPFSについて,現在の標準治療と比べた第Ⅲ相試験の結果はないため,標準治療との比較では益が勝るとはいえないと考えられた。導入化学療法後の抗HER2療法と内分泌療法の併用による維持療法に関しては,抗HER2療法単独との比較試験がないためにその有効性については不明であるものの,PERTAIN試験の結果から害が大きく増えることはないと考える。併用する抗HER2療法についてはDual HER2-blockadeのほうがPFSを延長させる可能性があるが,OSや二次治療以降のデータは乏しく,注意が必要である。またSYSUCC-002試験より, 抗HER2療法+内分泌療法併用は, 抗HER2療法+化学療法併用に対する同等の予後および有害事象が少ないことが示されているが, 本試験もペルツズマブの併用はされておらず, 現在の標準治療と異なるため注意が必要である。
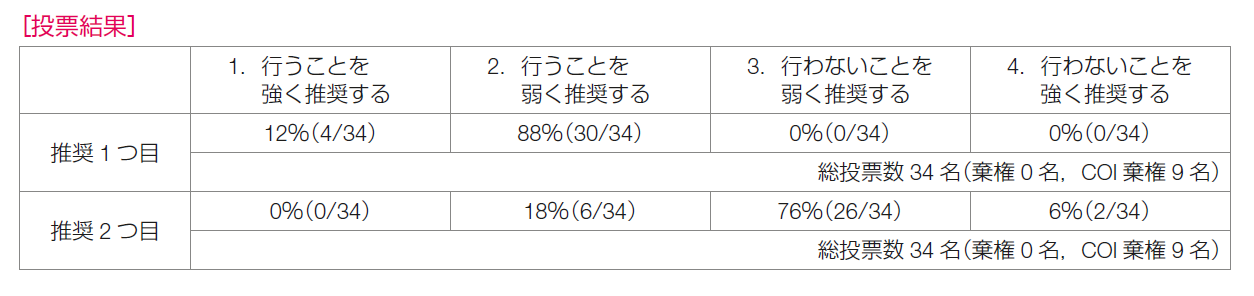
推奨決定会議での投票では,「抗HER2療法と内分泌療法併用」に関しては,「行うことを強く推奨する」が12%,「行うことを弱く推奨する」が88%であり,推奨は「化学療法の適応とならないHER2陽性・ホルモン受容体陽性転移・再発乳癌に対して,抗HER2療法と内分泌療法併用を行うことを弱く推奨する」とした。また,「内分泌療法単独」に関しては,「行うことを弱く推奨する」が18%,「行わないことを弱く推奨する」が76%,「行わないことを強く推奨する」が6%であり,推奨は「内分泌療法単独は行わないことを弱く推奨する」とした。SYSUCC-002試験に関する記載は今回のWeb改訂で追加されたため, 推奨決定会議時には考慮されていない。
検索キーワード・参考にした二次資料
PubMed,Cochraneにて,“Breast Neoplasms”,“Neoplasm Metastasis”,“Neoplasm Recurrence”,“Local”,“ErbB-2”,“Estrogen Antagonists”,“Aromatase Inhibitors”のキーワードを用いて検索した。医中誌では,“乳房腫瘍”,“進行再発”,“Erb-2”,“内分泌療法”のキーワードを用いて検索した。2018年版における文献検索期間は2016年11月までとし,1,443件がヒットした。一次スクリーニングで18編,二次スクリーニングで4編の論文が抽出された。2022年版ガイドライン改訂では,検索期間を2021年3月までとしたところ,539件が新たにヒットし, うち一次スクリーニングで11編,二次スクリーニングで4編の論文が追加抽出された。今回Web改定にあたりハンドサーチで文献検索したところ1件の論文が追加され, 解説文に記載の通り,定量的および定性的システマティック・レビューを行った。
参考文献
1)Kaufman B, Mackey JR, Clemens MR, Bapsy PP, Vaid V, Wardley A, et al. Trastuzumab plus anastrozole versus anastrozole alone for the treatment of postmenopausal women with human epidermal growth factor receptor 2-positive, hormone receptor-positive metastatic breast cancer:results from the randomized phase Ⅲ TAnDEM study. J Clin Oncol. 2009;27(33):5529-37. [PMID:19786670]
2)Huober J, Fasching PA, Barsoum M, Petruzelka L, Wallwiener D, Thomssen C, et al. Higher efficacy of letrozole in combination with trastuzumab compared to letrozole monotherapy as first-line treatment in patients with HER2-positive, hormone-receptor-positive metastatic breast cancer―results of the eLEcTRA trial. Breast. 2012;21(1):27-33. [PMID:21862331]
3)Schwartzberg LS, Franco SX, Florance A, O’Rourke L, Maltzman J, Johnston S. Lapatinib plus letrozole as first-line therapy for HER-2+hormone receptor-positive metastatic breast cancer. Oncologist. 2010;15(2):122-9. [PMID:20156908]
4)Sherrill B, Amonkar MM, Sherif B, Maltzman J, O’Rourke L, Johnston S. Quality of life in hormone receptor-positive HER-2+metastatic breast cancer patients during treatment with letrozole alone or in combination with lapatinib. Oncologist. 2010;15(9):944-53. [PMID:20798196]
5)Johnston SRD, Hegg R, Im SA, Park IH, Burdaeva O, Kurteva G, et al. Phase Ⅲ, randomized study of dual human epidermal growth factor receptor 2(HER2)blockade with lapatinib plus trastuzumab in combination with an aromatase inhibitor in postmenopausal women with HER2-positive, hormone receptor-positive metastatic breast cancer:updated results of ALTERNATIVE. J Clin Oncol. 2021;39(1):79-89. [PMID:32822287]
6)Rimawi M, Ferrero JM, de la Haba-Rodriguez J, Poole C, De Placido S, Osborne CK, et al;PERTAIN Study Group. First-line trastuzumab plus an aromatase inhibitor, with or without pertuzumab, in human epidermal growth factor receptor 2-positive and hormone receptor-positive metastatic or locally advanced breast cancer(PERTAIN):a randomized, open-label phase ⅱ trial. J Clin Oncol. 2018;36(28):2826-35. [PMID:30106636]
7) Hua X, Bi XW, Zhao JL, Shi YX, Lin Y, Wu ZY, et al;Trastuzumab Plus Endocrine Therapy or Chemotherapy as First-line Treatment for Patients with Hormone Receptor-Positive and HER2-Positive Metastatic Breast Cancer (SYSUCC-002). Clin Cancer Res. 2022;28(4):637-645. [PMID:34810217]