CQ19 閉経前ホルモン受容体陽性HER2陰性転移・再発乳癌に対する二次以降の内分泌療法として,何が推奨されるか?
背 景・目 的
ホルモン受容体陽性HER2陰性転移・再発乳癌に対する基本的な治療方針は,生命に差し迫った状況でなければ可能な限り内分泌療法を継続することである。一次内分泌療法抵抗性転移・再発乳癌の二次以降の内分泌療法として,どのような治療が推奨されるか検証した。二次内分泌療法の定義は,治療編 総説.Ⅴ.4.a.a-1.1)を参照のこと。
解 説
1)二次内分泌療法
(1)LH-RHアゴニスト+フルベストラント+CDK4/6阻害薬の併用療法について
閉経前転移・再発乳癌を含む,フルベストラントにCDK4/6阻害薬の併用の有無を評価した質の高いランダム化比較試験は,パルボシクリブの有効性を検討したPALOMA-3試験と,アベマシクリブの有効性を検討したMONARCH-2試験がある1)2)。
両試験とも閉経前患者に関して,一次内分泌療法を施行中もしくは終了後1カ月以内に病勢進行した転移乳癌と,タモキシフェンによる術後内分泌療法施行中もしくは終了後1年以内に再発を認めた症例を対象とするが,PALOMA-3試験では二次以降の内分泌療法後や前化学療法1レジメン以内が許容されるのに対し,MONARCH-2試験には含まれないという違いがある。
PALOMA-3試験の閉経前サブグループ解析(全症例の20.7%)において,無増悪生存期間(PFS)はパルボシクリブ併用群で有意に改善を認めた(パルボシクリブ群:9.5カ月,プラセボ群:5.6カ月,ハザード比(HR)0.50,95%CI 0.29-0.87)3)。全生存期間(OS)は,HR 1.07(95%CI 0.61-1.86)と延長傾向は認められなかった4)。有害事象の発生頻度は閉経後患者と同様であった。
MONARCH-2試験での閉経前サブグループ(全症例の17.0%)については,PFSで28.6カ月vs 10.26カ月(HR 0.477,95%CI 0.302-0.755)と有意な改善が報告されている5)。OSはアベマシクリブ群では未達であり,プラセボ群では47.31カ月(HR 0.689,95%CI 0.379-1.252)と有意差は認めなかったが,全体集団と類似の改善傾向が示された6)。また有害事象は全体集団と同等であった。
(2023Web改訂、更新情報)二次内分泌療法において,中国のみで行われたdalpiciclib(未承認)+フルベストラントとプラセボ+フルベストラントを比較検討した第Ⅲ相ランダム化試験(DAWNA-1)が報告されている7)。DAWNA-1試験は,一次内分泌療法で6カ月以上経過したのちに進行した患者と,術後内分泌療法の2年経過後から終了後1年以内に再発した患者を対象とし,前化学療法1レジメンが許容された。閉経前サブグループ(全症例の44.3%)において,PFSのHRは0.68(95%CI 0.41–1.14)であった。
以上より,質の高いランダム化比較試験が3つ存在しているが,サブグループ解析であることを考慮し,エビデンスの強さは「中」とした。
益と害のバランスについては,Grade 3以上の有害事象がCDK4/6阻害薬併用群で有意に高いが,併用によるPFS延長の大きさから益が害に勝る可能性が考慮される。また,CDK4/6阻害薬併用による費用の増加に関しては,患者の希望にばらつきが出ることが予想される。
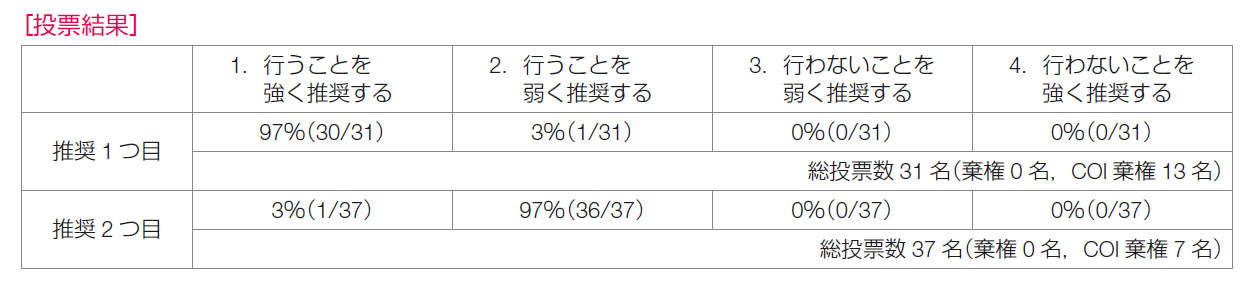
推奨決定会議での投票では,「行うことを強く推奨する」が97%,「行うことを弱く推奨する」が3%であった。
CDK4/6阻害薬によるPFSの延長に関しては,長期ベネフィットが確立されていると考えられ,エビデンスの程度,益と害のバランス,患者の希望などを勘案し,推奨は「LH-RHアゴニスト+フルベストラント+CDK4/6阻害薬の併用療法を行うことを強く推奨する」とした。
一次内分泌療法と二次内分泌療法でのCDK4/6阻害薬併用の有用性を比較したSONIA試験については薬物CQ20参照のこと。
(2)LH-RHアゴニストとアロマターゼ阻害薬などの閉経後に用いる内分泌療法薬との併用療法について
タモキシフェン後の二次治療の閉経前乳癌患者を対象としたランダム化比較試験は,一つ報告されている。これは少数例のランダム化第Ⅱ相試験であり,タモキシフェン前治療歴を有する閉経前ホルモン受容体陽性HER2陰性患者に対して,ゴセレリン単剤に対するゴセレリン+アナストロゾールの併用療法,または,ゴセレリン単剤に対するゴセレリン+フルベストラントの併用療法の有効性を探索した3アームのランダム化比較試験(FLAG試験)である。主要評価項目は,主治医判断のTTP(time to progression)であり,治療開始を起点として,初めての腫瘍の増大による悪化か,死亡(腫瘍増大の有無にかかわらず)をイベントと定義した。この結果,TTPはゴセレリン単剤が13.5カ月であったのに対して,フルベストラント+ゴセレリンが16.3カ月(p=0.049),ゴセレリン+アナストロゾールが14.5カ月(p=0.937)と,フルベストラント併用のTTPが良好であった8)。奏効率は併用療法で高い結果であった。なお,フルベストラントの国内の添付文書では,用法・用量として,閉経前乳癌に対しては,LH-RHアゴニスト投与下でCDK4/6阻害薬と併用することとされている。また,LH-RHアゴニストと閉経後の内分泌療法(アロマターゼ阻害薬,フルベストラント)の有効性を検討した単一アーム前向きコホート研究の結果が報告されている9)10)。これらの試験において,卵巣機能抑制と内分泌療法の併用によってクリニカルベネフィット率を6割前後の症例に認めている。
以上より,当該対象における治療成績は,新規のランダム化比較試験を含めても,少ない症例数の前向きコホート研究が中心であり,エビデンスの強さは「弱」とした。
一般的に内分泌療法は化学療法と比較して副作用が少ないため,益と害のバランスについては,益が勝ると考えられ,卵巣機能抑制を用いて閉経後の内分泌療法を併用することは,患者の希望等を考慮しても望ましい治療オプションである。患者の希望のばらつきは少ないと思われる。
推奨決定会議での投票では,「行うことを強く推奨する」が3%,「行うことを弱く推奨する」が97%であった。
以上より,エビデンスの程度,益と害のバランス,患者の希望などを勘案し,推奨は「卵巣機能抑制を行い,アロマターゼ阻害薬などの閉経後に用いる内分泌療法薬との併用療法を行うことを弱く推奨する」とした。
(2023Web改訂,更新情報)転移乳癌二次~三次,また早期再発一次内分泌療法の閉経前,閉経後AI耐性患者を対象とし,汎AKT阻害薬capivasertibのフルベストラントに対する上乗せ効果を検証した第Ⅲ相ランダム化比較試験(CAPItello-291)に関しては薬物FRQ10を参照。
2)三次治療以降の内分泌療法
一般的に後のラインになるに従って,内分泌療法のクリニカルベネフィットは小さくなってくるが,一次治療,二次治療ともに内分泌療法によるクリニカルベネフィットが得られなかった症例や生命に差し迫った症例でない限り,使用していない機序の内分泌療法を順次使用することも許容される。三次以降の内分泌療法においても卵巣機能抑制を行い閉経後の状態とし,前治療で使われていない薬剤(アロマターゼ阻害薬,フルベストラント+CDK4/6阻害薬の併用療法など)を用いる。ほかに後期ラインで用いられる内分泌療法としてエストラジオールや酢酸メドロキシプロゲステロン(MPA)があるが,エストラジオールは血栓症や腟出血,MPAは血栓症や体重増加などの有害事象の面から上記の内分泌療法施行後に使用する11)~13)。
検索キーワード・参考にした二次資料
薬物CQ18~22の共通の検索として,PubMedで,“Breast Neoplasms”,“Neoplasm Metastasis”,“Neoplasm Recurrence, Local”,“Endocrine therapy”,“tamoxifen”,“toremifene”,“Fulvestrant”,“Aromatase Inhibitor”,“CDK4/6 inhibitor”,“everolimus”,“Buparlisib”,“pictilisib”,“alpelisib”,“AKT inhibitor”のキーワードとその同義語で検索した。医中誌・Cochrane Libraryも同等のキーワードで検索した。検索期間は2016年1月~2021年3月とし,共通の検索結果として1370件がヒットした。検索期間以後を含めハンドサーチを追加後,一次スクリーニングで6件が該当し,二次スクリーニングでMONARCH-2閉経前患者の論文1編を採用した。
参考文献
1)Cristofanilli M, Turner NC, Bondarenko I, Ro J, Im SA, Masuda N, et al. Fulvestrant plus palbociclib versus fulvestrant plus placebo for treatment of hormone-receptor-positive, HER2-negative metastatic breast cancer that progressed on previous endocrine therapy(PALOMA-3):final analysis of the multicentre, double-blind, phase 3 randomised controlled trial. Lancet Oncol. 2016;17(4):425-39. [PMID:26947331]
2)Sledge GW Jr, Toi M, Neven P, Sohn J, Inoue K, Pivot X, et al. MONARCH 2:abemaciclib in combination with fulvestrant in women with HR+/HER2- advanced breast cancer who had progressed while receiving endocrine therapy. J Clin Oncol. 2017;35(25):2875-84. [PMID:28580882]
3)Loibl S, Turner NC, Ro J, Cristofanilli M, Iwata H, Im SA, et al. Palbociclib combined with fulvestrant in premenopausal women with advanced breast cancer and prior progression on endocrine therapy:PALOMA-3 results. Oncologist. 2017;22(9):1028-38. [PMID:28652278]
4)Turner NC, Slamon DJ, Ro J, Bondarenko I, Im SA, Masuda N, et al. Overall survival with palbociclib and fulvestrant in advanced breast cancer. N Engl J Med. 2018;379(20):1926-36. [PMID:30345905]
5)Neven P, Rugo HS, Tolaney SM, Iwata H, Toi M, Goetz MP, et al. Abemaciclib plus fulvestrant in hormone receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer in premenopausal women:subgroup analysis from the MONARCH 2 trial. Breast Cancer Res. 2021;23(1):87. [PMID:34425869]
6)Sledge GW Jr, Toi M, Neven P, Sohn J, Inoue K, Pivot X, et al. The effect of abemaciclib plus fulvestrant on overall survival in hormone receptor-positive, erbb2-negative breast cancer that progressed on endocrine therapy-MONARCH 2:a randomized clinical trial. JAMA Oncol. 2020;6(1):116-24. [PMID:31563959]
7)Xu B, Zhang Q, Zhang P, Hu X, Li W, Tong Z, et al, Dalpiciclib or placebo plus fulvestrant in hormone receptor-positive and HER2-negative advanced breast cancer: a randomized, phase 3 trial. Nat Med. 2021 : 27 (11) : 1904-1909. [PMID:34737452]
8)Kim JY, Im SA, Jung KH, Ro J, Sohn J, Kim JH, et al;breast cancer committee of Korean Cancer Study Group(KCSG). Fulvestrant plus goserelin versus anastrozole plus goserelin versus goserelin alone for hormone receptor-positive, HER2-negative tamoxifen-pretreated premenopausal women with recurrent or metastatic breast cancer(KCSG BR10-04):a multicentre, open-label, three-arm, randomised phase Ⅱ trial(FLAG study). Eur J Cancer. 2018;103:127-36. [PMID:30223226]
9)Bartsch R, Bago-Horvath Z, Berghoff A, DeVries C, Pluschnig U, Dubsky P, et al. Ovarian function suppression and fulvestrant as endocrine therapy in premenopausal women with metastatic breast cancer. Eur J Cancer. 2012;48(13):1932-8. [PMID:22459763]
10)Nishimura R, Anan K, Yamamoto Y, Higaki K, Tanaka M, Shibuta K, et al. Efficacy of goserelin plus anastrozole in premenopausal women with advanced or recurrent breast cancer refractory to an LH-RH analogue with tamoxifen:results of the JMTO BC08-01 phase Ⅱ trial. Oncol Rep. 2013;29(5):1707-13. [PMID:23446822]
11)Martoni A, Longhi A, Canova N, Pannuti F. High-dose medroxyprogesterone acetate versus oophorectomy as first-line therapy of advanced breast cancer in premenopausal patients. Oncology. 1991;48(1):1-6. [PMID:1824798]
12)Abrams J, Aisner J, Cirrincione C, Berry DA, Muss HB, Cooper MR, et al. Dose-response trial of megestrol acetate in advanced breast cancer:cancer and leukemia group B phase Ⅲ study 8741. J Clin Oncol. 1999;17(1):64-73. [PMID:10458219]
13)Ellis MJ, Gao F, Dehdashti F, Jeffe DB, Marcom PK, Carey LA, et al. Lower-dose vs high-dose oral estradiol therapy of hormone receptor-positive, aromatase inhibitor-resistant advanced breast cancer:a phase 2 randomized study. JAMA. 2009;302(7):774-80. [PMID:19690310]