乳癌診療ガイドライン2018年版作成にあたって
―医師と患者のShared Decision Makingのサポートツールとしてのガイドラインを目指して―
1.乳癌診療ガイドラインのこれまでの経緯と今回改訂のコンセプト
2002(平成14)年に厚生労働科学研究費補助金 研究報告書として作成された“科学的根拠に基づく乳がん診療ガイドライン作成に関する研究”が現在の乳癌診療ガイドラインの始まりである。その後,ガイドラインの作成は日本乳癌学会(以下,本学会)に移管され,臨床試験検討委員会が担当して2004年と2005年にそれぞれの分野別(薬物療法,外科療法,放射線療法,検診・診断,疫学・予防)に5つの冊子として初版が刊行された。そして薬物療法は3年ごとの2回の改訂,その他4冊は3年後の1回の改訂を経て,2011年に現在の体裁と同じ,治療編と疫学・診断編の2分冊として発刊された。その後も日々蓄積されるデータと標準治療の変化に対応すべく改訂の間隔を2年ごととして,2013年・2015年と改訂版を発刊してきた。
乳癌診療ガイドラインは初期の頃から,科学的根拠に基づいたガイドラインとして,多くの臨床試験等のデータのレビューを行い,そのデータの「エビデンスレベル(試験デザインに基づいたエビデンスの評価)」によって信頼性を担保したうえで,エキスパートの作成委員が協議のうえ,ガイドラインの執筆を行い,推奨に迷うクリニカルクエスチョン(CQ)では,作成委員会の中で投票が行われ,A,B,C1,C2,Dの「推奨グレード」を決定してきた。2004年当時のガイドライン黎明期に,このような作成手順は他の領域からも高く評価され,その後の多くのガイドライン作成に影響を与えたことは論を待たない。また1年遅れで作成してきた“患者向けガイドライン”は,作成委員の中に乳癌経験者や看護師,薬剤師など,多職種が参画して作成するガイドラインとして,診療の現場で活用され,患者さんに信頼される情報源として重要な位置を占めてきた。
しかし近年,世界的なガイドライン作成の標準化の流れの中で,今までの乳癌診療ガイドライン作成手順は少し時代遅れとなってきていた。前版までのガイドラインは,日常臨床で重要なテーマをCQとして決定し,これに関する文献を網羅的に検索し,文献の批判的吟味の後に本文を作成し,委員相互のレビューの後に,推奨グレードの決定および最終版の完成という手順をとってきた。もちろん前版までの乳癌診療ガイドラインも完成度の高いガイドラインとして高く評価され,日本の乳癌診療の均てん化に大きく貢献してきたことは確かである。しかし,今までのガイドラインの記載の中でやや欠けていた点に「益と害のバランス」という視点がある。
今回のガイドラインでは,最初に「益と害」の具体的な指標としてのアウトカム(例えば,「益」として「全生存期間」,「害」として「毒性」など)を,あらかじめCQごとに数個設定し,それぞれのアウトカムに1~9点までの重要度の点数を与えることで,アウトカムの「重み付け」をする。この最初に設定した「益と害」の具体的なアウトカムとその重み付けが,それぞれのCQの最終的な「推奨とその強さ」の決定に大きな影響を与えることになる。この一連の作業は,前版までのガイドライン作成過程と比べて,より論理的であり,作成者の判断の偏りが入る余地が少ないガイドラインの作成手順であると考える。
ガイドラインは標準的な診療の道標であるとともに,困ったときに考える材料を提供するツールでもある。我々の日常診療は介入(診断,外科療法,放射線療法,薬物療法など)の連続であり,どの手段をとるのかの判断の際に,無意識に益と害を考慮して手段を選んでいるはずである。しかし本来,介入手段を決定する際には,医師個人の判断だけでなく,益と害のバランスを患者さんと共有することが大切である(shared decision making)。そこで,今回の乳癌診療ガイドライン改訂にあたっては,医師と患者がshared decision makingをするためのツールとしてのガイドライン作成をコンセプトに作業を進めた。作成手順として参考にしたのが,「Minds診療ガイドライン作成マニュアルVer. 2.0(2016. 3. 15)」である。
2.本ガイドライン(2018年版)の策定手順
今回の改訂を行うにあたり,新たな委員長および委員会メンバーが任命され,2016年8月に作業を開始した。第1回の診療ガイドライン委員会(2016年8月18日)において今回の改訂の骨子と作業手順を示すとともに,作業手順の大幅な変更と作業量から1年での改訂作業は困難と判断して2018年の発刊を目指すことを決定した。そして最初に委員全員参加の全体方針会議を開催し(2016年9月4日),改訂の骨子を示し作業方針を確認した。以降は「薬物療法」「外科療法」「放射線療法」「疫学・予防」「検診・画像診断」「病理診断」の小委員会に分かれて作業を行った。
1)改訂作業の骨子
今までのガイドラインでは,ランダム化比較試験(RCT)やメタアナリシスでポジティブな結果が出ているものは,レベル1のエビデンスがあるとして多くの場合“強く推奨する”としていた。しかし今回はCQごとに複数のアウトカム(益と害の両面から各3~6項目程度)を設定して,そのアウトカムごとに臨床の重要度を決定した。そしてCQに関連したキーワードから文献検索・抽出の後に,複数のアウトカムごとに定量的あるいは定性的システマティック・レビューを行い,益と害のバランスを考慮してCQに対する推奨の強さを各小員会で決定した。各小員会から提案された推奨文および推奨の強さを,推奨決定会議での議論・投票で最終決定した。この最終決定に基づき,担当委員が解説文の執筆を行い,相互レビューのうえで最終版を完成させている。
2)ガイドラインの構成
総説:治療の基本的概念,言葉の定義,歴史的流れ,教科書的な話題などを記載。
BQ(バックグランドクエスチョン):旧来のガイドラインで標準治療として位置付けられ,専門医でなくても遵守してほしい内容,および日常臨床で判断に迷う内容で本来CQで扱うべき内容であるが,古いデータしかなく,今後も新たなエビデンスが出てくることはないと予想される内容もBQと位置付け概説している。BQの構成:BQ文,ステートメント,解説。
CQ(クリニカルクエスチョン):日常臨床で判断に迷うテーマを取り上げ,定量的あるいは定性的システマティック・レビューを行い,推奨決定会議の投票を経て,推奨および推奨の強さを決定し,その内容について,推奨決定会議の議論のポイント等も踏まえて解説している。CQの構成:CQ文,推奨,推奨の強さ,エビデンスの強さ,合意率,解説。
FQ(フューチャーリサーチクエスチョン):CQとして取り上げるには,データが不足しているが,今後の重要な課題と考えられるCQについて,現状の考え方を説明している。FQの構成:FQ文,ステートメント,解説。
3)具体的な作業手順
(1)BQ,CQ,FQの設定:領域ごとに協議して,2015年版のCQを照合しつつ整理し,取り上げるCQおよびBQ・FQを決定した。
(2)CQの作成手順:CQに関してのみ以下の手順(3)~(18)を行った。BQとFQのステートメントについては診療ガイドライン委員会内のディスカッションにて決定しており,原則として手順(9)「エビデンスの評価」以降の作業は行っていない。
(3)CQの構成要素:CQの構成要素はPICO〔P:Patients(介入を受ける対象),I:Intervention(推奨するかどうか検討する介入),C:Comparisons(Iと比較したい介入),O:Outcome(アウトカム)〕と呼ばれる形式で抽出した。
(4)アウトカムの設定:各CQに対して,数個のアウトカムを設定した。このアウトカムは「益」と「害」が必ず含まれるように設定しなければならない。前述したように,アウトカムには1~9点までの重要度の点数を付けて,それぞれのアウトカムの「重み付け」をする。この「重み付け」は,「推奨とその強さ」を決定する際の判断材料になる。
(5)エビデンスの収集:各委員は担当CQごとに関連するキーワードを設定し,協力いただいた日本医学図書館協会に送付して検索式を立て,網羅的に検索を行った。検索データベースはPubMed,医中誌Web,Cochrane Libraryを用いた。各CQの検索式の詳細は,本学会のホームページ(http://jbcs.gr.jp/)に掲載する。
(6)一次スクリーニング:各委員は一次スクリーニングとして文献リストの論題・抄録・索引語から明らかにCQに合致していない文献を除外,必要に応じてキーワードの追加,検索式の変更を行い再度スクリーニングを行った。
(7)二次スクリーニング:次に各委員は二次スクリーニングとして,一次スクリーニングで残した文献の本文を読み,アウトカムごとに採用文献を決定した。選択基準は原則としてランダム化比較試験とし,該当文献がない場合は観察研究も含めることとした。
(8)ハンドサーチ:さらにハンドサーチで重要文献を追加して,可能な限り漏れのない検索を心掛けた。
(9)エビデンスの評価(個々の論文の評価):アウトカムごとにまとめられた文献集合の個々の論文について,研究デザイン(介入研究,観察研究)ごとに,バイアスリスク(risk of bias 9要素:選択バイアス,実行バイアスなど),非直接性(indirectness:従来の「外的妥当性」,「一般化可能性」に相当)を評価する。
(10)エビデンス総体(body of evidence)(=エビデンスの強さ)の評価:1つのアウトカムで選択抽出された複数の論文をまとめて,エビデンスの総体を評価する。評価の方法は,研究デザインによって分類(RCT群,観察研究群)してまとめ,改めて,①バイアスリスク(risk of bias 9要素),②非直接性(indirectness)を評価し,これに加えて,③非一貫性(inconsistency),④不精確(imprecision),⑤出版バイアス(publication bias)などを評価する。RCTでは「エビデンスの強さ」を“強”から始めて,上記①~⑤を考慮して,必要であれば段階を下げて最終評価とした。観察研究ではエビデンスの強さの評価を,①効果が大きい(large effect),②用量反応勾配あり(dose―dependent gradient),③可能性のある交絡因子が提示された効果を減弱させている(plausible confounder)の要素で優れたものは1段階上げるなどの評価を行った。
(11)エビデンスの強さの分類:エビデンスの評価の判定は,1つひとつのアウトカムに対して,関係論文内容を上記規定で評価集約し,最終的に1つのCQに対する「エビデンス総体」として「エビデンスの強さ」を「強」,「中」,「弱」,「とても弱い」の4段階に分類した。この分類が益と害の大きさとバランスに対する確実性を評価していることになる。
なお,前版までのガイドラインでは「エビデンスレベル」という表現を用いてきたが,「エビデンスレベル」と「エビデンスの強さ」は同じ意味ではない。従来用いられてきた「エビデンスレベル」という表現は,ランダム化第Ⅲ相比較試験やコホート試験といった「試験デザイン」のみに基づいており,試験そのものの「質」を問うものではなかった。一方,今回のガイドラインから使用している「エビデンスの強さ」は,バイアスリスクなど,手順(9)(10)で記載したような,規定の因子を1つずつ丹念に評価したうえで決定される。したがって,ランダム化第Ⅲ相試験が複数あっても,その臨床試験の「質」によって,「エビデンスの強さ」は「強」ではなく「中」になることもある。
(12)エビデンスの統合〔定性的システマティック・レビューと定量的システマティック・レビュー(メタアナリシス)〕:各CQのアウトカムごとに,定量的システマティック・レビューが可能なものは,ガイドライン作成委員が,このガイドラインのために独自にメタアナリシスを行い評価した。この点は前版までのガイドラインと非常に大きく異なる点である。定量的評価(メタアナリシス)ができないものは,論理性・確実性などを文脈から評価する定性的システマティック・レビューのみを行った。各CQのシステマティック・レビューの詳細は,本HPに掲載する。
(13)推奨の作成:各領域の小委員会で,CQごとに,①アウトカム全般に関するエビデンスの強さ,②益と害のバランス,③患者の価値観や好み,④コスト(=コストに関する報告やガイドラインがあれば利用するが,なければ評価に入れない)の4要素を考慮して「推奨」と「推奨の強さ」を決定し,推奨文を推奨決定会議に提出した。推奨の作成に際して本邦での保険承認の有無は特段に考慮することはなく,上記4要素によって決定した。
(14)推奨決定会議の開催:各小委員会(薬物療法,外科療法,放射線療法,疫学・予防,検診・画像診断,病理診断)で提案された「推奨」と「推奨の強さ」について推奨決定会議で投票を行い(無記名,自動集計),それぞれのCQについて,最終的な「推奨」と「推奨の強さ」を決定した。
(15)推奨決定会議の参加者とvotingのルール:推奨決定会議に参加したのは,各小委員長(各分野の専門家)と乳癌経験者2名,薬剤師1名,看護師1名,ガイドライン委員長,副委員長の12名である。投票に際しては,各委員はCQごとに経済的COI,学術的COI(臨床試験,治験等への関与)を自己申告し,COIありの場合は,2017年の本学会COI基準に従い,当該CQの投票を棄権することで意見の偏りを防ぐ努力をした。この理由によって投票者総数は変動した。このため推奨文には合意率(%)に加えて,投票実数をカッコ内に記載した。また1回目のvotingで合意率が70%に至らなかったCQは再度の議論(説明の追加や,誤解の解消など)のうえ,3回目までのvotingを行い,70%を超えるvoting結果を採用したが,3回目までに70%を超える一致をみなかったCQは“合意に至らず”という結論とするルールを決めて行った。合意に至らなかったCQなどでは,解説文に推奨決定会議での意見の相違なども記載した。
(16)解説文の執筆:推奨決定会議の結果を受け,各小委員会でCQの解説文を執筆した。前版のガイドラインと同様にCQ,推奨文,背景・目的,解説文という流れは同じであるが,解説文にはエビデンスの強さとその根拠,益と害のバランス,患者さんの希望に一貫性はあるか(多様性はあるか),経済的な観点(国の視点ではなく,あくまで個人の),推奨決定会議の議論の内容(意見の相違点,日本の臨床で注意する点など)を記載して,より実践的な内容になっている。
(17)評価委員会による評価:執筆の後,評価委員会で独立性をもって,本ガイドラインの作成プロセスが評価された(AGREEⅡで評価)。
(18)理事会の承認とWEB版:推奨決定会議の後に,CQごとの推奨文・合意率などが出た段階で,理事会に提示して意見をいただき,評価委員会の後に理事会での承認を得て最終版が確定した。出版と同時期に本学会ホームページhttp://jbcs.gr.jp/に自由に閲覧可能なWEB版を掲載する。
3.推奨の強さ,エビデンスグレード,エビデンスの強さ,合意率
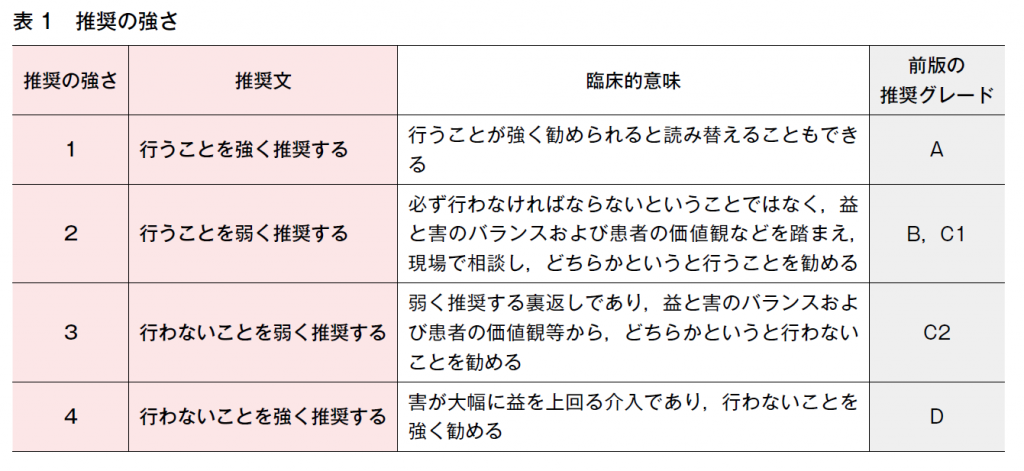
今回の推奨の強さは,前回までの科学的根拠だけでなく,日常臨床で介入することによって起こる益と害のバランスおよび患者の希望の一貫性,経済的視点等を踏まえて,行うことをどの程度推奨するのかを決定した。推奨の強さは「Minds診療ガイドライン作成マニュアルVer. 2.0」を遵守して4段階に分けた(表1)。前版までの推奨グレードA,B,C1,C2,Dとの大まかな対応も示す。
前版と同様に,疫学・予防のCQの多くは介入のCQではなく,日常生活において気を付けるべきことをCQとして挙げている。よって,行う,行わない等を推奨する立場をとらずに,あくまで科学的な根拠の確からしさをエビデンスグレードとして明示することにした(表2)。
「エビデンスの強さ」は推奨文の中に「強」,「中」,「弱」,「とても弱い」の4段階で表示した(表3)。CQごとに設定したアウトカムすべてにおいて,全体的なエビデンスが強いほど推奨は“強く”なる。逆に全体的なエビデンスが弱いほど,推奨は“弱く”なる。エビデンスの強さの決定の基本原則は,その治療効果推定値に対する確信が,その推奨を支持するうえでどの程度十分かを表している。
推奨決定会議の合意率(%)を記載している理由は,例えば同じ「弱く推奨する」でも,合意率100%と73%では意味合いが違うためである。少数ではあるが強く推奨に傾いているのか,弱く推奨しないほうに傾いているのかを知ることで,実際の治療介入の参考にしていただきたい。また一度の投票で決定されたのか,複数回の投票で合意に至ったのかで意見の相違があるか否かも理解できるようになっている。つまり,現場でshared decision makingをする際に,専門家の間でも意見が分かれていることを患者さんと共有したうえで,最終介入の手段を決定していただければと考えている。3回の投票で合意に至らなかったものは,「合意率:合意に至らず」と記載した。このようなCQは推奨の強さを1~2,2~3,3~4のように幅をもたせた記載としている。どこで意見が分かれたのかを知ることができるので介入手段の決定の際に参考にしてほしい。


4.保険承認,保険適用状況による記載の工夫
・保険承認,保険適用の状況により特に薬剤については表記を変えて記載している。
・乳癌に対して適応のある薬剤の薬剤名はすべて片仮名表記とし,一般名を用いた。例:タモキシフェン
・日本ではどの疾患に対しても使用が許可されていない薬剤については薬剤名を英名表記とし,その後に(未承認)と加えた。例:neratinib(未承認)
・日本では乳癌以外の他の疾患に対しては使用が許可されているものの乳癌には許可されていない薬剤については,薬剤名は片仮名表記とし,その後に(保険適用外)と加えた。例:ラロキシフェン(保険適用外)
5.評 価
2018年2月3日,診療ガイドライン評価委員会によりAGREEⅡに従って評価を受けた。また評価委員会より提案された修正点を,可能な限り原稿に反映させた後,最終案が承認された。2018年3月30日の本学会理事会で最終的な承認がなされ発刊が決定した。今後は本学会QI委員会と共同して,本ガイドライン発刊による行動変容を調査研究することも考えられている。
6.資金源
本ガイドライン作成にあたり掛かる費用(交通費,会議費,印刷費,文献検索費等)は,すべて本学会より拠出されており,特定の企業等からの提供は受けていない。
7.利益相反
本ガイドラインの発刊は,本学会の承認を受けた事業であり,他のいかなる団体からの影響も受けていない。本学会はガイドライン作成に関与した委員(診療ガイドライン委員,各小委員会の作成メンバーおよび協力委員)の利益相反の状況を確認した。推奨決定会議での投票の際には,利益相反(経済的COI,学術的COI)を自己申告し,COIありの場合は当該CQの投票を棄権することで意見の偏りを防ぐ努力をした。各委員のCOIは本ガイドラインCOIページに記載されている。
8.今後の改訂
診療ガイドライン委員会では,次回の改訂版出版は2021年(3年後)を予定している。しかし目まぐるしく進歩する医療の中で,エビデンスの創出は日進月歩である。この進歩に合わせるように,半年ごとにエビデンスの蓄積を確認して,必要に応じてWEB版の改訂(追加,修正等)を進める予定である。また本ガイドラインには,内容をわかりやすく解説した“患者向けガイドライン”が用意されており,そちらも1年後に改訂版が出版される予定である。
9.おわりに
多様化する乳癌診療の中で,医師および医療関係者と患者さんの間の関係は,主従ではなく,仲間でもなく,相互に信頼しあう同志の関係性であるべきと考える。乳癌診療の現場では,常に介入をするための決断が求められている。検診をすべきかどうか? 精密検査に何をするべきか? 乳癌と診断されたらどのような治療を選ぶべきか? 治療前に何の検査が必要なのか? 等々,毎日が患者さんに向き合い,介入のための決断の連続である。その際,考えるべきは,介入をしたことで患者さんが受ける益(良い面)と害(悪い面)である。医療の現場で行う介入は,すべて良い面だけの介入はほとんどなく,程度の違いはあれ必ず害の側面をもつ。介入を決定するにあたり,益と害の両面を患者さんと話し合い介入を決定するプロセス(shared decision making)こそ,相互に信頼する同志の関係性を構築するうえで重要である。
今回のガイドラインはこのような乳癌治療の現場の中で,医療者が患者さんに向き合う際のツールとして使用していただきたい。ガイドラインは絶対的なルールブックではない。解説文を読んで患者さんに“強く推奨する”と説明をしたとしても,個々の患者さんの価値観によっては,逆の選択になる場合も考えられる。そのような現場の個々の価値判断は尊重されるべきであるが,その前提としてガイドラインで記載された内容の情報が,患者さんに正しく伝えられていることが必須である。臨床現場で本ガイドラインが活用されることによって,より的確な診療が広まり,その結果,少しでも多くの患者さんが救われることを期待したい。
今回のガイドラインは,大幅な改訂作業を行ったことから,現場からの様々な意見が予想される。前版の序文で述べられているように,現場から支持され使用されるものでなければ意味がない。使いやすく,有益なガイドラインにしていくために,引き続き皆様からの声が不可欠である。ガイドラインに関するご意見,ご指摘等は本学会ホームページで受け付けているので,皆様からの忌憚のないご意見をお願いしたい。
最後に本ガイドライン改訂に多くの時間を費やし尽力くださった委員の先生方,改訂作業の最初から多くのアドバイス等をいただいた日本医学図書館協会の河合富士美氏,国際医療福祉大学の吉田雅博教授に深謝するとともに,診療ガイドライン評価委員会,本学会理事各位,ならびに編集担当の金原出版佐々木瞳氏,宇野和代氏に,この場を借りて御礼申し上げる。
[診療ガイドライン委員会委員長 岩田 広治]


